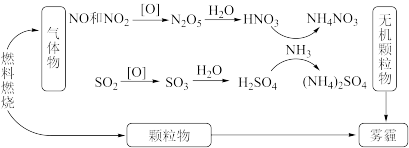
我国“蓝天保卫战”成果显著,肆虐的雾霾逐渐被遏止。科学家研究发现含氮化合物和含硫化合物在形成雾霾时与大气中的氨有关,转化关系如图所示:
回答下列问题:
(1)从物质分类的角度看,图中的物质属于酸性氧化物的有_______ (写化学式)。
(2)写出 转化为
转化为 的化学方程式:
的化学方程式:_______ 。
(3)工业上合成氨的化学方程式为_______ 。
(4)实验室长期保存浓硝酸,需使用棕色试剂瓶,并放置在阴凉处,其原因为_______ (用化学方程式表示)。
(5)氨与一氧化氮(NO)在一定条件下反应可生成对空气无污染的物质,该反应的化学方程式为_______ 。

回答下列问题:
(1)从物质分类的角度看,图中的物质属于酸性氧化物的有
(2)写出
 转化为
转化为 的化学方程式:
的化学方程式:(3)工业上合成氨的化学方程式为
(4)实验室长期保存浓硝酸,需使用棕色试剂瓶,并放置在阴凉处,其原因为
(5)氨与一氧化氮(NO)在一定条件下反应可生成对空气无污染的物质,该反应的化学方程式为
21-22高一下·山西太原·阶段练习 查看更多[4]
山西省太原师范学院附属中学、太原市师苑中学校2021-2022学年高一下学期3月月考化学试题(已下线)1.1.3 物质性质与变化(好题帮)-备战2023年高考化学一轮复习考点帮(新教材新高考)(已下线)考点11 氮及其化合物-备战2023年高考化学一轮复习考点帮(全国通用)(已下线)考点11 氮及其化合物(核心考点精讲精练)-备战2024年高考化学一轮复习考点帮(全国通用)
更新时间:2022-03-25 10:33:20
|
相似题推荐
填空题
|
适中
(0.65)
名校
【推荐1】现有下列十种物质:①HCl;②NaHCO3;③K2SO4溶液;④CO2;⑤蔗糖晶体;⑥Ca(OH)2;⑦氢氧化铁胶体;⑧NH3·H2O;⑨空气;⑩Al2(SO4)3。
(1)属于分散系的是_______ ,NH3·H2O属于_______ (填“酸”、“碱”、“盐”或“氧化物”)。
(2)CO2属于酸性氧化物,SiO2也属于酸性氧化物,请写出SiO2和CaO反应的化学方程式:_______ 。
(3)若⑦中混有少量的③,提纯的方法是:_______ 。
(4)3.6g碳在一定量的氧气中燃烧,反应后生成一氧化碳和二氧化碳混合气体的平均摩尔质量是32g·mol-1,则生成的一氧化碳的质量是_______ 。
(5)二氧化硫、氢气、二氧化碳组成的混合气体在同温、同压下与笑气(N2O)的密度相同,则该混合气体中二氧化硫、氢气、二氧化碳的体积比可能为_______ (填字母)。
(1)属于分散系的是
(2)CO2属于酸性氧化物,SiO2也属于酸性氧化物,请写出SiO2和CaO反应的化学方程式:
(3)若⑦中混有少量的③,提纯的方法是:
| A.蒸馏(分馏) | B.萃取 | C.渗析 | D.分液 |
(5)二氧化硫、氢气、二氧化碳组成的混合气体在同温、同压下与笑气(N2O)的密度相同,则该混合气体中二氧化硫、氢气、二氧化碳的体积比可能为
| A.42:20:13 | B.22:1:14 | C.13:8:13 | D.21:10:12 |
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】价类二维图是以元素化合价为纵坐标,以物质类别为横坐标的二维平面图像。如图为氯元素价类二维图,据此回答下列问题:

(1)根据化合价和物质类别写出有关物质的化学式:①HCl、②Cl2、③________ 、④_______ 、⑤NaCl、⑥NaClO。
(2)工业上用水吸收HCl气体来生产质量分数为36.5%、密度为1.19g/mL的盐酸,该盐酸的物质的量浓度为_______ ;若用该盐酸配制220mL0.5mol•L-1稀盐酸除玻璃棒、胶头滴管还需用到_______ (填字母)。
a.10mL量筒 b.20mL量筒 c.100mL容量瓶 d.250mL容量瓶
(3)用NaOH溶液吸收②Cl2可制备某漂白液。已知1molCl2可反应生成等物质的量的NaCl和NaClO,则该反应化学方程式为:_______ ;NaClO在水溶液中的电离方程式为:_______ 。
(4)已知:MnO2+4HCl(浓) MnCl2+Cl2↑+2H2O。实验室用8.7gMnO2(Mr为87)与100mL11.9mol•L-1盐酸混合共热,若MnO2完全反应则生成Cl2在标准状况下的体积为
MnCl2+Cl2↑+2H2O。实验室用8.7gMnO2(Mr为87)与100mL11.9mol•L-1盐酸混合共热,若MnO2完全反应则生成Cl2在标准状况下的体积为_______ ,反应消耗HCl的物质的量为_______ ,反应后溶液中c(Cl-)为_______ (溶液的体积变化忽略不计)。

(1)根据化合价和物质类别写出有关物质的化学式:①HCl、②Cl2、③
(2)工业上用水吸收HCl气体来生产质量分数为36.5%、密度为1.19g/mL的盐酸,该盐酸的物质的量浓度为
a.10mL量筒 b.20mL量筒 c.100mL容量瓶 d.250mL容量瓶
(3)用NaOH溶液吸收②Cl2可制备某漂白液。已知1molCl2可反应生成等物质的量的NaCl和NaClO,则该反应化学方程式为:
(4)已知:MnO2+4HCl(浓)
 MnCl2+Cl2↑+2H2O。实验室用8.7gMnO2(Mr为87)与100mL11.9mol•L-1盐酸混合共热,若MnO2完全反应则生成Cl2在标准状况下的体积为
MnCl2+Cl2↑+2H2O。实验室用8.7gMnO2(Mr为87)与100mL11.9mol•L-1盐酸混合共热,若MnO2完全反应则生成Cl2在标准状况下的体积为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】根据所学知识回答下列问题:
(1)下列试剂瓶中盛放的化学试剂为氧化物的是_______ (填标号)。
(2)科学家曾用DNA制造出一种臂长只有7 nm的纳米级镊子,这种镊子能夹起分子或原子,并将它们随意组合。下列分散系中分散质的微粒直径与纳米粒子的数量级不相同的是_______ (填标号)。
a.有色玻璃 b.澄清石灰水 c.雾
(3)下列物质属于酸性氧化物的是_______ (填标号,下同),属于盐的是_______ 。
① ②
② ③CO④
③CO④ ⑤
⑤ (葡萄糖)⑥
(葡萄糖)⑥ ⑦石墨
⑦石墨
(4)化学计量是化学定量研究的基础:
①室温下,某密闭容器中盛有 、
、 、
、 的混合气体,通过电火花点燃后,容器内三种气体恰好完全反应,冷却至室温后得到质量分数为7.3%的盐酸,则容器中
的混合气体,通过电火花点燃后,容器内三种气体恰好完全反应,冷却至室温后得到质量分数为7.3%的盐酸,则容器中 、
、 、
、 的体积比为
的体积比为_______ 。
②标准状况下V L氨气溶解在a L水中(水的密度近似为1 g·cm );所得溶液的物质的量浓度为c mol·L
);所得溶液的物质的量浓度为c mol·L ,则该溶液的密度为
,则该溶液的密度为_______ g·cm (用含V、a、c的式子表示)。
(用含V、a、c的式子表示)。
③200 mL的 溶液中,含
溶液中,含 的质量为1.08 g,在该溶液中加入300 mL 0.1 mol·L
的质量为1.08 g,在该溶液中加入300 mL 0.1 mol·L
 溶液,反应后溶液中
溶液,反应后溶液中 的物质的量浓度为
的物质的量浓度为_______ mol·L (不考虑溶液混合时体积的变化)。
(不考虑溶液混合时体积的变化)。
(1)下列试剂瓶中盛放的化学试剂为氧化物的是
| 化学试剂 | 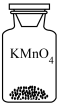 |  | 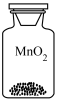 |  |
| 选项 | A | B | C | D |
a.有色玻璃 b.澄清石灰水 c.雾
(3)下列物质属于酸性氧化物的是
①
 ②
② ③CO④
③CO④ ⑤
⑤ (葡萄糖)⑥
(葡萄糖)⑥ ⑦石墨
⑦石墨(4)化学计量是化学定量研究的基础:
①室温下,某密闭容器中盛有
 、
、 、
、 的混合气体,通过电火花点燃后,容器内三种气体恰好完全反应,冷却至室温后得到质量分数为7.3%的盐酸,则容器中
的混合气体,通过电火花点燃后,容器内三种气体恰好完全反应,冷却至室温后得到质量分数为7.3%的盐酸,则容器中 、
、 、
、 的体积比为
的体积比为②标准状况下V L氨气溶解在a L水中(水的密度近似为1 g·cm
 );所得溶液的物质的量浓度为c mol·L
);所得溶液的物质的量浓度为c mol·L ,则该溶液的密度为
,则该溶液的密度为 (用含V、a、c的式子表示)。
(用含V、a、c的式子表示)。③200 mL的
 溶液中,含
溶液中,含 的质量为1.08 g,在该溶液中加入300 mL 0.1 mol·L
的质量为1.08 g,在该溶液中加入300 mL 0.1 mol·L
 溶液,反应后溶液中
溶液,反应后溶液中 的物质的量浓度为
的物质的量浓度为 (不考虑溶液混合时体积的变化)。
(不考虑溶液混合时体积的变化)。
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】元素①~⑧在元素周期表中的位置如图,回答有关问题:
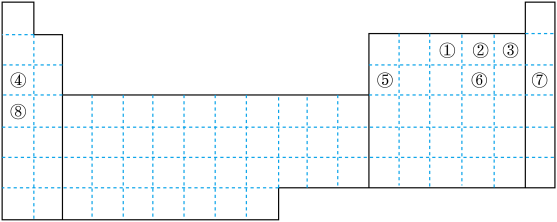
(1)画出⑦的原子结构示意图___________ 。
(2)写出②含有10个中子的核素的化学符号___________ 。
(3)表中②、③、⑥对应的简单离子半径由小到大的顺序为___________ (填离子符号)。
(4)请写出①的氢化物发生催化氧化的化学方程式___________ 。
(5)请写出元素①~⑧中能形成两性氢氧化物的元素对应的单质与⑧的最高价氧化物的水化物反应的离子方程式___________ 。

(1)画出⑦的原子结构示意图
(2)写出②含有10个中子的核素的化学符号
(3)表中②、③、⑥对应的简单离子半径由小到大的顺序为
(4)请写出①的氢化物发生催化氧化的化学方程式
(5)请写出元素①~⑧中能形成两性氢氧化物的元素对应的单质与⑧的最高价氧化物的水化物反应的离子方程式
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】氮及其化合物在自然界中存在循环,请回答下列问题:
(1)氮元素在周期表中的位置是_______ 。
(2)氨气分子的结构式为_______ ,N2的电子式为_______ 。
(3)CN-中N元素显-3价,说明非金属性N_______ C(填“>”或“<”),请写出一个能比较N和C非金属性强弱的化学事实:_______ 。
(4)NO2是燃油汽车尾气中的主要污染物之一。
①在催化剂和加热条件下,NO2与NH3可反应生成无害物质,请写出反应的化学方程式:_______ 。
②实验室可用烧碱溶液吸收NO2和NO,(已知2NO2+2NaOH=NaNO2+NaNO3+H2O,NO2+NO+2NaOH=2NaNO2+H2O),当消耗100mL0.5mol·L-1的烧碱溶液时,共吸收混合气体_______ L(标准状态)。
(5)氨水是一种很好的氮肥,常温下测定0.1mol·L-1氨水溶液,其OH-浓度小于0.1mol·L-1,其原因是_______ (用电离方程式解释),常见氮肥种类有_______ (列举两个)。
(1)氮元素在周期表中的位置是
(2)氨气分子的结构式为
(3)CN-中N元素显-3价,说明非金属性N
(4)NO2是燃油汽车尾气中的主要污染物之一。
①在催化剂和加热条件下,NO2与NH3可反应生成无害物质,请写出反应的化学方程式:
②实验室可用烧碱溶液吸收NO2和NO,(已知2NO2+2NaOH=NaNO2+NaNO3+H2O,NO2+NO+2NaOH=2NaNO2+H2O),当消耗100mL0.5mol·L-1的烧碱溶液时,共吸收混合气体
(5)氨水是一种很好的氮肥,常温下测定0.1mol·L-1氨水溶液,其OH-浓度小于0.1mol·L-1,其原因是
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】氮元素的化合物种类繁多。请结合以下工业制硝酸的原理示意图回答含氮化合物的相关问题:

(1)与氮氧化物有关的全球性大气环境问题有_______(填字母序号)。
(2)下列有关NH3的说法,不正确的是_______(填字母序号)。
(3)如图是喷泉实验装置,在烧瓶中充满干燥气体,胶头滴管及烧杯中分别盛有相同液体。下列组合能形成喷泉的是_______(填字母序号)。
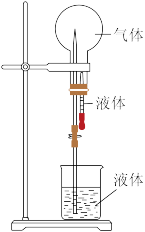
(4)请写出氧化炉中反应的化学方程式_______ 。
(5)实验室制取NH3的化学方程式_______ ,检验氨气是否收集满的方法_______ 。

(1)与氮氧化物有关的全球性大气环境问题有_______(填字母序号)。
| A.酸雨 | B.沙尘暴 | C.光化学烟雾 | D.白色污染 |
| A.工业合成NH3属于人工固氮 | B.NH3可用来生产尿素等氮肥 |
| C.NH3可用浓硫酸或无水氯化钙干燥 | D.实验室用向下排空气法收集氨气 |

| A.HCl与水 | B.Cl2与饱和氯化钠溶液 |
| C.SO2与NaOH溶液 | D.CO2与水 |
(5)实验室制取NH3的化学方程式
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】“钠碱法”与“钙碱法”都是常见的SO2处理方案。钠碱法即利用NaOH溶液吸收SO2,一般形成Na2SO3与NaHSO3的混合液;钙碱法即利用消石灰悬浊液吸收。
(1)用150g质量分数为40.0%的NaOH溶液吸收SO2,最多可吸收
 (折算到标准状况下);此时溶液中的主要溶质是
(折算到标准状况下);此时溶液中的主要溶质是(2)如图是常温下一定量SO2通入一定浓度的NaOH溶液后含硫微粒分布系数随pH的关系图(已知:含硫微粒
 的分布系数
的分布系数 )。基于该图可得该条件下亚硫酸的一级电离常数为
)。基于该图可得该条件下亚硫酸的一级电离常数为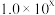 的形式表示,下同);SO
的形式表示,下同);SO 的水解平衡常数为
的水解平衡常数为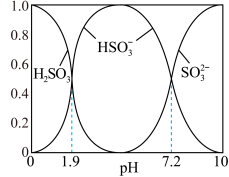
(3)若某浓度的NaOH溶液吸收了0.1molSO2,且吸收后
 ,则c(Na+)=c(
,则c(Na+)=c( )+
)+(4)用钙碱法吸收SO2后往往会生成CaSO3沉淀
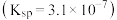 ,将足量该沉淀置于0.10mol/LNa2SO3溶液中,求c(Ca2+)(写出过程):
,将足量该沉淀置于0.10mol/LNa2SO3溶液中,求c(Ca2+)(写出过程):
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】低浓度SO2废气的处理是工业难题,目前常用的方法如下:
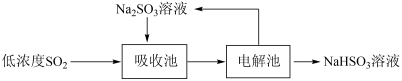
(1) 溶液吸收SO2的化学方程式是
溶液吸收SO2的化学方程式是_______ 。
(2)如果用含等物质的量溶质的下列各溶液分别吸收SO2,则理论吸收量最多的是_______ 。
a. b.
b. c.溴水 d.酸性
c.溴水 d.酸性
氧化剂与还原剂的物质的量之比为_______ 。
(3)研究大气中含硫化合物(主要是 和
和 )的转化具有重要意义。
)的转化具有重要意义。 资源化利用途径之一是回收能量并得到单质硫,如图为质子膜(该膜的作用就是只容许固体电解质中的H+自由通过)H2S燃料电池的示意图。
资源化利用途径之一是回收能量并得到单质硫,如图为质子膜(该膜的作用就是只容许固体电解质中的H+自由通过)H2S燃料电池的示意图。
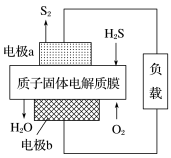
①电极b为电池的_______ 极,电极a上发生的电极反应为:_______ 。
②硫元素在元素周期表中的位置_______ ,其气态氢化物的电子式_______ 。
③每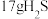 参与反应,正极消耗的
参与反应,正极消耗的 为
为_______ mol。
(4)汽车的启动电源常用铅蓄电池。放电时其电池反应为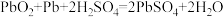 。当外电路转移1mol电子时,会消耗
。当外电路转移1mol电子时,会消耗_______ mol ,此时正极质量增加
,此时正极质量增加_______ g。

(1)
 溶液吸收SO2的化学方程式是
溶液吸收SO2的化学方程式是(2)如果用含等物质的量溶质的下列各溶液分别吸收SO2,则理论吸收量最多的是
a.
 b.
b. c.溴水 d.酸性
c.溴水 d.酸性
氧化剂与还原剂的物质的量之比为
(3)研究大气中含硫化合物(主要是
 和
和 )的转化具有重要意义。
)的转化具有重要意义。 资源化利用途径之一是回收能量并得到单质硫,如图为质子膜(该膜的作用就是只容许固体电解质中的H+自由通过)H2S燃料电池的示意图。
资源化利用途径之一是回收能量并得到单质硫,如图为质子膜(该膜的作用就是只容许固体电解质中的H+自由通过)H2S燃料电池的示意图。
①电极b为电池的
②硫元素在元素周期表中的位置
③每
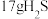 参与反应,正极消耗的
参与反应,正极消耗的 为
为(4)汽车的启动电源常用铅蓄电池。放电时其电池反应为
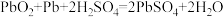 。当外电路转移1mol电子时,会消耗
。当外电路转移1mol电子时,会消耗 ,此时正极质量增加
,此时正极质量增加
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】氮及其化合物的转化关系如下图所示,

(1)①~④各步转化中,属于氮的固定的是___________ (填序号)。
(2)写出工业上制备氨气的化学方程式___________ 。
(3)工业制硝酸时尾气中含有NO、NO2,常用NaOH溶液吸收处理。
①NaOH溶液吸收尾气时发生的反应有:2NaOH+NO+NO2=NaNO2+H2O,NaOH溶液吸收NO2的离子方程式为___________ 。
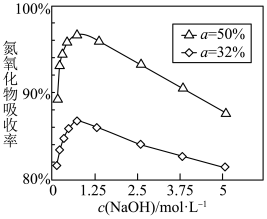
②用不同浓度的NaOH溶液吸收NO2含量不同的尾气,氮氧化物的吸收率随NaOH溶液浓度的变化如下图所示(α表示尾气里NO、NO2中NO2的含量)。当α小于50%时,加入H2O2能提高氮氧化物的吸收率,原因是___________ 。
③不用水吸收处理NO2的原因是___________ 。

(1)①~④各步转化中,属于氮的固定的是
(2)写出工业上制备氨气的化学方程式
(3)工业制硝酸时尾气中含有NO、NO2,常用NaOH溶液吸收处理。
①NaOH溶液吸收尾气时发生的反应有:2NaOH+NO+NO2=NaNO2+H2O,NaOH溶液吸收NO2的离子方程式为
②用不同浓度的NaOH溶液吸收NO2含量不同的尾气,氮氧化物的吸收率随NaOH溶液浓度的变化如下图所示(α表示尾气里NO、NO2中NO2的含量)。当α小于50%时,加入H2O2能提高氮氧化物的吸收率,原因是

③不用水吸收处理NO2的原因是
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】化学与生产、生活息息相关。请回答以下问题。
(1)小苏打可用于治疗胃酸过多,写出该反应的离子方程式_______ 。
(2)合成氨工业化,对人类影响深远。工业上合成氨的化学方程式为_______ 。
(3)沾有水的铁锅在高温火焰上灼烧会发黑,该反应的化学方程式为_______ 。
(4)用碘水、淀粉等试剂检测葡萄酒中 的含量,写出相应的离子方程式
的含量,写出相应的离子方程式_______ 。
(5)洁厕剂的主要成分为盐酸。欲配制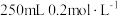 的盐酸,需要HCl的物质的量为
的盐酸,需要HCl的物质的量为_______ 。
(1)小苏打可用于治疗胃酸过多,写出该反应的离子方程式
(2)合成氨工业化,对人类影响深远。工业上合成氨的化学方程式为
(3)沾有水的铁锅在高温火焰上灼烧会发黑,该反应的化学方程式为
(4)用碘水、淀粉等试剂检测葡萄酒中
 的含量,写出相应的离子方程式
的含量,写出相应的离子方程式(5)洁厕剂的主要成分为盐酸。欲配制
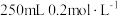 的盐酸,需要HCl的物质的量为
的盐酸,需要HCl的物质的量为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】请根据要求书写出方程式。
(1)2021年3月18日,在由全球权威电子行业媒体ASPENCORE主办的2021年中国IC领袖峰会上,苏州芯联成软件有限公司获优异表现,芯片的主要成分是_______ ,写出其工业制备粗产品的化学反应方程式_______
(2)精美的雕花玻璃使我们的世界变得绚丽多彩,雕花玻璃涉及的主要反应的化学方程式为_______ 。
(3)1754年,Briestly用硵砂(主要成份NH4Cl)和熟石灰共热制得了氨,化学反应方程式为_______ 。
(4)可利用CH4等气体除去烟气中的氮氧化物,生成物为可参与大气循环的气体,请写出CH4与NO反应的化学方程式_______ 。
(5)将H2S和空气的混合气体通入FeCl3、FeCl2、CuCl2的混合溶液中反应可以回收S,其物质转化如图所示。该图示的总反应为_______ 。

(6)将 3.2g 铜与 60.0mL 一定浓度的硝酸发生反应,铜完全溶解,产生 NO2 和 NO 混合气体的体积为 8.96L(标况)。待产生的气体全部释放后,向溶液加入 100mL 2.0mol/L 的 NaOH 溶液,恰好使溶液中的 Cu2+全部转化成沉淀,则原硝酸溶液的浓度为_______ mol/L。
(1)2021年3月18日,在由全球权威电子行业媒体ASPENCORE主办的2021年中国IC领袖峰会上,苏州芯联成软件有限公司获优异表现,芯片的主要成分是
(2)精美的雕花玻璃使我们的世界变得绚丽多彩,雕花玻璃涉及的主要反应的化学方程式为
(3)1754年,Briestly用硵砂(主要成份NH4Cl)和熟石灰共热制得了氨,化学反应方程式为
(4)可利用CH4等气体除去烟气中的氮氧化物,生成物为可参与大气循环的气体,请写出CH4与NO反应的化学方程式
(5)将H2S和空气的混合气体通入FeCl3、FeCl2、CuCl2的混合溶液中反应可以回收S,其物质转化如图所示。该图示的总反应为

(6)将 3.2g 铜与 60.0mL 一定浓度的硝酸发生反应,铜完全溶解,产生 NO2 和 NO 混合气体的体积为 8.96L(标况)。待产生的气体全部释放后,向溶液加入 100mL 2.0mol/L 的 NaOH 溶液,恰好使溶液中的 Cu2+全部转化成沉淀,则原硝酸溶液的浓度为
您最近一年使用:0次




