研究金属的腐蚀过程及防腐蚀对人们的日常生活有重大意义。
(1)如图中的铁棒若为纯铁,则其腐蚀过程属于_______ 腐蚀(选填“化学”或“电化学”)。
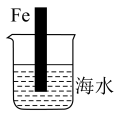
(2)若铁棒的含碳量为10.8%,浸入一段时间之后发现,越靠近烧杯底部发生电化学腐蚀就越轻微,该实验说明_______ 因素会影响铁的腐蚀速率;腐蚀时,正极的电极反应式为_______ 。(已知:海水pH约为8.1)
(1)如图中的铁棒若为纯铁,则其腐蚀过程属于

(2)若铁棒的含碳量为10.8%,浸入一段时间之后发现,越靠近烧杯底部发生电化学腐蚀就越轻微,该实验说明
更新时间:2023-09-18 10:13:53
|
相似题推荐
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】如图所示,组成一种原电池。试回答下列问题(灯泡功率合适):
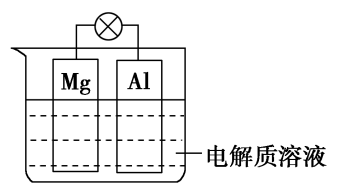
(1)电解质溶液为稀硫酸时,灯泡亮,Mg电极上发生的反应为____________ ;Al电极上发生的反应为________ 。溶液中 向
向________ 移动(填“Mg电极”或“Al电极”)
(2)电解质溶液为NaOH溶液时,灯泡________ (填“亮”或“不亮”,填“亮”做a题,填“不亮”做b题)。_______________
a.若灯泡亮,Al电极为_______________(填“正极”或“负极”)。
b.若灯泡不亮,其理由为__________________。

(1)电解质溶液为稀硫酸时,灯泡亮,Mg电极上发生的反应为
 向
向(2)电解质溶液为NaOH溶液时,灯泡
a.若灯泡亮,Al电极为_______________(填“正极”或“负极”)。
b.若灯泡不亮,其理由为__________________。
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】根据所学知识,回答下列问题:
(1)下列变化中,属于吸热反应的是_______ 。(填标号)
①氧化钙与水反应;②石灰石在高温下的分解反应;③酸碱中和反应;④二氧化碳通过炽热的炭发生的反应;⑤食物因氧化而腐败发生的反应;⑥ 与
与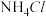 的反应;⑦干冰汽化。
的反应;⑦干冰汽化。
(2)为探究固体M溶于水的热效应,选择如图所示装置进行实验(反应在甲中进行)。观察到烧杯里产生气泡,则M溶于水_______ (填“一定”或“可能”)是放热反应。

(3)铅蓄电池是常用的化学电源,其电极材料分别是Pb和 ,电解液为硫酸。
,电解液为硫酸。
①铅蓄电池属于_______ (填“一次”或“二次”)电池,该蓄电池放电时,电解质溶液中阴离子移向_______ (填“正”或“负”)极。正极反应方程式为_______
②充电时,以氢氧燃料电池(30%KOH溶液为电解质溶液)为电源,则该氢氧燃料电池负极上的电极反应式为_______ 。
③乙醇(C2H5OH)燃料电池(Pt为电极),以KOH为电解质溶液,写出负极电极反应式_______ ,当转移电子1.2mol时,消耗氧气标况下体积为_______ 。
(1)下列变化中,属于吸热反应的是
①氧化钙与水反应;②石灰石在高温下的分解反应;③酸碱中和反应;④二氧化碳通过炽热的炭发生的反应;⑤食物因氧化而腐败发生的反应;⑥
 与
与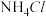 的反应;⑦干冰汽化。
的反应;⑦干冰汽化。(2)为探究固体M溶于水的热效应,选择如图所示装置进行实验(反应在甲中进行)。观察到烧杯里产生气泡,则M溶于水

(3)铅蓄电池是常用的化学电源,其电极材料分别是Pb和
 ,电解液为硫酸。
,电解液为硫酸。①铅蓄电池属于
②充电时,以氢氧燃料电池(30%KOH溶液为电解质溶液)为电源,则该氢氧燃料电池负极上的电极反应式为
③乙醇(C2H5OH)燃料电池(Pt为电极),以KOH为电解质溶液,写出负极电极反应式
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】I.在2L的恒容密闭容器中充入1mol CO和2molH2, 一定条件下发生反应:CO(g)+2H2(g)  CH3OH (g),测得CO和CH3OH(g)的物质的量变化如图1所示,反应过程中的能量变化如图2所示。
CH3OH (g),测得CO和CH3OH(g)的物质的量变化如图1所示,反应过程中的能量变化如图2所示。
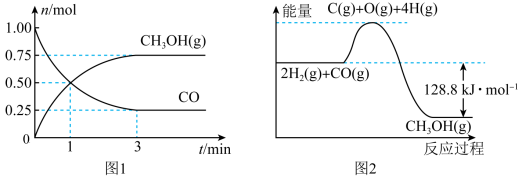
(1)从反应开始至达到平衡,以H2表示的反应的平均反应速率v(H2)=_________ 。外界条件不变时,随着反应的进行,该反应的化学反应速率逐渐减小的原因可能是_________ (填字母)。
A.温度减低 B.压强降低,
C.CO的浓度减小 D.CH3OH 的浓度增大
(2)下列描述中能说明上述反应达到平衡状态的是___________
(3)平衡时H2的转化率为___________ ,平衡时与起始时容器内的压强比为_______ ;
(4)已知断开1mol CO(g)和2mol H2(g)中的化学键需要吸收的能量为1924kJ,则断开lmol CH3OH(g)中的化学键共需要吸收___________ kJ的能量。
Ⅱ.电能是现代社会应用最广泛的能源之一
(5)关于图I所示装置的说法中,正确的是_________ 。
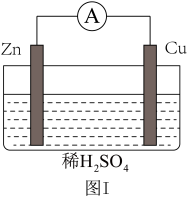
a.负极反应是Zn-2e-=Zn2+
b.电子由Zn片通过导线流向Cu片
c.一段时间后,溶液酸性增强
d.溶液中的H+向Cu片移动
(6)图I所示原电池中,当Cu表面析出4.48L氢气(标准状况)时,导线中通过的电子的物质的量为___________ mol。
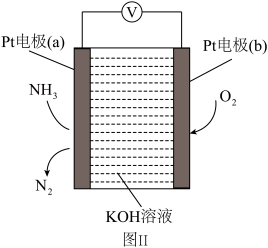
(7)图Ⅱ所示装置为电化学气级传感器,通过电压表示数可测量环境中NH3的含量。电极b是___________ 。(填“正”或“负”)极:电极a上发生的电极反应为___________ 。
 CH3OH (g),测得CO和CH3OH(g)的物质的量变化如图1所示,反应过程中的能量变化如图2所示。
CH3OH (g),测得CO和CH3OH(g)的物质的量变化如图1所示,反应过程中的能量变化如图2所示。
(1)从反应开始至达到平衡,以H2表示的反应的平均反应速率v(H2)=
A.温度减低 B.压强降低,
C.CO的浓度减小 D.CH3OH 的浓度增大
(2)下列描述中能说明上述反应达到平衡状态的是___________
| A.CO、H2和CH3OH三种物质的浓度相等 |
| B.混合气体的密度不随时间的变化而变化 |
| C.混合气体的总物质的量不随时间的变化而变化 |
| D.单位时间内消耗2mol H2的同时生成lmol CH3OH |
(4)已知断开1mol CO(g)和2mol H2(g)中的化学键需要吸收的能量为1924kJ,则断开lmol CH3OH(g)中的化学键共需要吸收
Ⅱ.电能是现代社会应用最广泛的能源之一
(5)关于图I所示装置的说法中,正确的是

a.负极反应是Zn-2e-=Zn2+
b.电子由Zn片通过导线流向Cu片
c.一段时间后,溶液酸性增强
d.溶液中的H+向Cu片移动
(6)图I所示原电池中,当Cu表面析出4.48L氢气(标准状况)时,导线中通过的电子的物质的量为
(7)图Ⅱ所示装置为电化学气级传感器,通过电压表示数可测量环境中NH3的含量。电极b是

您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】本题为《化学与生活(选修1)》选做题
请根据题意,选择恰当的选项用字母代号填空。
(1)均衡营养和正确使用药物是保证身心健康的重要方面,现有下列四种物质:
A.葡萄糖 B.氨基酸 C.麻黄碱 D.阿司匹林
①蛋白质水解的最终产物是_______ ;
②人体内最重要的供能物质是________ ;
③具有解热镇痛作用,用于治疗感冒的是_______ ;
④对支气管哮喘症有明显疗效的是_________ 。
(2)材料是人类赖以生存和发展的重要物质基础。
①试管、烧杯和烧瓶等化学仪器的主要材质是________ ;
A.玻璃 B.陶瓷
②钢铁是目前用量最大的铁合金。钢铁接触海水发生电化学腐蚀,其负极反应式为_________ ;
A.O2+2H2O + 4e- = 4OH- B.Fe - 2e -= Fe2+
因此,为防止轮船船体被腐蚀,可在船体上安装一定量的_______ 。
A.锌块 B.铜块
(3)当前,环境治理已成为重要的民生工程。
①2014年1月,教育部规定在学校公共场所禁止吸烟。下列有关说法中,不正确
的是_________ ;
A.吸烟会对室内和公共场所造成污染
B.吸入焦油、尼古丁及颗粒物可导致多种病变
C.N2、CO2、CO和尼古丁都属于室内空气污染物
②下列做法可能会加重“雾霾”的是______ ;
A.大量焚烧秸秆
B.在汽车尾气系统装置催化转化器
C.发展煤的气化和液化等洁净煤技术
③下列处理垃圾的方法中,不正确的是_____________ 。
A.回收利用废纸 B.回收利用易拉罐 C.填埋废旧电池
请根据题意,选择恰当的选项用字母代号填空。
(1)均衡营养和正确使用药物是保证身心健康的重要方面,现有下列四种物质:
A.葡萄糖 B.氨基酸 C.麻黄碱 D.阿司匹林
①蛋白质水解的最终产物是
②人体内最重要的供能物质是
③具有解热镇痛作用,用于治疗感冒的是
④对支气管哮喘症有明显疗效的是
(2)材料是人类赖以生存和发展的重要物质基础。
①试管、烧杯和烧瓶等化学仪器的主要材质是
A.玻璃 B.陶瓷
②钢铁是目前用量最大的铁合金。钢铁接触海水发生电化学腐蚀,其负极反应式为
A.O2+2H2O + 4e- = 4OH- B.Fe - 2e -= Fe2+
因此,为防止轮船船体被腐蚀,可在船体上安装一定量的
A.锌块 B.铜块
(3)当前,环境治理已成为重要的民生工程。
①2014年1月,教育部规定在学校公共场所禁止吸烟。下列有关说法中,不正确
的是
A.吸烟会对室内和公共场所造成污染
B.吸入焦油、尼古丁及颗粒物可导致多种病变
C.N2、CO2、CO和尼古丁都属于室内空气污染物
②下列做法可能会加重“雾霾”的是
A.大量焚烧秸秆
B.在汽车尾气系统装置催化转化器
C.发展煤的气化和液化等洁净煤技术
③下列处理垃圾的方法中,不正确的是
A.回收利用废纸 B.回收利用易拉罐 C.填埋废旧电池
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】恒温条件下,用图1所示装置研究铁的电化学腐蚀,测定结果如图2。 段主要发生
段主要发生___________ 腐蚀, 段负极反应式为
段负极反应式为___________ 。
 段主要发生
段主要发生 段负极反应式为
段负极反应式为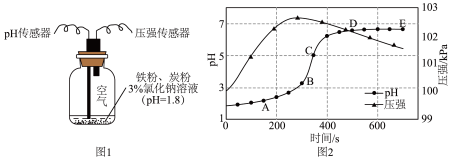
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】如何防止铁的锈蚀是工业上研究的重点内容。为研究铁的锈蚀,某同学做了探究实验,如下图所示,铁处于①②③三种不同的环境中
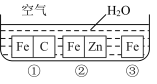
请回答:
(1)金属腐蚀主要分为__________ 腐蚀和_____________ 腐蚀两种。
(2)铁被腐蚀的速率由快到慢的顺序是_________________ (填序号)。
(3)①中正极的电极反应式为_________________________________________________ ,②中负极的电极反应式为_________________________________________ 。
(4)据资料显示,全世界每年因腐蚀而报废的金属材料相当于其年产量的20%以上。为防护金属被腐蚀可采取的措施有__________ (填序号)。
①健身器材刷油漆 ②自行车钢圈镀铬
③将钢管用导线与铜条连接 ④将钢管用导线与碳棒连接

请回答:
(1)金属腐蚀主要分为
(2)铁被腐蚀的速率由快到慢的顺序是
(3)①中正极的电极反应式为
(4)据资料显示,全世界每年因腐蚀而报废的金属材料相当于其年产量的20%以上。为防护金属被腐蚀可采取的措施有
①健身器材刷油漆 ②自行车钢圈镀铬
③将钢管用导线与铜条连接 ④将钢管用导线与碳棒连接
您最近一年使用:0次



