碳是形成化合物种类最多的元素,其单质及其部分化合物是人类生产生活的主要能源物质。请回答下列问题:
(1)有机物M经过太阳光光照可转化成N,转化过程如下:
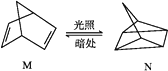
ΔH=+88.6 kJ·mol-1,则M、N相比,较稳定的是__________ 。
(2)CH3OH+O2(g) =CO2(g)+2H2O(g) ΔH=-akJ·mol-1,则a________ (填“>”“<”或“=”)238.6。(已知甲醇的燃烧热为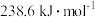 )
)
(3)使Cl2和H2O(g)通过灼热的炭层,生成HCl和CO2,当有1 mol Cl2参与反应时释放出145 kJ热量,写出该反应的热化学方程式:____________________________ 。
(4)将石墨、铝粉和二氧化钛按一定比例混合在高温下煅烧,所得物质可作耐高温材料,4Al(s)+3TiO2(s)+3C(s) ===2Al2O3(s)+3TiC(s) ΔH= -1 176 kJ·mol-1,则反应过程中,每转移1 mol电子放出的热量为_____________ 。
(1)有机物M经过太阳光光照可转化成N,转化过程如下:

ΔH=+88.6 kJ·mol-1,则M、N相比,较稳定的是
(2)CH3OH+O2(g) =CO2(g)+2H2O(g) ΔH=-akJ·mol-1,则a
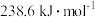 )
) (3)使Cl2和H2O(g)通过灼热的炭层,生成HCl和CO2,当有1 mol Cl2参与反应时释放出145 kJ热量,写出该反应的热化学方程式:
(4)将石墨、铝粉和二氧化钛按一定比例混合在高温下煅烧,所得物质可作耐高温材料,4Al(s)+3TiO2(s)+3C(s) ===2Al2O3(s)+3TiC(s) ΔH= -1 176 kJ·mol-1,则反应过程中,每转移1 mol电子放出的热量为
13-14高三·全国·课时练习 查看更多[14]
辽宁省普兰店市第一中学2019届高三上学期期中考试化学试题高二人教版选修4 期末学业测评(二)【全国百强校】福建省三明市第一中学2018-2019学年高二上学期第一次月考化学试题(已下线)《2018-2019学年同步单元双基双测AB卷》第一单元 化学反应与能量单元测试(A卷)河南省鹤壁市淇县第一中学2018-2019学年高二(普通班)上学期第一次月考化学试题四川省成都经济技术开发区实验中学校2019届高三上学期入学考试化学试题2018-2019学年人教版高中化学选修四 章末综合测评1 化学反应与能量2018-2019学年人教版高二化学选修四章:化学反应与能量末测试题河北省安平中学2017-2018学年高一下学期期末考试化学试题1【全国百强校】广东仲元中学2017-2018学年高二下学期期中考试(理)化学试题(已下线)二轮复习 专题8 化学反应中与能量变化 押题专练重庆市九校联盟2017-2018学年高二上学期期中考试化学试题山西省实验中学2017-2018学年高二上学期10月月考化学试题(已下线)2014年高考化学一轮复习课后规范训练6-1练习卷
更新时间:2016-12-08 21:45:51
|
相似题推荐
填空题
|
适中
(0.65)
【推荐1】化学反应一定伴随能量变化。
(1)将20gBa(OH)2·8H2O晶体与10g NH4Cl晶体一起放入烧杯中,并将烧杯放在滴有几滴水的玻璃片上,用玻璃棒快速搅拌,闻到______ 气味,用手触摸烧杯底部感觉________ ,烧杯下面的玻璃片可能与烧杯___ 。 说明Ba(OH)2·8H2O跟NH4Cl的反应是_____ (填“吸热”或“放热”)反应。该反应的化学方程式_________
(2)NaOH稀溶液跟稀盐酸反应的中和热与KOH稀溶液跟稀硫酸反应的中和热_____ (填 “相等”或“不等”),原因是(用适当的文字和离子方程式解释)_____
(3)下列措施可以提高燃料的燃烧效率的是________ (填序号)
①提高燃料的着火点,②降低燃料的着火点,③将固体燃料粉碎,④将液体燃料雾化,⑤将燃料煤气化处理,⑥通入适量空气
(1)将20gBa(OH)2·8H2O晶体与10g NH4Cl晶体一起放入烧杯中,并将烧杯放在滴有几滴水的玻璃片上,用玻璃棒快速搅拌,闻到
(2)NaOH稀溶液跟稀盐酸反应的中和热与KOH稀溶液跟稀硫酸反应的中和热
(3)下列措施可以提高燃料的燃烧效率的是
①提高燃料的着火点,②降低燃料的着火点,③将固体燃料粉碎,④将液体燃料雾化,⑤将燃料煤气化处理,⑥通入适量空气
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】反应A(g)+B(g) C(g)+D(g)过程中的能量变化如图所示,回答下列问题。
C(g)+D(g)过程中的能量变化如图所示,回答下列问题。
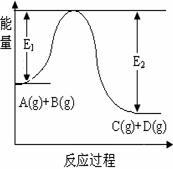
(1)该反应是__________ 反应(填“吸热”“放热”);
(2)当反应达到平衡时,升高温度,A的转化率________ (填“增大”“减小”“不变”)。
(3)在反应体系中加入催化剂,反应速率增大,E1和E2的变化是:E1_______ ,E2_______ (填“增大”“减小”“不变”)。
(4)已知下列热化学方程式:
①H2(g)+1/2O2(g)=H2O(l);ΔH=-285 kJ·mol-1
②H2(g)+1/2O2(g)=H2O(g);ΔH=-241.8 kJ·mol-1
③C(s)+1/2O2(g)=CO(g);ΔH=-110.5 kJ·mol-1
④ C(s)+O2(g)=CO2(g);ΔH=-393.5 kJ·mol-1
回答下列问题:
① 燃烧1gH2生成液态水,放出的热量为__________________ 。
②写出CO燃烧热的热化学方程式___________________________________________ 。
 C(g)+D(g)过程中的能量变化如图所示,回答下列问题。
C(g)+D(g)过程中的能量变化如图所示,回答下列问题。
(1)该反应是
(2)当反应达到平衡时,升高温度,A的转化率
(3)在反应体系中加入催化剂,反应速率增大,E1和E2的变化是:E1
(4)已知下列热化学方程式:
①H2(g)+1/2O2(g)=H2O(l);ΔH=-285 kJ·mol-1
②H2(g)+1/2O2(g)=H2O(g);ΔH=-241.8 kJ·mol-1
③C(s)+1/2O2(g)=CO(g);ΔH=-110.5 kJ·mol-1
④ C(s)+O2(g)=CO2(g);ΔH=-393.5 kJ·mol-1
回答下列问题:
① 燃烧1gH2生成液态水,放出的热量为
②写出CO燃烧热的热化学方程式
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】(1)为了探究化学能与热能的转化,某实验小组设计了如下三套实验装置:
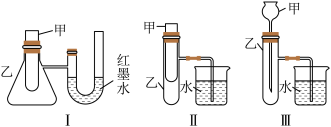
①上述装置中,不能用来证明“锌和稀硫酸反应是吸热反应还是放热反应”的是___________ (填序号)。
②某同学选用装置Ⅰ进行实验(实验前U形管里液面左右相平),在甲试管里加入适量氢氧化钡晶体与氯化铵固体搅拌反应,U形管中可观察到的现象是_________ 。
③除了图示某些装置,还有其它方法能证明超氧化钾粉末与水的反应(4KO2+2H2O=4KOH+3O2↑)是放热反应还是吸热反应:取适量超氧化钾粉末用脱脂棉包裹并放在石棉网上,向脱脂棉上滴加几滴蒸馏水,片刻后,若观察到棉花燃烧,则说明该反应是________ 反应(填“放热”或“吸热”)。
(2)化学反应的焓变通常用实验进行测定,也可进行理论推算。
①实验测得,标准状况下11.2L甲烷在氧气中充分燃烧生成液态水和二氧化碳气体时释放出akJ的热量,试写出表示甲烷燃烧热的热化学方程式:_______ ;
②已知反应CH3—CH3(g)→CH2=CH2(g)+H2(g) ΔH,有关化学键的键能如下:
通过计算得出该反应的焓变ΔH=_________ ;
(3)研究NO2、SO2、CO等大气污染气体的处理有重要意义。
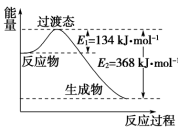
如图为1molNO2(g)和1molCO(g)反应生成NO(g)和CO2(g)过程中的能量变化示意图。已知E1=134kJ·mol-1,E2=368kJ·mol-1(E1、E2为反应的活化能)。
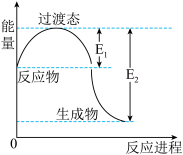
若在反应体系中加入催化剂,反应速率增大,则E1、ΔH的变化分别是________ 、________ (填“增大”、“减小”或“不变”);该反应放出的热量为__________ kJ。

①上述装置中,不能用来证明“锌和稀硫酸反应是吸热反应还是放热反应”的是
②某同学选用装置Ⅰ进行实验(实验前U形管里液面左右相平),在甲试管里加入适量氢氧化钡晶体与氯化铵固体搅拌反应,U形管中可观察到的现象是
③除了图示某些装置,还有其它方法能证明超氧化钾粉末与水的反应(4KO2+2H2O=4KOH+3O2↑)是放热反应还是吸热反应:取适量超氧化钾粉末用脱脂棉包裹并放在石棉网上,向脱脂棉上滴加几滴蒸馏水,片刻后,若观察到棉花燃烧,则说明该反应是
(2)化学反应的焓变通常用实验进行测定,也可进行理论推算。
①实验测得,标准状况下11.2L甲烷在氧气中充分燃烧生成液态水和二氧化碳气体时释放出akJ的热量,试写出表示甲烷燃烧热的热化学方程式:
②已知反应CH3—CH3(g)→CH2=CH2(g)+H2(g) ΔH,有关化学键的键能如下:
| 化学键 | C—H | C=C | C—C | H—H |
| 键能/kJ·mol-1 | 414.4 | 615.3 | 347.3 | 435.3 |
通过计算得出该反应的焓变ΔH=
(3)研究NO2、SO2、CO等大气污染气体的处理有重要意义。
如图为1molNO2(g)和1molCO(g)反应生成NO(g)和CO2(g)过程中的能量变化示意图。已知E1=134kJ·mol-1,E2=368kJ·mol-1(E1、E2为反应的活化能)。

若在反应体系中加入催化剂,反应速率增大,则E1、ΔH的变化分别是
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】碳是化合物种类最多的元素,其单质及化合物是人类生产生活的主要能源物质。请回答下列问题:
(1)有机物M经过太阳光照可转化成N,转化过程如下,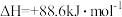 。则M、N相比,较稳定的是
。则M、N相比,较稳定的是_______
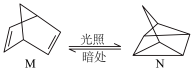
(2)已知 (l)的燃烧热为238.6kJ/mol,
(l)的燃烧热为238.6kJ/mol,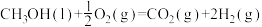
 ,则a
,则a_______ 238.6(填“ ”、“
”、“ ”或“
”或“ ”)。
”)。
(3)使 和
和 (g)通过灼热的炭层,生成HCl(g)和
(g)通过灼热的炭层,生成HCl(g)和 ,当有1mol
,当有1mol 参与反应时释放出145kJ热量,写出该反应的热化学方程式
参与反应时释放出145kJ热量,写出该反应的热化学方程式_______ 。
(4)火箭和导弹表面的薄层是耐高温物质。下列反应可制得耐高温材料,热化学方程式为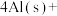
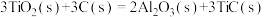
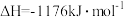 。反应过程中每转移1mol
。反应过程中每转移1mol 放出的热量为
放出的热量为_______ kJ。
(5)已知1mol燃料完全燃烧的数据分别为:
使用上述燃料最能体现“低碳经济”理念的是_______ 。
(6)乙基叔丁基醚(以ETBE表示)是一种性能优良的高辛烷值汽油调和剂。用乙醇与异丁烯(以IB表示)在催化剂HZSM—5催化下合成ETBE,反应的热化学方程式为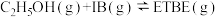
 。反应物被催化剂HZSM—5吸附的顺序与反应历程的关系如图所示,该反应的
。反应物被催化剂HZSM—5吸附的顺序与反应历程的关系如图所示,该反应的
_______ a ;反应历程的最优途径是
;反应历程的最优途径是
_______ (填“ ”、“
”、“ ”或“
”或“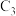 ”)。
”)。
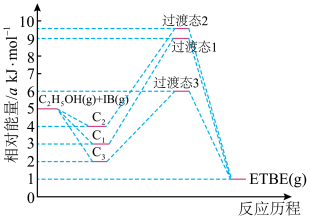
 表示先吸附乙醇,
表示先吸附乙醇, 表示先吸附异丁烯,
表示先吸附异丁烯,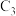 表示乙醇和异丁烯同时吸附
表示乙醇和异丁烯同时吸附
(1)有机物M经过太阳光照可转化成N,转化过程如下,
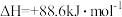 。则M、N相比,较稳定的是
。则M、N相比,较稳定的是
(2)已知
 (l)的燃烧热为238.6kJ/mol,
(l)的燃烧热为238.6kJ/mol,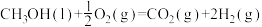
 ,则a
,则a ”、“
”、“ ”或“
”或“ ”)。
”)。(3)使
 和
和 (g)通过灼热的炭层,生成HCl(g)和
(g)通过灼热的炭层,生成HCl(g)和 ,当有1mol
,当有1mol 参与反应时释放出145kJ热量,写出该反应的热化学方程式
参与反应时释放出145kJ热量,写出该反应的热化学方程式(4)火箭和导弹表面的薄层是耐高温物质。下列反应可制得耐高温材料,热化学方程式为
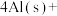
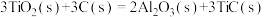
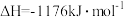 。反应过程中每转移1mol
。反应过程中每转移1mol 放出的热量为
放出的热量为(5)已知1mol燃料完全燃烧的数据分别为:
| 燃料 | 一氧化碳 | 甲烷 | 异辛烷(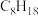 ) ) | 乙醇 |
 | 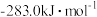 | 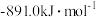 | 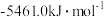 | 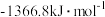 |
(6)乙基叔丁基醚(以ETBE表示)是一种性能优良的高辛烷值汽油调和剂。用乙醇与异丁烯(以IB表示)在催化剂HZSM—5催化下合成ETBE,反应的热化学方程式为
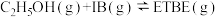
 。反应物被催化剂HZSM—5吸附的顺序与反应历程的关系如图所示,该反应的
。反应物被催化剂HZSM—5吸附的顺序与反应历程的关系如图所示,该反应的
 ;反应历程的最优途径是
;反应历程的最优途径是
 ”、“
”、“ ”或“
”或“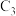 ”)。
”)。
 表示先吸附乙醇,
表示先吸附乙醇, 表示先吸附异丁烯,
表示先吸附异丁烯, 表示乙醇和异丁烯同时吸附
表示乙醇和异丁烯同时吸附
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】对于可逆反应 2 A( ?) + B(g)  2C( g) ;下图
2C( g) ;下图
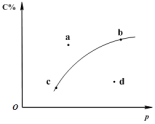
是其它条件一定时反应中 C 的百分含量与压强的关系曲线。回答下列问题:
(1) 物质 A 的状态是_____________________ (填“气体”、“液体”或“固体”) ;
(2) 图中 a、b、c、d 四点中表示 Q > K的点是_________ ;
(3) 在 a、b、c 三种条件下达平衡时,v ( a)、v ( b)、v ( c)按由大到小排序___________
(4) 如图是该反应正向过程的能量变化示意图。其逆反应的活化能以及热化学方程式为________ kJ/mol,____________
(5) 对于2SO2(g) + O2(g) 2SO3(g) Δ H = -198 kJ /mo l。在实际生产过程中,原料气中SO2 为 7%( 体积分数) 、O2 为 11% ,在常压下、温度 4 50 ℃ 左右进行,原料气中 SO2 与 O2 的体积比不是 2 ∶1 的原因是
2SO3(g) Δ H = -198 kJ /mo l。在实际生产过程中,原料气中SO2 为 7%( 体积分数) 、O2 为 11% ,在常压下、温度 4 50 ℃ 左右进行,原料气中 SO2 与 O2 的体积比不是 2 ∶1 的原因是___________________ 。
 2C( g) ;下图
2C( g) ;下图
是其它条件一定时反应中 C 的百分含量与压强的关系曲线。回答下列问题:
(1) 物质 A 的状态是
(2) 图中 a、b、c、d 四点中表示 Q > K的点是
(3) 在 a、b、c 三种条件下达平衡时,v ( a)、v ( b)、v ( c)按由大到小排序
(4) 如图是该反应正向过程的能量变化示意图。其逆反应的活化能以及热化学方程式为

(5) 对于2SO2(g) + O2(g)
 2SO3(g) Δ H = -198 kJ /mo l。在实际生产过程中,原料气中SO2 为 7%( 体积分数) 、O2 为 11% ,在常压下、温度 4 50 ℃ 左右进行,原料气中 SO2 与 O2 的体积比不是 2 ∶1 的原因是
2SO3(g) Δ H = -198 kJ /mo l。在实际生产过程中,原料气中SO2 为 7%( 体积分数) 、O2 为 11% ,在常压下、温度 4 50 ℃ 左右进行,原料气中 SO2 与 O2 的体积比不是 2 ∶1 的原因是
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】NH3、N2H4在工业生产和国防建设中都有广泛应用。回答下列问题:
(1)纳米钴的催化作用下,N2H4可分解生成两种气体,其中一种能使湿润的红色石蕊试纸变蓝,一种能参与大气循环。当反应在不同温度下达到平衡时,混合气体中各组分的体积分数如图所示。
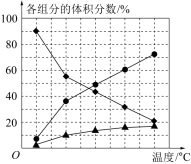
该反应的△H_______ (填“>”或“<”)0,N2H4发生分解反应的化学方程式为_______ 。
(2)T℃时,向一体积为2L的恒容密闭容器中充入总物质的量为4mol的CO2和NH3,在一定条件下发生反应:2NH3(g)+CO2(g)=CO(NH2)2(s)+H2O(g)。混合气体中氨气的体积分数随反应时间的变化如图所示。
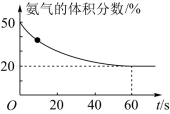
①0~60s内,反应速率v(CO2)=_______ mol∙L-1·s-1
②T℃时,该反应的化学平衡常数K=_______ 。
(1)纳米钴的催化作用下,N2H4可分解生成两种气体,其中一种能使湿润的红色石蕊试纸变蓝,一种能参与大气循环。当反应在不同温度下达到平衡时,混合气体中各组分的体积分数如图所示。

该反应的△H
(2)T℃时,向一体积为2L的恒容密闭容器中充入总物质的量为4mol的CO2和NH3,在一定条件下发生反应:2NH3(g)+CO2(g)=CO(NH2)2(s)+H2O(g)。混合气体中氨气的体积分数随反应时间的变化如图所示。

①0~60s内,反应速率v(CO2)=
②T℃时,该反应的化学平衡常数K=
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】完成下列热化学方程式:
(1)理论上稀的强酸溶液和稀的强碱溶液反应生成1mol水时放出的热量为57.3kJ,写出表示稀硫酸和稀NaOH溶液反应的热化学方程式____________ 。
(2)已知拆开1molH—H键,1molN—H键,1molN≡N键分别需要的能量是436kJ、391kJ、946kJ,则N2与H2反应生成NH3的热化学方程式______ 。
(3)25℃时,1gCH4气体完全燃烧生成二氧化碳和液态水,放出55.6kJ的热量,该反应的热化学方程为___________ 。
(4)已知:P4(白磷,s)+5O2(g)=P4O10(s)ΔH=-2983.2kJ·mol-1
P(红磷,s)+ O2(g)=
O2(g)= P4O10(s)△H=-738.5kJ·mol-1
P4O10(s)△H=-738.5kJ·mol-1
则白磷转化为红磷的热化学方程式为___________ 。
(1)理论上稀的强酸溶液和稀的强碱溶液反应生成1mol水时放出的热量为57.3kJ,写出表示稀硫酸和稀NaOH溶液反应的热化学方程式
(2)已知拆开1molH—H键,1molN—H键,1molN≡N键分别需要的能量是436kJ、391kJ、946kJ,则N2与H2反应生成NH3的热化学方程式
(3)25℃时,1gCH4气体完全燃烧生成二氧化碳和液态水,放出55.6kJ的热量,该反应的热化学方程为
(4)已知:P4(白磷,s)+5O2(g)=P4O10(s)ΔH=-2983.2kJ·mol-1
P(红磷,s)+
 O2(g)=
O2(g)= P4O10(s)△H=-738.5kJ·mol-1
P4O10(s)△H=-738.5kJ·mol-1则白磷转化为红磷的热化学方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】(1)已知:Al2O3(s)+3C(s)=2Al(s)+3CO(g) ΔH1=+1 344.1 kJ·mol-1,2AlCl3(g)=2Al(s)+3Cl2(g) ΔH2=+1 169.2 kJ·mol-1,由Al2O3、C和Cl2反应生成AlCl3的热化学方程式为______________ 。
(2)贮氢合金ThNi5可催化由CO、H2合成CH4的反应。已知温度为T时:CH4(g)+2H2O(g)=CO2(g)+4H2(g) ΔH=+165 kJ·mol-1,CO(g)+H2O(g)=CO2(g)+H2(g) ΔH=-41 kJ·mol-1,温度为T时,该反应的热化学方程式为__________ 。
(3)FeSO4可转化为FeCO3,FeCO3在空气中加热反应可制得铁系氧化物材料。已知25 ℃,101 kPa时:4Fe(s)+3O2(g)=2Fe2O3(s) ΔH=-1 648 kJ·mol-1,C(s)+O2(g)=CO2(g) ΔH=-393 kJ·mol-1 2Fe(s)+2C(s)+3O2(g)=2FeCO3(s) ΔH=-1 480 kJ·mol-1,FeCO3在空气中加热反应生成Fe2O3的热化学方程式是______ 。
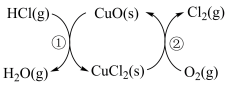
(4)用O2将HCl转化为Cl2,可提高效益,减少污染。 传统上该转化通过如图所示的催化循环实现,其中,反应①为:2HCl(g)+CuO(s) H2O(g)+CuCl2(s) ΔH1,反应②生成1 mol Cl2(g)的反应热为ΔH2,则总反应的热化学方程式为
H2O(g)+CuCl2(s) ΔH1,反应②生成1 mol Cl2(g)的反应热为ΔH2,则总反应的热化学方程式为________ (反应热用ΔH1和ΔH2表示)。
(2)贮氢合金ThNi5可催化由CO、H2合成CH4的反应。已知温度为T时:CH4(g)+2H2O(g)=CO2(g)+4H2(g) ΔH=+165 kJ·mol-1,CO(g)+H2O(g)=CO2(g)+H2(g) ΔH=-41 kJ·mol-1,温度为T时,该反应的热化学方程式为
(3)FeSO4可转化为FeCO3,FeCO3在空气中加热反应可制得铁系氧化物材料。已知25 ℃,101 kPa时:4Fe(s)+3O2(g)=2Fe2O3(s) ΔH=-1 648 kJ·mol-1,C(s)+O2(g)=CO2(g) ΔH=-393 kJ·mol-1 2Fe(s)+2C(s)+3O2(g)=2FeCO3(s) ΔH=-1 480 kJ·mol-1,FeCO3在空气中加热反应生成Fe2O3的热化学方程式是
(4)用O2将HCl转化为Cl2,可提高效益,减少污染。 传统上该转化通过如图所示的催化循环实现,其中,反应①为:2HCl(g)+CuO(s)
 H2O(g)+CuCl2(s) ΔH1,反应②生成1 mol Cl2(g)的反应热为ΔH2,则总反应的热化学方程式为
H2O(g)+CuCl2(s) ΔH1,反应②生成1 mol Cl2(g)的反应热为ΔH2,则总反应的热化学方程式为
您最近一年使用:0次




