细菌可以促使铁、氮两种元素进行氧化还原反应,并耦合两种元素的循环。耦合循环中的部分转化如图所示。
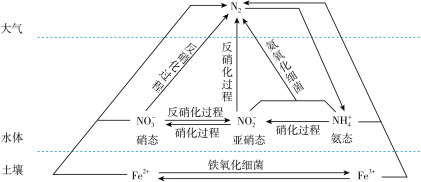
(1)如图所示氮循环中,属于氮的固定的有_______ (填字母序号)。
a. N2转化为氨态氮 b. 硝化过程 c. 反硝化过程
(2)氮肥是水体中氨态氮的主要来源之一,氨气是生产氮肥的主要原料,工业合成氨的化学方程式为_______ 。
(3)硝化过程中,含氮物质发生_______ (填“氧化”或“还原”)反应。
(4)土壤中的铁循环可用于水体脱氮:脱氮是指将氮元素从水体中除去,用离子方程式说明利用土壤中的铁循环脱除水体中氨态氮的原理:_______ ,
(5)NO是大气污染气体,测定某气体样品中NO含量操作如下:将v L气样通入适量酸化的H2O2溶液中,使NO完全被氧化为 。向上述反应后溶液中加入v1 mL c1 mol·L−1FeSO4溶液(过量),充分反应后,多余Fe2+与v2mL、c2 mol·L−1 K2Cr2O7恰好反应。 NO被H2O2氧化为
。向上述反应后溶液中加入v1 mL c1 mol·L−1FeSO4溶液(过量),充分反应后,多余Fe2+与v2mL、c2 mol·L−1 K2Cr2O7恰好反应。 NO被H2O2氧化为 的离子方程式是
的离子方程式是_______ 。上述过程中发生下列反应:3Fe2++ +4H+=NO↑+3Fe3++2H2O;
+4H+=NO↑+3Fe3++2H2O;  + 6Fe2+ +14H+ =2Cr3+ +6Fe3++7H2O,则气样中NO的含量为
+ 6Fe2+ +14H+ =2Cr3+ +6Fe3++7H2O,则气样中NO的含量为_______ g /L。

(1)如图所示氮循环中,属于氮的固定的有
a. N2转化为氨态氮 b. 硝化过程 c. 反硝化过程
(2)氮肥是水体中氨态氮的主要来源之一,氨气是生产氮肥的主要原料,工业合成氨的化学方程式为
(3)硝化过程中,含氮物质发生
(4)土壤中的铁循环可用于水体脱氮:脱氮是指将氮元素从水体中除去,用离子方程式说明利用土壤中的铁循环脱除水体中氨态氮的原理:
(5)NO是大气污染气体,测定某气体样品中NO含量操作如下:将v L气样通入适量酸化的H2O2溶液中,使NO完全被氧化为
 。向上述反应后溶液中加入v1 mL c1 mol·L−1FeSO4溶液(过量),充分反应后,多余Fe2+与v2mL、c2 mol·L−1 K2Cr2O7恰好反应。 NO被H2O2氧化为
。向上述反应后溶液中加入v1 mL c1 mol·L−1FeSO4溶液(过量),充分反应后,多余Fe2+与v2mL、c2 mol·L−1 K2Cr2O7恰好反应。 NO被H2O2氧化为 的离子方程式是
的离子方程式是 +4H+=NO↑+3Fe3++2H2O;
+4H+=NO↑+3Fe3++2H2O;  + 6Fe2+ +14H+ =2Cr3+ +6Fe3++7H2O,则气样中NO的含量为
+ 6Fe2+ +14H+ =2Cr3+ +6Fe3++7H2O,则气样中NO的含量为
更新时间:2023-10-07 10:32:42
|
相似题推荐
填空题
|
适中
(0.65)
解题方法
【推荐1】氮化铝(AlN)在电子、陶瓷工业应用广泛。工业上常通过如下反应合成: ,下列有关该反应的说法中,正确的是
,下列有关该反应的说法中,正确的是__________ 。
A.Al2O3是氧化剂
B.每生成1molAlN时至少消耗36g单质碳
C.C被还原,发生氧化反应
D.当有0.6mol电子转移时,生成0.3molCO
E.在氮化铝的合成反应中,N2还原剂,C是氧化剂
F.氮化铝中氮元素的化合价为+3
G.上述反应中每生成2molAlN,N2得到的3mol电子
H.氮化铝晶体属于原子晶体
 ,下列有关该反应的说法中,正确的是
,下列有关该反应的说法中,正确的是A.Al2O3是氧化剂
B.每生成1molAlN时至少消耗36g单质碳
C.C被还原,发生氧化反应
D.当有0.6mol电子转移时,生成0.3molCO
E.在氮化铝的合成反应中,N2还原剂,C是氧化剂
F.氮化铝中氮元素的化合价为+3
G.上述反应中每生成2molAlN,N2得到的3mol电子
H.氮化铝晶体属于原子晶体
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】中央电视台播放的《我在故宫修文物》展示了专家精湛的技艺和对传统文化的热爱与坚守,也令人体会到化学方法在文物保护中的巨大作用。某博物馆修复出土铁器的过程如下:
(1)检测锈蚀产物
铁器在具有 、
、___________ 等环境中容易被腐蚀;FeOCl中铁元素的化合价为___________ 。
(2)分析腐蚀原理:一般认为,铁经过了如下腐蚀循环。
Ⅰ.Fe转化为 。
。
Ⅱ.FeO(OH)和 反应形成致密的
反应形成致密的 保护层,
保护层, 的作用是
的作用是___________ (填字母)。
a.氧化剂 b.还原剂 c.既不是氧化剂也不是还原剂
(3)研究发现, 对铁的腐蚀会造成严重影响。化学修复方法为:脱氯、还原,形成
对铁的腐蚀会造成严重影响。化学修复方法为:脱氯、还原,形成 保护层。修复过程为:将铁器浸没在盛有0.5
保护层。修复过程为:将铁器浸没在盛有0.5
 、0.5
、0.5 NaOH混合液的容器中,缓慢加热至60~90℃。一段时间后,取出器物,用NaOH溶液洗涤至无
NaOH混合液的容器中,缓慢加热至60~90℃。一段时间后,取出器物,用NaOH溶液洗涤至无 。
。
①检测洗涤液中无 的方法是
的方法是___________ 。
②配平 还原FeO(OH)形成
还原FeO(OH)形成 的化学方程式并用双线桥法标出电子转移的方向和数目:
的化学方程式并用双线桥法标出电子转移的方向和数目:_____ 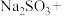 ___________
___________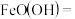 ___________
___________ ___________
___________ ___________
___________ ;生成1mol
;生成1mol  时转移
时转移___________ 个电子。
(1)检测锈蚀产物
| 主要成分的化学式 | |||
 | 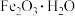 | FeO(OH) | FeOCl |
 、
、(2)分析腐蚀原理:一般认为,铁经过了如下腐蚀循环。
Ⅰ.Fe转化为
 。
。Ⅱ.FeO(OH)和
 反应形成致密的
反应形成致密的 保护层,
保护层, 的作用是
的作用是a.氧化剂 b.还原剂 c.既不是氧化剂也不是还原剂
(3)研究发现,
 对铁的腐蚀会造成严重影响。化学修复方法为:脱氯、还原,形成
对铁的腐蚀会造成严重影响。化学修复方法为:脱氯、还原,形成 保护层。修复过程为:将铁器浸没在盛有0.5
保护层。修复过程为:将铁器浸没在盛有0.5
 、0.5
、0.5 NaOH混合液的容器中,缓慢加热至60~90℃。一段时间后,取出器物,用NaOH溶液洗涤至无
NaOH混合液的容器中,缓慢加热至60~90℃。一段时间后,取出器物,用NaOH溶液洗涤至无 。
。①检测洗涤液中无
 的方法是
的方法是②配平
 还原FeO(OH)形成
还原FeO(OH)形成 的化学方程式并用双线桥法标出电子转移的方向和数目:
的化学方程式并用双线桥法标出电子转移的方向和数目: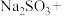 ___________
___________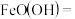 ___________
___________ ___________
___________ ___________
___________ ;生成1mol
;生成1mol  时转移
时转移
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】钠的化合物广泛应用于工业生产。
(1)氢化钠(NaH)中氢元素的化合价为___________ 。
(2)NaH能与水剧烈反应,反应方程式为 ,该反应中的氧化剂是
,该反应中的氧化剂是___________ ,NaH与液氨也有类似的反应,写出反应的化学方程式___________ 。
(3)在高温下氢化钠(NaH)可将四氯化钛( )还原成金属钛,写出该反应的化学方程式
)还原成金属钛,写出该反应的化学方程式___________ 。
(4)硼氢化钠( )与
)与 反应生成
反应生成 和
和 (已知反应过程中B的化合价不变)。写出该反应的化学方程式
(已知反应过程中B的化合价不变)。写出该反应的化学方程式___________ 。
(5)已知 在空气中完全燃烧,将燃烧产物全部通过足量的
在空气中完全燃烧,将燃烧产物全部通过足量的 ,则
,则 增加的质量是
增加的质量是___________ g。
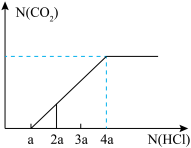
(6)现有由两种含钠化合物组成的混合物,溶于水后,逐滴加入某浓度盐酸,所得 的粒子数目与所耗HCl的粒子数目关系如图,两种含钠化合物的化学式和粒子数目之比为
的粒子数目与所耗HCl的粒子数目关系如图,两种含钠化合物的化学式和粒子数目之比为___________ 。
(1)氢化钠(NaH)中氢元素的化合价为
(2)NaH能与水剧烈反应,反应方程式为
 ,该反应中的氧化剂是
,该反应中的氧化剂是(3)在高温下氢化钠(NaH)可将四氯化钛(
 )还原成金属钛,写出该反应的化学方程式
)还原成金属钛,写出该反应的化学方程式(4)硼氢化钠(
 )与
)与 反应生成
反应生成 和
和 (已知反应过程中B的化合价不变)。写出该反应的化学方程式
(已知反应过程中B的化合价不变)。写出该反应的化学方程式(5)已知
 在空气中完全燃烧,将燃烧产物全部通过足量的
在空气中完全燃烧,将燃烧产物全部通过足量的 ,则
,则 增加的质量是
增加的质量是(6)现有由两种含钠化合物组成的混合物,溶于水后,逐滴加入某浓度盐酸,所得
 的粒子数目与所耗HCl的粒子数目关系如图,两种含钠化合物的化学式和粒子数目之比为
的粒子数目与所耗HCl的粒子数目关系如图,两种含钠化合物的化学式和粒子数目之比为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】氮元素在地球上含量丰富,是构成生命体的基本元素之一、回答下列问题:
(1)N元素在元素周期表中的位置为_______ 。
(2)制备下列物质属于固氮的是 _______。
(3)受到阳光照射浓硝酸会变黄的原因是 _______ ( 用化学方程式表示)。
(4)近几年来关于氮污染的治理倍受关注,根据氮的性质回答以下问题;
①氮的氧化物是空气的主要污染物,下列环境问题与氮的氧化物排放有关的是_______ 。
A.酸雨 B.光化学烟雾
C.白色污染 D.水土流失
②向酸性工业废水中加入次氯酸钠溶液,可将其中的NH 完全转化为N2,而次氯酸钠被还原为NaCl。写出上述反应的离子方程式:
完全转化为N2,而次氯酸钠被还原为NaCl。写出上述反应的离子方程式: _______ 。
(5)潜艇中使用的液氨-液氧燃料电池工作原理如图所示:

①电极a名称是_______ 。
②电解质溶液中OH- 离子向_______ 移动 (填“电极a”或“电极b”)。
③电极b的电极反应式为_______ 。
(1)N元素在元素周期表中的位置为
(2)制备下列物质属于固氮的是 _______。
| A.用氮气和氢气合成氨 |
| B.分离液态空气获得氮气 |
| C.用NH4Cl和熟石灰制备氨气 |
| D.NO2溶于水得到HNO3 |
(4)近几年来关于氮污染的治理倍受关注,根据氮的性质回答以下问题;
①氮的氧化物是空气的主要污染物,下列环境问题与氮的氧化物排放有关的是
A.酸雨 B.光化学烟雾
C.白色污染 D.水土流失
②向酸性工业废水中加入次氯酸钠溶液,可将其中的NH
 完全转化为N2,而次氯酸钠被还原为NaCl。写出上述反应的离子方程式:
完全转化为N2,而次氯酸钠被还原为NaCl。写出上述反应的离子方程式: (5)潜艇中使用的液氨-液氧燃料电池工作原理如图所示:

①电极a名称是
②电解质溶液中OH- 离子向
③电极b的电极反应式为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】已知氮元素是地球大气中含量最多的元素,请完成下列有关问题:
(1)写出N2的电子式:__ 。
(2)将空气中的氮气转化为氮的化合物的过程称为固氮,则下列属于固氮过程的是__ (填字母)。
A.NH3经过催化氧化生成NO
B.NH3和HNO3反应生成NH4NO3
C.N2和H2在一定条件下反应生成NH3
D.雷雨闪电时空气中的N2和O2化合生成NO
(3)如图是实验室制取氨气的装置和选用试剂,其中错误的是__ (填字母)。
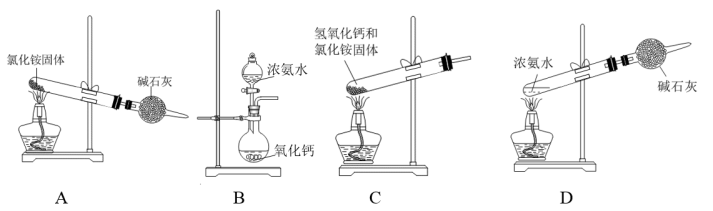
选取了正确的制备装置后,若想收集一试管氨气,可用___ 排空气法。
(4)NH4HCO3是常用的铵态氮肥,在施用时若受热会释放出氨气而降低肥效。检验其中 的方法是将固体溶于水配制浓溶液,加入浓
的方法是将固体溶于水配制浓溶液,加入浓__ 溶液、加热,再用__ 试纸检验产生的气体,若试纸变蓝则表明含有 。
。
(1)写出N2的电子式:
(2)将空气中的氮气转化为氮的化合物的过程称为固氮,则下列属于固氮过程的是
A.NH3经过催化氧化生成NO
B.NH3和HNO3反应生成NH4NO3
C.N2和H2在一定条件下反应生成NH3
D.雷雨闪电时空气中的N2和O2化合生成NO
(3)如图是实验室制取氨气的装置和选用试剂,其中错误的是

选取了正确的制备装置后,若想收集一试管氨气,可用
(4)NH4HCO3是常用的铵态氮肥,在施用时若受热会释放出氨气而降低肥效。检验其中
 的方法是将固体溶于水配制浓溶液,加入浓
的方法是将固体溶于水配制浓溶液,加入浓 。
。
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】氮元素在海洋中的循环,是整个海洋生态系统的基础和关键。海洋中无机氮的循环过程可用下图表示。
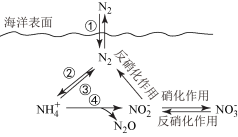
①下列关于海洋氮循环的说法正确的是___________
a.海洋中的反硝化作用一定有氧气的参与
b.海洋中的氮循环起始于氮的氧化
c.向海洋排放含NO 的废水会影响海洋中NH
的废水会影响海洋中NH 的含量
的含量
d.海洋中存在游离态的氮
②有氧时,在硝化细菌作用下,NH 可实现过程④的转化,将过程④的离子方程式补充完整(需配平):
可实现过程④的转化,将过程④的离子方程式补充完整(需配平):________ _______NH + 5O2= 2NO
+ 5O2= 2NO + _______H+ +________+________
+ _______H+ +________+________
③有人研究了温度对海洋硝化细菌去除氨氮效果的影响,下表为对10 L人工海水样本的监测数据:
硝化细菌去除氨氮的最佳反应温度是___________ ,在最佳反应温度时,48 h内去除氨氮反应的平均速率是___________ mg/(L·h)。
④海洋中的氮循环起始于氮的固定,氮的固定是几百年来科学家一直研究的课题。下表列举了不同温度下大气固氮和工业固氮的部分K值。
分析数据可知:大气固氮反应属于___________ (填“吸热”或“放热”)反应。从平衡视角考虑,工业固氮应该选择常温条件,但实际工业生产却选择500℃左右的高温,解释其原因___________ 。
⑤25℃时,向0.1mol/L的氨水中加入少量氯化铵固体,当固体溶解后,测得溶液pH减小,主要原因是(填序号)___________ 。
a.氨水与氯化铵发生化学反应
b.氯化铵溶液水解显酸性,增加了c(H+)
c.铵根离子浓度增大,抑制了氨水的电离,使c(OH―)减小
⑥室温下,如果将0.1mol NH4Cl和0.05mol NaOH全部溶于水,形成混合溶液(假设无损失),___________ 、___________ 和___________ 三种粒子的物质的量之和等于0.1mol。

①下列关于海洋氮循环的说法正确的是
a.海洋中的反硝化作用一定有氧气的参与
b.海洋中的氮循环起始于氮的氧化
c.向海洋排放含NO
 的废水会影响海洋中NH
的废水会影响海洋中NH 的含量
的含量d.海洋中存在游离态的氮
②有氧时,在硝化细菌作用下,NH
 可实现过程④的转化,将过程④的离子方程式补充完整(需配平):
可实现过程④的转化,将过程④的离子方程式补充完整(需配平): + 5O2= 2NO
+ 5O2= 2NO + _______H+ +________+________
+ _______H+ +________+________③有人研究了温度对海洋硝化细菌去除氨氮效果的影响,下表为对10 L人工海水样本的监测数据:
| 温度/℃ | 样本氨氮含量/mg | 处理24 h | 处理48 h |
| 氨氮含量/mg | 氨氮含量/mg | ||
| 20 | 1008 | 838 | 788 |
| 25 | 1008 | 757 | 468 |
| 30 | 1008 | 798 | 600 |
| 40 | 1008 | 977 | 910 |
④海洋中的氮循环起始于氮的固定,氮的固定是几百年来科学家一直研究的课题。下表列举了不同温度下大气固氮和工业固氮的部分K值。
| 反应 | 大气固氮 N2 (g)+O2 (g)  2NO(g) 2NO(g) | 工业固氮 N2 (g)+3H2 (g)  2NH3(g) 2NH3(g) | |||
| 温度/℃ | 27 | 2000 | 25 | 400 | 450 |
| K | 3.84×10-31 | 0.1 | 5×108 | 0.507 | 0.152 |
⑤25℃时,向0.1mol/L的氨水中加入少量氯化铵固体,当固体溶解后,测得溶液pH减小,主要原因是(填序号)
a.氨水与氯化铵发生化学反应
b.氯化铵溶液水解显酸性,增加了c(H+)
c.铵根离子浓度增大,抑制了氨水的电离,使c(OH―)减小
⑥室温下,如果将0.1mol NH4Cl和0.05mol NaOH全部溶于水,形成混合溶液(假设无损失),
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】氮元素是地球上含量丰富的一种元素,氮单质及其化合物在工农业生产、生活中有着重要作用。请回答下列问题:
(1)二氧化氮溶于水时与水反应生成硝酸和一氧化氮,请写出该反应的化学方程式:_______ 。
(2)下列有关氮元素的说法正确的是_______(填字母)。
(3)豆科植物种植时不需施加氮肥的原因是_______ 。
(4)在一定条件下氨气亦可用来将氮氧化物转化为无污染的物质。写出氨气与二氧化氮在一定条件下反应的化学方程式:_______ 。
(1)二氧化氮溶于水时与水反应生成硝酸和一氧化氮,请写出该反应的化学方程式:
(2)下列有关氮元素的说法正确的是_______(填字母)。
| A.氮气因为其化学性质不活泼,可以做保护气,比如充填食品包装,充填电灯泡,保存贵重书画等 |
| B.医学上常用液氮作冷冻剂,在冷冻麻醉条件下做手术,是利用氮气化学性质的不活泼性 |
| C.氮、磷、钾是植物生长必需的营养元素 |
| D.用NO2与水反应制取硝酸时,水做还原剂 |
(4)在一定条件下氨气亦可用来将氮氧化物转化为无污染的物质。写出氨气与二氧化氮在一定条件下反应的化学方程式:
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】I.硫元素是动植物生长不可缺少的元素,硫酸是用途广泛的化工原料,可作脱水剂、吸水剂、氧化剂和催化剂等。
(1)Na2SO3溶液易变质,实验室检验Na2SO3溶液是否变质的基本操作是_______ 。
(2)甲、乙两位同学用铜和硫酸做原料,设计了两种制取硫酸铜的方案。
方案甲:铜与浓硫酸加热直接反应,即Cu→CuSO4,方案乙:由Cu→CuO→CuSO4
①方案甲中,铜和浓硫酸反应的化学方程式是_______ 。该反应体现了浓硫酸_______ 性。
②这两种方案,你认为哪一种方案更合理?_______ 。理由是_______ 。
II.氨和硝酸是重要的工业产品,如图是工业合成氨及制备硝酸的流程示意图:
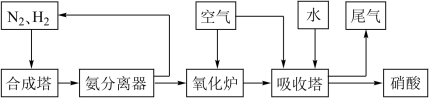
(3)合成塔中发生反应的化学方程式为_______ 。
(4)氨分离器中压强约为15MPa,温度约为-20℃,分离氨应用了氨的_______ 性质。
(5)氧化炉中,NH3转化为NO的化学方程式为_______ 。标准状况下,5.6LNH3被氧化为NO时转移电子的物质的量为_______ 。
(6)写出铜与稀HNO3反应的离子方程式_______
(7)吸收塔中出来的尾气可用Na2CO3溶液吸收,主要反应为:
a.2NO2 + Na2CO3 = NaNO3 +NaNO2 +CO2
b.NO+NO2 + Na2CO3 = 2NaNO2+CO2
根据反应b,每产生22.4L(标准状况下)CO2,吸收液质量将增加_______ g。
(1)Na2SO3溶液易变质,实验室检验Na2SO3溶液是否变质的基本操作是
(2)甲、乙两位同学用铜和硫酸做原料,设计了两种制取硫酸铜的方案。
方案甲:铜与浓硫酸加热直接反应,即Cu→CuSO4,方案乙:由Cu→CuO→CuSO4
①方案甲中,铜和浓硫酸反应的化学方程式是
②这两种方案,你认为哪一种方案更合理?
II.氨和硝酸是重要的工业产品,如图是工业合成氨及制备硝酸的流程示意图:

(3)合成塔中发生反应的化学方程式为
(4)氨分离器中压强约为15MPa,温度约为-20℃,分离氨应用了氨的
(5)氧化炉中,NH3转化为NO的化学方程式为
(6)写出铜与稀HNO3反应的离子方程式
(7)吸收塔中出来的尾气可用Na2CO3溶液吸收,主要反应为:
a.2NO2 + Na2CO3 = NaNO3 +NaNO2 +CO2
b.NO+NO2 + Na2CO3 = 2NaNO2+CO2
根据反应b,每产生22.4L(标准状况下)CO2,吸收液质量将增加
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】探究氮及其化合物的性质,可以有效改善人类的生存环境。氮元素化合价—物质类别关系图如下。回答下列问题:
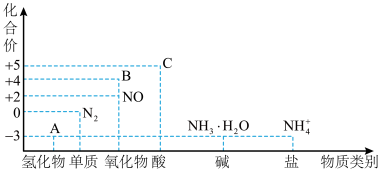
(1)实验室常用NH4Cl与Ca(OH)2制取物质A,A的电子式为___________ ,该反应的化学方程式为___________ 。
(2)在催化剂和加热的条件下,物质A生成NO是工业制硝酸的重要反应,化学方程式是___________ 。
(3)在加热条件下,物质C的稀溶液与铜反应,写出该反应的离子化学方程式:___________ 。
(4)在催化剂和加热条件下,A与B可反应生成无害物质,请写出反应的化学方程式:___________ 。
(5)将盛有N2和NO2混合气体的试管倒立于水中,经过足够长时间后,试管内气体的体积缩小为原来的一半,则原混合气体中N2与NO2的体积比是___________ 。
(6)50 mL浓HNO3与12.8 g Cu恰好完全反应,生成NO、NO2混合气体4.48 L(转化为标准状况下):
①反应生成NO、NO2体积比是___________ ;
②50 mL浓HNO3的物质的量浓度是___________ 。

(1)实验室常用NH4Cl与Ca(OH)2制取物质A,A的电子式为
(2)在催化剂和加热的条件下,物质A生成NO是工业制硝酸的重要反应,化学方程式是
(3)在加热条件下,物质C的稀溶液与铜反应,写出该反应的离子化学方程式:
(4)在催化剂和加热条件下,A与B可反应生成无害物质,请写出反应的化学方程式:
(5)将盛有N2和NO2混合气体的试管倒立于水中,经过足够长时间后,试管内气体的体积缩小为原来的一半,则原混合气体中N2与NO2的体积比是
(6)50 mL浓HNO3与12.8 g Cu恰好完全反应,生成NO、NO2混合气体4.48 L(转化为标准状况下):
①反应生成NO、NO2体积比是
②50 mL浓HNO3的物质的量浓度是
您最近一年使用:0次



