苯胺是一种重要精细化工原料,在染料、医药等行业中具有广泛的应用。可利用硝基苯制取苯胺,其原理如下:
I.制取硝基苯。
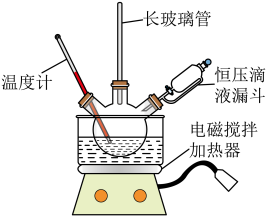
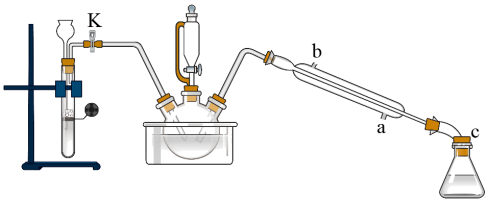
实验步骤:实验室采用如图所示装置制取硝基苯,恒压滴液漏斗中装有一定量的苯,三颈烧瓶装有一定比例的浓硫酸和浓硝酸混合物。
(1)实验装置中长玻璃管可以用___________ 代替(填仪器名称),图中恒压滴液漏斗侧面橡胶管的作用___________
(2)下列说法中正确的是___________(填序号)。
(3)三颈烧瓶中发生反应的化学方程式___________ 。
(4)提纯产品的过程中需要用5%NaOH溶液洗涤三颈烧瓶中的粗产品,其目的是______ 。
II.制取苯胺
①组装好实验装置(如下图,夹持仪器已略去),并检查气密性。
③打开活塞K,通入H2一段时间。
④利用油浴加热,使反应液温度维持在140℃进行反应。
⑤反应结束后,关闭活塞K,向三颈烧瓶中加入生石灰。
⑥调整好温度计的位置,继续加热,收集182~186℃馏分,得到较纯苯胺。
回答下列问题:
(5)若实验中步骤③和④的顺序颠倒,则实验中可能产生的不良后果是___________ 。
(6)步骤⑤中,加入生石灰的作用是___________ 。
(7)若实验中硝基苯用量为10 mL,最后得到苯胺5.6g,苯胺的产率为___________ (计算结果精确到0.1%)。
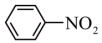 +3H2
+3H2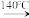
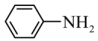 +2H2O
+2H2O
| 物质 | 相对分子质量 | 沸点/℃ | 密度 g/mL | 溶解性 |
| 硝基苯 | 123 | 210.9 | 1.23 | 不溶于水,易溶于乙醇、乙醚 |
| 苯胺 | 93 | 184.4 | 1.02 | 微溶于水,易溶于乙醇、乙醚;还原性强、易被氧化 |
实验步骤:实验室采用如图所示装置制取硝基苯,恒压滴液漏斗中装有一定量的苯,三颈烧瓶装有一定比例的浓硫酸和浓硝酸混合物。
(1)实验装置中长玻璃管可以用
(2)下列说法中正确的是___________(填序号)。
| A.配制混酸时,将浓硝酸沿杯壁缓缓加入浓硫酸中,并不断搅拌、冷却 |
| B.温度控制在50~60℃原因之一是减少副反应的发生 |
| C.制得的粗硝基苯可以先用乙醇萃取,分液后再洗涤 |
| D.浓硫酸可以降低该反应活化能 |
(3)三颈烧瓶中发生反应的化学方程式
(4)提纯产品的过程中需要用5%NaOH溶液洗涤三颈烧瓶中的粗产品,其目的是
II.制取苯胺
①组装好实验装置(如下图,夹持仪器已略去),并检查气密性。
③打开活塞K,通入H2一段时间。
④利用油浴加热,使反应液温度维持在140℃进行反应。
⑤反应结束后,关闭活塞K,向三颈烧瓶中加入生石灰。
⑥调整好温度计的位置,继续加热,收集182~186℃馏分,得到较纯苯胺。
回答下列问题:
(5)若实验中步骤③和④的顺序颠倒,则实验中可能产生的不良后果是
(6)步骤⑤中,加入生石灰的作用是
(7)若实验中硝基苯用量为10 mL,最后得到苯胺5.6g,苯胺的产率为
更新时间:2023-09-08 16:22:03
|
相似题推荐
解答题-有机推断题
|
适中
(0.65)
名校
【推荐1】化合物A是合成雌酮激素的中间体,合成路线如下:
(1)若C的结构简式是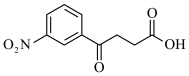 ,则B的结构简式是
,则B的结构简式是_______ 。化合物A中的含氧官能团的名称是_______ 。
(2)若D中只有两种含氧官能团,D的结构简式是_______ 。D的同分异构体W符合下列条件,则W的结构有_______ 种。
①苯环上只有三个取代基,其中一个是氨基
②1molW能与2molNaHCO3反应
③不能发生银镜反应,也不和FeCl3溶液发生反应
(3)B转化为C的化学方程式是_______ 。C转化为D的反应类型是_______ 。
(4)E与足量的氢氧化钠溶液反应的化学方程式为_______ 。
(5)设计由乙酸酐[(CH3CO)2O]和苯制备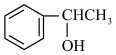 的合成路线:
的合成路线:_______ (无机试剂任选)。
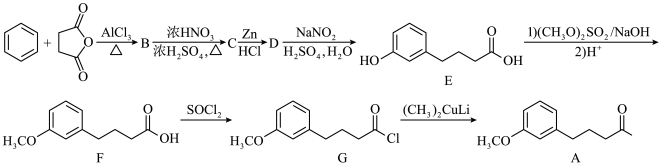
(1)若C的结构简式是
 ,则B的结构简式是
,则B的结构简式是(2)若D中只有两种含氧官能团,D的结构简式是
①苯环上只有三个取代基,其中一个是氨基
②1molW能与2molNaHCO3反应
③不能发生银镜反应,也不和FeCl3溶液发生反应
(3)B转化为C的化学方程式是
(4)E与足量的氢氧化钠溶液反应的化学方程式为
(5)设计由乙酸酐[(CH3CO)2O]和苯制备
 的合成路线:
的合成路线:
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐2】硝基苯是重要的有机中间体。其制备过程如下。
I.硝基苯的制备:
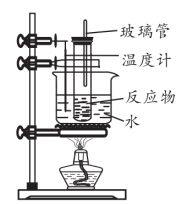
取足量浓硝酸于试管中,再逐滴加入一定量的浓硫酸,边滴边振荡,冷却至室温,最后再加入2.2mL苯,振荡混匀。连好装置,将试管置于50℃至60℃的水浴中加热,一段时间后,将所得液体倒入冷水中,观察制得的硝基苯颜色。
II.硝基苯的提纯:
将已倒入水中的硝基苯转移到梨形分液漏斗中,振荡,静置,进行分液。对下层液体进行水洗、碱洗、水洗并分别分液,再加入无水 ,然后过滤。最后再进行蒸馏,制得硝基苯1.60g。
,然后过滤。最后再进行蒸馏,制得硝基苯1.60g。
回答下列问题。
(1)装置中玻璃管的作用是_______ 。
(2)写出苯和浓硝酸反应的化学方程式_______ 。
(3)此法制备的硝基苯显黄色,可能的原因是_______ 。
(4)对粗硝基苯进行第一次水洗的目的是_______ ,后来加入无水 的作用是
的作用是_______ 。
(5)最后蒸馏操作先出来的馏分是_______ 。
(6)此实验中硝基苯的产率约为_______ (保留三位有效数字)。
I.硝基苯的制备:
取足量浓硝酸于试管中,再逐滴加入一定量的浓硫酸,边滴边振荡,冷却至室温,最后再加入2.2mL苯,振荡混匀。连好装置,将试管置于50℃至60℃的水浴中加热,一段时间后,将所得液体倒入冷水中,观察制得的硝基苯颜色。

| 名称 | 沸点/℃ | 熔点/℃ | 密度/g/mL | 相对分子质量 |
| 苯 | 80.1 | 5.5 | 0.88 | 78 |
| 硝基苯 | 210 | 5.8 | 1.205 | 123 |
将已倒入水中的硝基苯转移到梨形分液漏斗中,振荡,静置,进行分液。对下层液体进行水洗、碱洗、水洗并分别分液,再加入无水
 ,然后过滤。最后再进行蒸馏,制得硝基苯1.60g。
,然后过滤。最后再进行蒸馏,制得硝基苯1.60g。回答下列问题。
(1)装置中玻璃管的作用是
(2)写出苯和浓硝酸反应的化学方程式
(3)此法制备的硝基苯显黄色,可能的原因是
(4)对粗硝基苯进行第一次水洗的目的是
 的作用是
的作用是(5)最后蒸馏操作先出来的馏分是
(6)此实验中硝基苯的产率约为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐3】硝基苯是制造染料的重要原料。某同学在实验室里用下图装置制取硝基苯,主要步骤如下:

①在大试管里将2mL浓硫酸和1.5mL浓硝酸混合,摇匀,冷却到50~60℃以下。然后逐滴加入1mL苯,边滴边振荡试管。
②按图连接好装置,将大试管放入60℃的水浴中加热10分钟。
完成下列填空:
(1)指出图中的错误_________________ 、________________ 。
(2)向混合酸中加入苯时,“逐滴加入”、“边滴边振荡试管”的目的是________________ 。反应一段时间后,混合液明显分为两层,上层呈___________ 色,其中主要物质是_____________ (填写物质名称)。把反应后的混和液倒入盛有冷水的烧杯里,搅拌,可以看到_____ 。(选填编号)
a.水面上是含有杂质的硝基苯 b.水底有浅黄色、苦杏仁味的液体
c.烧杯中的液态有机物只有硝基苯 d.有无色、油状液体浮在水面
(3)为了获得纯硝基苯,实验步骤为:①水洗、分离;②将粗硝基苯转移到盛有_____________ 的烧杯中洗涤、用______________ (填写仪器名称)进行分离;③_____________ ;④干燥;⑤____________ 。
(4)实验装置经改进后,该同学按照上述实验步骤重新进行了多次实验,充分反应后有两种情况出现,请帮助他作出分析:
(1)产率低于理论值,原因是_____________________________________________ ;
(2)产率高于理论值,原因是___________________________________________ 。

①在大试管里将2mL浓硫酸和1.5mL浓硝酸混合,摇匀,冷却到50~60℃以下。然后逐滴加入1mL苯,边滴边振荡试管。
②按图连接好装置,将大试管放入60℃的水浴中加热10分钟。
完成下列填空:
(1)指出图中的错误
(2)向混合酸中加入苯时,“逐滴加入”、“边滴边振荡试管”的目的是
a.水面上是含有杂质的硝基苯 b.水底有浅黄色、苦杏仁味的液体
c.烧杯中的液态有机物只有硝基苯 d.有无色、油状液体浮在水面
(3)为了获得纯硝基苯,实验步骤为:①水洗、分离;②将粗硝基苯转移到盛有
(4)实验装置经改进后,该同学按照上述实验步骤重新进行了多次实验,充分反应后有两种情况出现,请帮助他作出分析:
(1)产率低于理论值,原因是
(2)产率高于理论值,原因是
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐1】硒(Se)是动物和人体所必需的微量元素之一,也是一种重要的工业原料。Na2SeO3可用于治疗克山病,H2Se是制备新型光伏太阳能电池、半导体材料和金属硒化物的重要原料。回答下列问题:
(1)硒在元素周期表的位置是:_______ 。
(2)工业上获得硒的方法很多。
方法一:从含硒废料中提取硒:用硫酸和硝酸钠的混合溶液处理含硒废料后获得亚硒酸和少量硒酸;硒酸再与盐酸共热转化为亚硒酸;最后通入SO2析出硒单质。请写出硒酸与盐酸反应的化学方程式为_______ 。
(3)方法二:某科研小组以硫铁矿生产硫酸过程中产生的含硒物料(主要含S、Se、Fe2O3、CuO、ZnO、SiO2等)提取硒,设计流程如图:

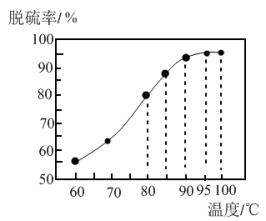
①“脱硫”时,测得脱硫率随温度的变化如图。随着温度的升高,脱硫率呈上升趋势,其原因是_______ 。 “脱硫”时最佳温度是_______ 。
②采用硫脲[ (NH2)2CS]联合亚硫酸钠进行“控电位还原”,将电位高的物质先还原,电位低的物质保留在溶液中,以达到硒与杂质金属的分离。表为“氧化酸浸’液中主要粒子的电位。
a.控制电位在0.740~1.511V范围内,在氧化酸浸液中添加硫脲,可选择性还原ClO2,该过程的还原反应(半反应)式为_______ 。
b.为使硒和杂质金属分离,用亚硫酸钠还原时的最低电位应不低于_______ V。
c.粗硒的精制过程:Na2SO3浸出[Se转化成硒代硫酸钠(Na2SeSO3)]→Na2S净化→H2SO4酸化等步骤。
净化后的溶液中c( Na2S)达到0. 026 mol•L-1,此时溶液中的c(Cu2+ )的最大值为_______ mol. L-1,精硒中基本不含铜。[Ksp(CuS) =1.3×10-36]
(4)某小组同学在实验室利用Na2SeO3溶液与SOCl2也成功制备出Se,请写出相应的离子方程式_______ 。
(1)硒在元素周期表的位置是:
(2)工业上获得硒的方法很多。
方法一:从含硒废料中提取硒:用硫酸和硝酸钠的混合溶液处理含硒废料后获得亚硒酸和少量硒酸;硒酸再与盐酸共热转化为亚硒酸;最后通入SO2析出硒单质。请写出硒酸与盐酸反应的化学方程式为
(3)方法二:某科研小组以硫铁矿生产硫酸过程中产生的含硒物料(主要含S、Se、Fe2O3、CuO、ZnO、SiO2等)提取硒,设计流程如图:

①“脱硫”时,测得脱硫率随温度的变化如图。随着温度的升高,脱硫率呈上升趋势,其原因是

②采用硫脲[ (NH2)2CS]联合亚硫酸钠进行“控电位还原”,将电位高的物质先还原,电位低的物质保留在溶液中,以达到硒与杂质金属的分离。表为“氧化酸浸’液中主要粒子的电位。
| 名称 | Cu2+/Cu | Zn2+/Zn | Fe2+/Fe | Fe3+/Fe | ClO2/Cl- | H2SeO3/Se |
| 电位/V | 0.345 | -0.760 | -0.440 | 0.770 | 1.511 | 0.740 |
b.为使硒和杂质金属分离,用亚硫酸钠还原时的最低电位应不低于
c.粗硒的精制过程:Na2SO3浸出[Se转化成硒代硫酸钠(Na2SeSO3)]→Na2S净化→H2SO4酸化等步骤。
净化后的溶液中c( Na2S)达到0. 026 mol•L-1,此时溶液中的c(Cu2+ )的最大值为
(4)某小组同学在实验室利用Na2SeO3溶液与SOCl2也成功制备出Se,请写出相应的离子方程式
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐2】用含钴废料(主要成分为Co,还含有一定量的NiO、Al2O3、Fe、SiO2等)制备草酸钴晶体(CoC2O4·2H2O)的工艺流程如下图所示:

已知:①草酸钴晶体难溶于水;
②RH为有机物(难电离)。
回答下列问题:
(1)滤渣Ⅰ的主要成分是___________ (填化学式),操作①的名称是___________ ,需用到的玻璃仪器有___________
(2)H2O2是一种绿色氧化剂,加入H2O2时发生反应的离子方程式为___________ 。加入CoO的目的是___________
(3)[已知:溶液中某种离子的浓度小于1.0×10-5mol·L-1,则认为该离子已经完全沉淀;Ni(OH)2、Fe(OH)3、Al(OH)3的Ksp分别为1.0×10-15、1.0×10-38、1.0×10-32]。若要将浸出液中Fe3+和Al3+全部沉淀,则应将浸出液的pH控制在___________ 之间
(4)加入有机溶剂的目的是___________ ,实验室可以用酸性KMnO4标准液滴定溶液中的C2O 浓度,KMnO4标准液常用硫酸酸化,若用盐酸酸化,会使测定结果
浓度,KMnO4标准液常用硫酸酸化,若用盐酸酸化,会使测定结果___________ (填“偏高”“偏低”或“无影响”)

已知:①草酸钴晶体难溶于水;
②RH为有机物(难电离)。
回答下列问题:
(1)滤渣Ⅰ的主要成分是
(2)H2O2是一种绿色氧化剂,加入H2O2时发生反应的离子方程式为
(3)[已知:溶液中某种离子的浓度小于1.0×10-5mol·L-1,则认为该离子已经完全沉淀;Ni(OH)2、Fe(OH)3、Al(OH)3的Ksp分别为1.0×10-15、1.0×10-38、1.0×10-32]。若要将浸出液中Fe3+和Al3+全部沉淀,则应将浸出液的pH控制在
(4)加入有机溶剂的目的是
 浓度,KMnO4标准液常用硫酸酸化,若用盐酸酸化,会使测定结果
浓度,KMnO4标准液常用硫酸酸化,若用盐酸酸化,会使测定结果
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
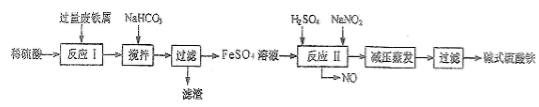
【推荐3】碱式硫酸铁[Fe(OH)SO4]是一种用于污水处理的新型高效絮凝剂,也可用于治疗消化性溃疡出血。工业上利用废铁屑(含少量氧化铝、氧化铁等)生产碱式硫酸铁的工艺流程如下:
回答下列问题:
(1)加入少量NaHCO3的目的是____ ,该反应的离子方程式为______ ;为了加快反应速率,“搅拌”的同时还可以_____ (填操作名称)。
(2)反应II的离子方程式为_____________________________ ;你认为用NaN02的不足之处是______________________ 。某同学选用H2O2代替NaNO2,反应时有气泡产生,写出生成该气体的化学方程式_________________________________ 。
(3)碱式硫酸铁溶于水后产生的Fe(OH)2+离子,可部分水解生成Fe2(OH)42+聚合离子。该水解反应的离子方程式为_______________________________ 。
(4)减压蒸发的目的是_______ 。
(5)为检验所得产品中是否含有Fe2+,可使用的试剂为____
A.氯水 B. KSCN溶液 C.K3[Fe(CN)6]溶液 D.酸性KMnO4溶液

回答下列问题:
(1)加入少量NaHCO3的目的是
(2)反应II的离子方程式为
(3)碱式硫酸铁溶于水后产生的Fe(OH)2+离子,可部分水解生成Fe2(OH)42+聚合离子。该水解反应的离子方程式为
(4)减压蒸发的目的是
(5)为检验所得产品中是否含有Fe2+,可使用的试剂为
A.氯水 B. KSCN溶液 C.K3[Fe(CN)6]溶液 D.酸性KMnO4溶液
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐1】二亚苄基丙酮是重要的有机合成中间体,实验室中由醛(酮)与有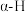 的醛(酮)发生羟醛缩合反应制备而成,其反应原理如下:
的醛(酮)发生羟醛缩合反应制备而成,其反应原理如下:

实验装置如图所示(夹持装置略)。

实验步骤:在仪器a中加入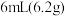 苯甲醛、
苯甲醛、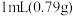 丙酮和
丙酮和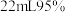 乙醇。启动搅拌器,缓缓滴入
乙醇。启动搅拌器,缓缓滴入 溶液,控制反应温度为
溶液,控制反应温度为 。滴加完毕继续保温搅拌
。滴加完毕继续保温搅拌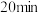 ,反应结束后过滤。向过滤后得到的固体中加入冰醋酸和乙醇的混合溶液,静置
,反应结束后过滤。向过滤后得到的固体中加入冰醋酸和乙醇的混合溶液,静置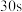 ,再次过滤水洗,晾干,制得
,再次过滤水洗,晾干,制得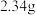 淡黄色固体。
淡黄色固体。
已知:
回答下列问题:
(1)仪器a的名称为___________ ,装置中支管b的作用为___________ 。
(2)苯甲醛久置会部分氧化为苯甲酸并溶于其中,实验前为提纯苯甲醛要___________ (填操作名称)。羟醛缩合反应为放热反应,实验中要控制反应温度为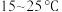 ,适宜的控温方式为
,适宜的控温方式为___________ 。
(3)开始时加入乙醇的作用为___________ 。
(4)若实验中所用 溶液的浓度过高,则苯甲醛易发生自身氧化还原反应,反应的方程式为
溶液的浓度过高,则苯甲醛易发生自身氧化还原反应,反应的方程式为___________ 。
(5)向过滤后得到的固体中加入冰醋酸和乙醇混合溶液,目的是___________ 。依据反应原理反应物分子间按照1∶1反应,可能生成的副产物的结构简式为___________ 。
(6)本实验的产率为___________ %(保留到小数点后一位)。
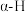 的醛(酮)发生羟醛缩合反应制备而成,其反应原理如下:
的醛(酮)发生羟醛缩合反应制备而成,其反应原理如下:
实验装置如图所示(夹持装置略)。

实验步骤:在仪器a中加入
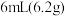 苯甲醛、
苯甲醛、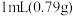 丙酮和
丙酮和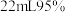 乙醇。启动搅拌器,缓缓滴入
乙醇。启动搅拌器,缓缓滴入 溶液,控制反应温度为
溶液,控制反应温度为 。滴加完毕继续保温搅拌
。滴加完毕继续保温搅拌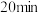 ,反应结束后过滤。向过滤后得到的固体中加入冰醋酸和乙醇的混合溶液,静置
,反应结束后过滤。向过滤后得到的固体中加入冰醋酸和乙醇的混合溶液,静置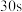 ,再次过滤水洗,晾干,制得
,再次过滤水洗,晾干,制得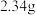 淡黄色固体。
淡黄色固体。已知:
| 苯甲醛 | 无色液体,沸点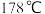 ,微溶于水,溶于乙醇等,易被氧化,相对分子质量为106 ,微溶于水,溶于乙醇等,易被氧化,相对分子质量为106 |
| 丙酮 | 无色液体,沸点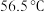 ,与水互溶,常用的有机溶剂,相对分子质量为58 ,与水互溶,常用的有机溶剂,相对分子质量为58 |
| 二亚苄基丙酮 | 淡黄色固体,熔点 ,不溶于水,溶于乙醇、丙酮等,相对分子质量为234 ,不溶于水,溶于乙醇、丙酮等,相对分子质量为234 |
(1)仪器a的名称为
(2)苯甲醛久置会部分氧化为苯甲酸并溶于其中,实验前为提纯苯甲醛要
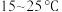 ,适宜的控温方式为
,适宜的控温方式为(3)开始时加入乙醇的作用为
(4)若实验中所用
 溶液的浓度过高,则苯甲醛易发生自身氧化还原反应,反应的方程式为
溶液的浓度过高,则苯甲醛易发生自身氧化还原反应,反应的方程式为(5)向过滤后得到的固体中加入冰醋酸和乙醇混合溶液,目的是
(6)本实验的产率为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐2】1—溴丙烷是一种重要的有机合成中间体,实验室制备1—溴丙烷(CH3CH2CH2Br)的主要反应如下:
Ⅰ.NaBr+H2SO4 NaHSO4+HBr
NaHSO4+HBr
CH3CH2CH2OH+HBr CH3CH2CH2Br+H2O
CH3CH2CH2Br+H2O
Ⅱ.2CH3CH2CH2OH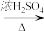 (CH3CH2CH2)2O(正丙醚)+H2O
(CH3CH2CH2)2O(正丙醚)+H2O
可能用到的数据如下:
实验室制备少量1—溴丙烷的主要步骤如下:
步骤1:在仪器A中加入搅拌磁子、12.00g正丙醇及20.0mL水,冰水冷却下缓慢加入28.0mL浓硫酸;冷却至室温,搅拌下加入24.00gNaBr。
步骤2:如图所示搭建实验装置,缓慢加热,直到无油状物馏出为止。
步骤3:将馏出液转入分液漏斗,分出有机相。
步骤4:将分出的有机相转入分液漏斗,依次用12.0mLH2O、12.0mL5%Na2CO3溶液和12.0mLH2O洗涤,分液。
步骤5:将有机相再蒸馏,收集馏出液,得到纯净的1—溴丙烷14.76g。

(1)仪器A的名称是__ ;加热A前,需先从__ (填“a”或“b”)口向A中通入水。加入搅拌磁子的目的是搅拌和__ 。
(2)步骤1中将浓硫酸与20.0mL水相混的主要目的是__ 。
(3)步骤2中需向接收瓶内加入少量冰水并置于冰水浴中的目的是___ 。
(4)步骤4加入12.0mL5%Na2CO3溶液洗涤的化学方程式为:___ 。
(5)步骤5再蒸馏需控制的合适温度为:___ ℃左右,收集馏出液本实验所得到的1—溴丙烷产率是__ 。
Ⅰ.NaBr+H2SO4
 NaHSO4+HBr
NaHSO4+HBrCH3CH2CH2OH+HBr
 CH3CH2CH2Br+H2O
CH3CH2CH2Br+H2OⅡ.2CH3CH2CH2OH
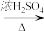 (CH3CH2CH2)2O(正丙醚)+H2O
(CH3CH2CH2)2O(正丙醚)+H2O可能用到的数据如下:
| 相对分子质量 | 密度/g•mL-1 | 沸点/℃ | 水中溶解性 | |
| 正丙醇 | 60 | 0.896 | 97.1 | 溶 |
| 正丙醚 | 102 | 0.74 | 90 | 几乎不溶 |
| 1—溴丙烷 | 123 | 1.36 | 71 | 不溶 |
步骤1:在仪器A中加入搅拌磁子、12.00g正丙醇及20.0mL水,冰水冷却下缓慢加入28.0mL浓硫酸;冷却至室温,搅拌下加入24.00gNaBr。
步骤2:如图所示搭建实验装置,缓慢加热,直到无油状物馏出为止。
步骤3:将馏出液转入分液漏斗,分出有机相。
步骤4:将分出的有机相转入分液漏斗,依次用12.0mLH2O、12.0mL5%Na2CO3溶液和12.0mLH2O洗涤,分液。
步骤5:将有机相再蒸馏,收集馏出液,得到纯净的1—溴丙烷14.76g。

(1)仪器A的名称是
(2)步骤1中将浓硫酸与20.0mL水相混的主要目的是
(3)步骤2中需向接收瓶内加入少量冰水并置于冰水浴中的目的是
(4)步骤4加入12.0mL5%Na2CO3溶液洗涤的化学方程式为:
(5)步骤5再蒸馏需控制的合适温度为:
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐3】青蒿素是烃的含氧衍生物,为无色针状晶体,在甲醇、乙醇、乙醚、石油醚中可溶解,在水中几乎不溶,熔点为156-157℃,热稳定性差,青蒿素是高效的抗疟药。已知:乙醚沸点为35℃,从青蒿素中提取青蒿素的方法之一是以萃取原理为基础的,主要有乙醚萃取法和汽油浸取法。乙醚浸取法的主要工艺如图所示:
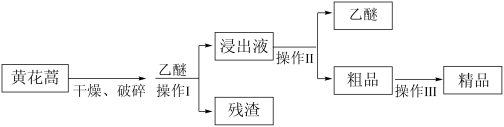
(1)操作I、Ⅱ中,不会用到的装置是______ (填序号)。
A. B.
B.  C.
C.
(2)向干燥、破碎后的黄花蒿中加入乙醚的作用是______ 。
(3)操作Ⅱ的名称是______ ,操作Ⅲ的主要过程可能是______ (填字母)。
A.加水溶解,蒸发浓缩、冷却结晶
B.加95%的乙醇,浓缩、结晶、过滤
C.加入乙醚进行萃取分液
(4)下列有关青蒿素研究的说法正确的是______ 。
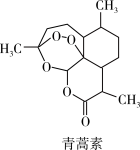
(5)青蒿素分子中的含氧官能团除过氧基(-O-O-)外,还有______ (写名称)。

(1)操作I、Ⅱ中,不会用到的装置是
A.
 B.
B.  C.
C.
(2)向干燥、破碎后的黄花蒿中加入乙醚的作用是
(3)操作Ⅱ的名称是
A.加水溶解,蒸发浓缩、冷却结晶
B.加95%的乙醇,浓缩、结晶、过滤
C.加入乙醚进行萃取分液
(4)下列有关青蒿素研究的说法正确的是

| A.利用黄花蒿茎叶研究青蒿素结构的基本步骤:分离、提纯→元素分析确定实验式→测定相对分子质量确定分子式→波谱分析确定结构式 |
| B.可用X射线衍射测定分子的空间结构 |
| C.元素分析仪可以确定青蒿素中是否含有C、H、O等元素 |
| D.可用质谱法确定分子中含有何种官能团的信息 |
您最近一年使用:0次



