A、B、C、D、E是八年级化学学习中常见的五种物质,它们之间的反应及转化关系如图所示。已知A、C为黑色固体,B、D常温下为气体,且含有相同元素。E中含有生物细胞中含量最多的金属元素。用“一”表示两种物质能够发生反应,用“→”表示一种物质可以转化为另一种物质,请回答问题:
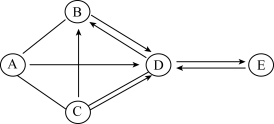
(1)写出B、D的化学式:B___________ 、D___________ 。
(2)写出A转化为D的化学方程式___________ 。
(3)写出D转化为E的化学方程式___________ 。
(4)写出A与C反应的化学方程式___________ 。该基本类型为___________ 。

(1)写出B、D的化学式:B
(2)写出A转化为D的化学方程式
(3)写出D转化为E的化学方程式
(4)写出A与C反应的化学方程式
更新时间:2023-09-10 12:33:31
|
相似题推荐
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐1】“84”消毒液是生活中常见的含氮消毒剂
(1)阅读资料,回答下列相关问题。
资料:“84”消毒液的名称源于北京某医院在1984年研制成功的一种高效含氯消毒液。“84”消毒液呈无色或淡黄色,可由 与NaOH溶液反应制得,其主要成分为NaClO、NaCl。
与NaOH溶液反应制得,其主要成分为NaClO、NaCl。
①资料涉及的物质中,属于碱的是___________ (填化学式,下同);属于盐的是___________ 。
② 与NaOH溶液反应制取“84”消毒液的离子方程式为
与NaOH溶液反应制取“84”消毒液的离子方程式为___________ 。
③“84”消毒液的稀溶液在浸泡餐具过程中,因吸收空气中 使消毒杀菌能力增强,产物中有小苏打,请用离子方程式说明原因:
使消毒杀菌能力增强,产物中有小苏打,请用离子方程式说明原因:___________ 。
(2)如果“84”消毒液与洁厕灵(浓盐酸)混用,会产生一种黄绿色有毒气体,无其它含氯产物,请写出产生该气体的离子方程式:___________ 。
(3)实验室需使用480mL 1.0mol/L的NaOH溶液来制备“84”消毒液。因此首先配制该NaOH溶液。回答下列问题。
①实验需要称量的NaOH固体的质量为___________ g。必须用到的仪器有托盘天平、药匙、玻璃棒、烧杯、胶头滴管和___________ 。称量NaOH固体___________ (填“是”或“否”)可以使用称量纸进行称量。
②下列实验操作步骤的顺序为_________________ (填字母序号)。
③配制过程中,下列操作会引起所配制溶液浓度偏低的是___________ (填字母序号)。
a.NaOH固体已经潮解 b.定容时,俯视容量瓶刻度
c.未洗涤烧杯和玻璃棒 d.摇匀后,发现液面低于刻度线,继续加水至刻度线
(1)阅读资料,回答下列相关问题。
资料:“84”消毒液的名称源于北京某医院在1984年研制成功的一种高效含氯消毒液。“84”消毒液呈无色或淡黄色,可由
 与NaOH溶液反应制得,其主要成分为NaClO、NaCl。
与NaOH溶液反应制得,其主要成分为NaClO、NaCl。①资料涉及的物质中,属于碱的是
②
 与NaOH溶液反应制取“84”消毒液的离子方程式为
与NaOH溶液反应制取“84”消毒液的离子方程式为③“84”消毒液的稀溶液在浸泡餐具过程中,因吸收空气中
 使消毒杀菌能力增强,产物中有小苏打,请用离子方程式说明原因:
使消毒杀菌能力增强,产物中有小苏打,请用离子方程式说明原因:(2)如果“84”消毒液与洁厕灵(浓盐酸)混用,会产生一种黄绿色有毒气体,无其它含氯产物,请写出产生该气体的离子方程式:
(3)实验室需使用480mL 1.0mol/L的NaOH溶液来制备“84”消毒液。因此首先配制该NaOH溶液。回答下列问题。
①实验需要称量的NaOH固体的质量为
②下列实验操作步骤的顺序为
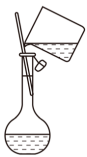 | 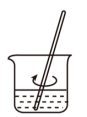 | 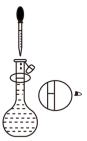 | 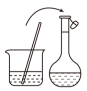 |
| a.转移 | b.溶解 | c.定容 | d.洗涤 |
a.NaOH固体已经潮解 b.定容时,俯视容量瓶刻度
c.未洗涤烧杯和玻璃棒 d.摇匀后,发现液面低于刻度线,继续加水至刻度线
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
【推荐2】粗盐中常含有MgCl2、CaCl2等杂质,提纯粗盐的工艺流程如图所示。回答下列问题:

(1)粗盐水中含有NaCl、CaCl2和MgCl2:
①CaCl2从组成的阳离子来看,属于________ 盐。
②常温下,仅由MgCl2形成的水溶液,________ (填“能”或“不能”)发生丁达尔效应。
(2)步骤Ⅰ中MgCl2与氢氧化钠溶液发生反应的离子方程式为________ 。
(3)步骤Ⅱ中的生成物为CaCO3,该物质中氧元素的质量分数为________ 。
(4)进行操作a时,所用到的装置如图所示(滤纸已略去):
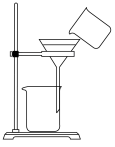
①该装置的错误有________ 处,请指出其错误:________ (写一处即可)。
②过滤后,若往漏斗下端的烧杯中滴入几滴红色石蕊试液,可观察到的现象为________ 。
(5)操作b为蒸发浓缩、冷却结晶,该过程中除了能将水蒸发,还能将过量的稀盐酸除去,主要利用了稀盐酸的________ (填“易挥发性”或“酸性”)。

(1)粗盐水中含有NaCl、CaCl2和MgCl2:
①CaCl2从组成的阳离子来看,属于
②常温下,仅由MgCl2形成的水溶液,
(2)步骤Ⅰ中MgCl2与氢氧化钠溶液发生反应的离子方程式为
(3)步骤Ⅱ中的生成物为CaCO3,该物质中氧元素的质量分数为
(4)进行操作a时,所用到的装置如图所示(滤纸已略去):

①该装置的错误有
②过滤后,若往漏斗下端的烧杯中滴入几滴红色石蕊试液,可观察到的现象为
(5)操作b为蒸发浓缩、冷却结晶,该过程中除了能将水蒸发,还能将过量的稀盐酸除去,主要利用了稀盐酸的
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐3】84消毒液是一种常见的含氯消毒剂,广泛用于家庭、医院的消毒。某学习小组对84消毒液的性质进行探究

查阅资料:①84消毒液的主要成分是 ,还含有少量的
,还含有少量的
②单质碘 (I2)遇淀粉变蓝。
预测性质:
(1)从物质类别看, 属于
属于_______ , 属于
属于_______ (填“强”或“弱”)酸, 可能与某些酸反应。
可能与某些酸反应。
(2)84消毒液具有氧化性,预测的依据是_______ 。
(3)实验验证:
(4)该学习小组同学对实验ⅲ进行了如下改进:
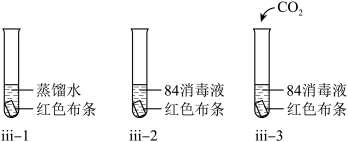
观察到ⅲ—1试管中无明显现象,ⅱ—2、ⅲ—3中红色布条均褪色,ⅲ—3中红色布条褪色更明显。
①对比ⅲ—1、ⅰ—2的现象,可得到的结论是_______ 。
②对比ⅰ—2、ⅲ—3的现象,产生该现象差异的原因是_______ 。

查阅资料:①84消毒液的主要成分是
 ,还含有少量的
,还含有少量的
②单质碘 (I2)遇淀粉变蓝。
预测性质:
(1)从物质类别看,
 属于
属于 属于
属于 可能与某些酸反应。
可能与某些酸反应。(2)84消毒液具有氧化性,预测的依据是
(3)实验验证:
| 实验序号 | 操作 | 现象 | 结论或解释 |
| ⅰ | 向稀释后的84消毒液中滴入稍过量的KI溶液和几滴淀粉 | 84消毒液具有氧化性 | |
| ⅱ | 向稀释后的84消毒液中滴入稀盐酸 | 溶液变为黄绿色 | 反应的离子方程式 |
| ⅲ | 向稀释后的84消毒液中通入 | 无明显现象 |

观察到ⅲ—1试管中无明显现象,ⅱ—2、ⅲ—3中红色布条均褪色,ⅲ—3中红色布条褪色更明显。
①对比ⅲ—1、ⅰ—2的现象,可得到的结论是
②对比ⅰ—2、ⅲ—3的现象,产生该现象差异的原因是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐1】用脱脂棉包住3.9g过氧化钠粉末,置于石棉网上,往脱脂棉上滴水,可观察到脱脂棉剧烈燃烧起来。
(1)由实验现象所得出的有关Na2O2和H2O反应的结论是:
a.该反应有氧气生成,且质量为_____ ;
b._____ 。
(2)某探究小组取相同质量过氧化钠粉末,拟用如图所示装置进行实验,以证明上述结论。
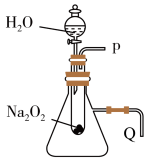
①该反应的离子方程式_____ 。
②用以验证结论a的实验操作方法及现象是_____ 。
③用以验证结论b的实验_____ 。
④向反应后试管中滴加酚酞试液并振荡,现象_____ 。
(3)经小组讨论认为Na2O2和H2O反应可生成H2O2。
①推测该反应类型为_____ ;
②请设计简单易行的实验证明Na2O2和足量的H2O充分反应后的溶液中有H2O2存在_____ 。
(1)由实验现象所得出的有关Na2O2和H2O反应的结论是:
a.该反应有氧气生成,且质量为
b.
(2)某探究小组取相同质量过氧化钠粉末,拟用如图所示装置进行实验,以证明上述结论。

①该反应的离子方程式
②用以验证结论a的实验操作方法及现象是
③用以验证结论b的实验
④向反应后试管中滴加酚酞试液并振荡,现象
(3)经小组讨论认为Na2O2和H2O反应可生成H2O2。
①推测该反应类型为
②请设计简单易行的实验证明Na2O2和足量的H2O充分反应后的溶液中有H2O2存在
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐2】现有金属单质A、B和气体甲、乙、丙及物质D、E、F、G、H,它们之间能发生如图反应(图中有些反应的产物和反应的条件没有标出)。
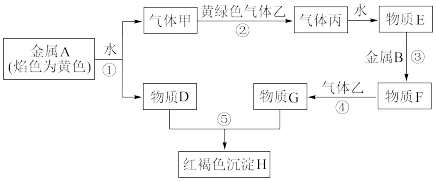
请根据以上信息回答下列问题:
(1)写出下列物质的化学式:F____ 、丙____ 。
(2)写出下列反应的离子方程式:
反应④____ ;
反应⑤____ 。
(3)反应①所属的反应类型是____ (填字母代号)。
(4)有一瓶存放时间长的F溶液,某学生判断其是否变质的检验方法是取F溶液少许,滴加____ ,看是否变红。若变质,应如何除去变质的杂质____ 。

请根据以上信息回答下列问题:
(1)写出下列物质的化学式:F
(2)写出下列反应的离子方程式:
反应④
反应⑤
(3)反应①所属的反应类型是
| A.化合反应 | B.分解反应 | C.置换反应 | D.复分解反应 |
您最近一年使用:0次
【推荐3】Ⅰ.过氧化氢(H2O2)的水溶液俗称双氧水,可用于消毒杀菌。已知:① 受热容易分解;②
受热容易分解;② 可看作二元弱酸。
可看作二元弱酸。
请回答下列问题:
(1) 在水中的主要电离方程式为
在水中的主要电离方程式为___________ 。
(2) 和稀盐酸反应可以生成
和稀盐酸反应可以生成 和
和 ,该反应属于四种基本反应类型中的
,该反应属于四种基本反应类型中的___________ 反应, 中氧元素的化合价为
中氧元素的化合价为___________ 。
(3)水电离生成 和
和 叫做水的自耦电离,可表示为:
叫做水的自耦电离,可表示为: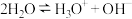 。和水类似,
。和水类似, 也有极微弱的自耦电离,其自耦电离方程式为
也有极微弱的自耦电离,其自耦电离方程式为___________ 。
(4) 与
与 溶液反应生成的“酸式盐”的化学式为
溶液反应生成的“酸式盐”的化学式为___________ 。
Ⅱ.过碳酸钠( )俗称固体双氧水,有
)俗称固体双氧水,有 和
和 的双重性质。
的双重性质。 和
和 反应可制备过碳酸钠,工艺流程如下:
反应可制备过碳酸钠,工艺流程如下:

查阅资料可知:
a.制备反应为 ,该反应放出大量热;
,该反应放出大量热;
b.过碳酸钠易溶于水,难溶于酒精:
c. 时
时 开始分解。
开始分解。
请回答下列问题:
(5)反应中控制温度不宜过高的原因是___________ 。
(6)下列试剂可作“稳定剂”使用的是___________。
 受热容易分解;②
受热容易分解;② 可看作二元弱酸。
可看作二元弱酸。请回答下列问题:
(1)
 在水中的主要电离方程式为
在水中的主要电离方程式为(2)
 和稀盐酸反应可以生成
和稀盐酸反应可以生成 和
和 ,该反应属于四种基本反应类型中的
,该反应属于四种基本反应类型中的 中氧元素的化合价为
中氧元素的化合价为(3)水电离生成
 和
和 叫做水的自耦电离,可表示为:
叫做水的自耦电离,可表示为: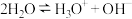 。和水类似,
。和水类似, 也有极微弱的自耦电离,其自耦电离方程式为
也有极微弱的自耦电离,其自耦电离方程式为(4)
 与
与 溶液反应生成的“酸式盐”的化学式为
溶液反应生成的“酸式盐”的化学式为Ⅱ.过碳酸钠(
 )俗称固体双氧水,有
)俗称固体双氧水,有 和
和 的双重性质。
的双重性质。 和
和 反应可制备过碳酸钠,工艺流程如下:
反应可制备过碳酸钠,工艺流程如下:
查阅资料可知:
a.制备反应为
 ,该反应放出大量热;
,该反应放出大量热;b.过碳酸钠易溶于水,难溶于酒精:
c.
 时
时 开始分解。
开始分解。请回答下列问题:
(5)反应中控制温度不宜过高的原因是
(6)下列试剂可作“稳定剂”使用的是___________。
A. | B. | C. | D. |
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐1】有关物质的转化关系如下图所示(部分物质已略去)。A、C都是常见的金属氧化物,B是常见的强酸,D是最常见的无色液体,E、F、H都是常见的气体,且E、F都可用于漂白,H是空气中主要成分之一,I、J都是由三种相同元素(短周期元素)组成的盐。
请回答下列问题:
(1) D的化学式为____________ 。
(2) G的电子式为____________ 。
(3) 写出反应①的化学方程式________________________ 。
(4) 写出反应②的离子方程式________________________ 。

请回答下列问题:
(1) D的化学式为
(2) G的电子式为
(3) 写出反应①的化学方程式
(4) 写出反应②的离子方程式
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
【推荐2】下图表示几种无机物之间的转换关系。其中A为磁性黑色晶体,B为非金属单质,C为无色无毒气体,D为金属单质,E是红棕色气体。
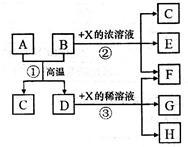
请回答下列问题:
(1)A的化学式为____________ ,C的电子式为_______________ 。
(2)反应②的化学方程式为___________________________ 。
(3)A与盐酸反应的离子方程式为________________________ 。
(4)反应③在X溶液温度、浓度不同时,产物也不同,则过量的D分别与一定量不同温度、浓度的X稀溶液反应时,若4mol X参加反应转移了3mol电子,此时反应的离子方程式为____________________ ;若5mol X参加反应转移了4mol电子,此时X的还原产物可能是下列选项中的______________ 。
a.NO b.N2O c.N2d.NH4NO3

请回答下列问题:
(1)A的化学式为
(2)反应②的化学方程式为
(3)A与盐酸反应的离子方程式为
(4)反应③在X溶液温度、浓度不同时,产物也不同,则过量的D分别与一定量不同温度、浓度的X稀溶液反应时,若4mol X参加反应转移了3mol电子,此时反应的离子方程式为
a.NO b.N2O c.N2d.NH4NO3
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐3】已知A、E为金属单质,B是淡黄色粉末且常用于防毒面具中,回答下题。

(1)实验室中A常常保存在盛放_______ 的广口瓶。
(2)写出B转变成C的化学方程式_______ 。该反应中氧化剂是_______ ,0.1mol B参与该反应,转移电子的个数为_______ 。(阿伏加德罗常数数值用 表示)
表示)
(3)写出D与F反应生成G的离子方程式:_______ 。
(4)描述G放在空气中的颜色变化_______ ,写出它的化学方程式_______ 。
(5)写出E与水蒸气反应的化学方程式_______ 。

(1)实验室中A常常保存在盛放
(2)写出B转变成C的化学方程式
 表示)
表示)(3)写出D与F反应生成G的离子方程式:
(4)描述G放在空气中的颜色变化
(5)写出E与水蒸气反应的化学方程式
您最近一年使用:0次



