“84”消毒液是生活中常见的含氮消毒剂
(1)阅读资料,回答下列相关问题。
资料:“84”消毒液的名称源于北京某医院在1984年研制成功的一种高效含氯消毒液。“84”消毒液呈无色或淡黄色,可由 与NaOH溶液反应制得,其主要成分为NaClO、NaCl。
与NaOH溶液反应制得,其主要成分为NaClO、NaCl。
①资料涉及的物质中,属于碱的是___________ (填化学式,下同);属于盐的是___________ 。
② 与NaOH溶液反应制取“84”消毒液的离子方程式为
与NaOH溶液反应制取“84”消毒液的离子方程式为___________ 。
③“84”消毒液的稀溶液在浸泡餐具过程中,因吸收空气中 使消毒杀菌能力增强,产物中有小苏打,请用离子方程式说明原因:
使消毒杀菌能力增强,产物中有小苏打,请用离子方程式说明原因:___________ 。
(2)如果“84”消毒液与洁厕灵(浓盐酸)混用,会产生一种黄绿色有毒气体,无其它含氯产物,请写出产生该气体的离子方程式:___________ 。
(3)实验室需使用480mL 1.0mol/L的NaOH溶液来制备“84”消毒液。因此首先配制该NaOH溶液。回答下列问题。
①实验需要称量的NaOH固体的质量为___________ g。必须用到的仪器有托盘天平、药匙、玻璃棒、烧杯、胶头滴管和___________ 。称量NaOH固体___________ (填“是”或“否”)可以使用称量纸进行称量。
②下列实验操作步骤的顺序为_________________ (填字母序号)。
③配制过程中,下列操作会引起所配制溶液浓度偏低的是___________ (填字母序号)。
a.NaOH固体已经潮解 b.定容时,俯视容量瓶刻度
c.未洗涤烧杯和玻璃棒 d.摇匀后,发现液面低于刻度线,继续加水至刻度线
(1)阅读资料,回答下列相关问题。
资料:“84”消毒液的名称源于北京某医院在1984年研制成功的一种高效含氯消毒液。“84”消毒液呈无色或淡黄色,可由
 与NaOH溶液反应制得,其主要成分为NaClO、NaCl。
与NaOH溶液反应制得,其主要成分为NaClO、NaCl。①资料涉及的物质中,属于碱的是
②
 与NaOH溶液反应制取“84”消毒液的离子方程式为
与NaOH溶液反应制取“84”消毒液的离子方程式为③“84”消毒液的稀溶液在浸泡餐具过程中,因吸收空气中
 使消毒杀菌能力增强,产物中有小苏打,请用离子方程式说明原因:
使消毒杀菌能力增强,产物中有小苏打,请用离子方程式说明原因:(2)如果“84”消毒液与洁厕灵(浓盐酸)混用,会产生一种黄绿色有毒气体,无其它含氯产物,请写出产生该气体的离子方程式:
(3)实验室需使用480mL 1.0mol/L的NaOH溶液来制备“84”消毒液。因此首先配制该NaOH溶液。回答下列问题。
①实验需要称量的NaOH固体的质量为
②下列实验操作步骤的顺序为
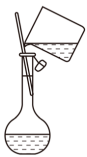 | 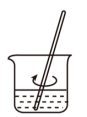 | 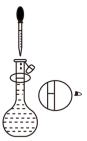 | 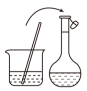 |
| a.转移 | b.溶解 | c.定容 | d.洗涤 |
a.NaOH固体已经潮解 b.定容时,俯视容量瓶刻度
c.未洗涤烧杯和玻璃棒 d.摇匀后,发现液面低于刻度线,继续加水至刻度线
更新时间:2023/11/05 11:19:15
|
相似题推荐
解答题-工业流程题
|
适中
(0.65)
名校
【推荐1】孔雀石主要含Cu2(OH)2CO3,还含少量Fe、SiO2.实验室以孔雀石为原料制备CuSO4•5H2O及CaCO3的步骤如图:
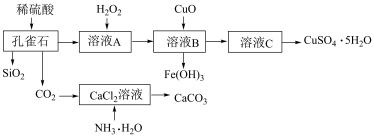
(1)H2O2中氧元素的化合价为___________ ,因此H2O2具有强氧化性。
(2)Cu2(OH)2CO3属于___________ (填“酸”“碱”或“盐”)。
(3)制备CaCO3时,发生的反应的化学方程式为___________ 。
(4)在一定条件下发生氧化还原反应的是___________ 。(填序号)
①孔雀石与稀盐酸 ②溶液A与H2O2
③溶液B与CuO ④CO2与NH3•H2O、CaCl2溶液
(5)C2O3能与水反应生成乙二酸(H2C2O4,一种二元酸),则C2O3是___________ 氧化物,(填“酸性”、“碱性”或“两性”)C2O3与足量NaOH溶液反应的化学方程式为___________ 。

(1)H2O2中氧元素的化合价为
(2)Cu2(OH)2CO3属于
(3)制备CaCO3时,发生的反应的化学方程式为
(4)在一定条件下发生氧化还原反应的是
①孔雀石与稀盐酸 ②溶液A与H2O2
③溶液B与CuO ④CO2与NH3•H2O、CaCl2溶液
(5)C2O3能与水反应生成乙二酸(H2C2O4,一种二元酸),则C2O3是
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐2】我国“蓝天保卫战”成果显著,肆虐的雾霾逐渐被遏止。科学家研究发现含氮化合物和含硫化合物在形成雾霾时与大气中的氨有关,转化关系如图所示。

回答下列问题:
(1)从物质分类的角度分析,图中物质属于酸性氧化物的是_______ (填化学式)。
(2)工业上利用氨气制备一氧化氮,反应的化学方程式为_______ 。
(3)下列关于雾霾叙述不正确的是_______(填字母)。
(4)实验室保存浓硝酸需使用棕色试剂瓶,并放置在阴凉避光处,原因是_______ (用化学方程式表示)。
(5)某化工小组进行了ClO2协同氨水法脱除模拟烟气中NOx和SO2的实验研究,其流程如图:
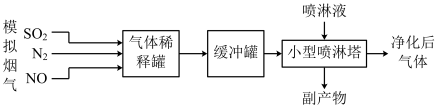
①制备“模拟烟气”时应首先向装置管道内通入_______ ,目的是_______ 。
②喷淋塔中所得副产物除NH4Cl外,还有_______ (填化学式)。
③传统湿式氨法烟气处理技术以尿素[CO(NH2)2]热水解产生的NH3溶于水为喷淋液。在催化剂作用下,喷淋除去NO过程中有一种无污染气体生成,该反应的化学方程式为_______ 。

回答下列问题:
(1)从物质分类的角度分析,图中物质属于酸性氧化物的是
(2)工业上利用氨气制备一氧化氮,反应的化学方程式为
(3)下列关于雾霾叙述不正确的是_______(填字母)。
| A.雾和霾的分散质、分散剂相同 | B.雾霾中含有硝酸铵和硫酸铵 |
| C.NH3是形成无机颗粒物的催化剂 | D.雾霾的形成与过度施用氮肥有关 |
(5)某化工小组进行了ClO2协同氨水法脱除模拟烟气中NOx和SO2的实验研究,其流程如图:

①制备“模拟烟气”时应首先向装置管道内通入
②喷淋塔中所得副产物除NH4Cl外,还有
③传统湿式氨法烟气处理技术以尿素[CO(NH2)2]热水解产生的NH3溶于水为喷淋液。在催化剂作用下,喷淋除去NO过程中有一种无污染气体生成,该反应的化学方程式为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐3】中药常采用硫黄熏蒸法以达到防霉、防虫等目的。我国规定党参等中药 残留量不得超过
残留量不得超过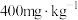 。某小组欲检测某药厂所售党参是否合格,查阅资料后得知:
。某小组欲检测某药厂所售党参是否合格,查阅资料后得知:
① 残留量是指残留硫的总量,以
残留量是指残留硫的总量,以 计;
计;
②中药中残留的 已大部分转化为
已大部分转化为 。
。
(1)将200g所售党参研碎,用500mL 0.01 NaOH溶液充分浸泡,得无色浸泡液X,将X分成两等份。用NaOH溶液浸泡的目的
NaOH溶液充分浸泡,得无色浸泡液X,将X分成两等份。用NaOH溶液浸泡的目的___________ (用化学方程式表示)。
(2)甲同学取一份X溶液采用如下方案测定党参中 残留量:
残留量: 溶液已过量的操作为
溶液已过量的操作为___________ 。
②党参中 残留量的表达式为
残留量的表达式为___________  (用含m的式子表示)。
(用含m的式子表示)。
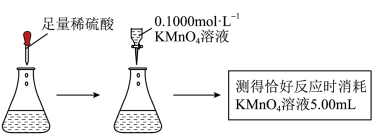
(3)乙同学取另一份X溶液采用如下方案进行测定(整个过程无气体放出),判断该党参___________ (填“符合”或“不符合”)国家标准。 排放。在煤炭中加入一定量石灰石,850℃在氧气的作用下,发生反应
排放。在煤炭中加入一定量石灰石,850℃在氧气的作用下,发生反应 。
。
①通入的气体中氧气的浓度偏低时,产生的CO与 反应生成CaO等三种氧化物,该反应的化学方程式为
反应生成CaO等三种氧化物,该反应的化学方程式为___________ ,被氧化的元素为___________ (填元素符号)。
②从物质类别角度分析,上述①中方程式涉及的物质中,既属于电解质又属于盐的是___________ 。
 残留量不得超过
残留量不得超过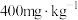 。某小组欲检测某药厂所售党参是否合格,查阅资料后得知:
。某小组欲检测某药厂所售党参是否合格,查阅资料后得知:①
 残留量是指残留硫的总量,以
残留量是指残留硫的总量,以 计;
计;②中药中残留的
 已大部分转化为
已大部分转化为 。
。(1)将200g所售党参研碎,用500mL 0.01
 NaOH溶液充分浸泡,得无色浸泡液X,将X分成两等份。用NaOH溶液浸泡的目的
NaOH溶液充分浸泡,得无色浸泡液X,将X分成两等份。用NaOH溶液浸泡的目的(2)甲同学取一份X溶液采用如下方案测定党参中
 残留量:
残留量: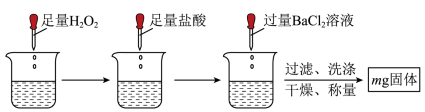
 溶液已过量的操作为
溶液已过量的操作为②党参中
 残留量的表达式为
残留量的表达式为 (用含m的式子表示)。
(用含m的式子表示)。(3)乙同学取另一份X溶液采用如下方案进行测定(整个过程无气体放出),判断该党参
 排放。在煤炭中加入一定量石灰石,850℃在氧气的作用下,发生反应
排放。在煤炭中加入一定量石灰石,850℃在氧气的作用下,发生反应 。
。①通入的气体中氧气的浓度偏低时,产生的CO与
 反应生成CaO等三种氧化物,该反应的化学方程式为
反应生成CaO等三种氧化物,该反应的化学方程式为②从物质类别角度分析,上述①中方程式涉及的物质中,既属于电解质又属于盐的是
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
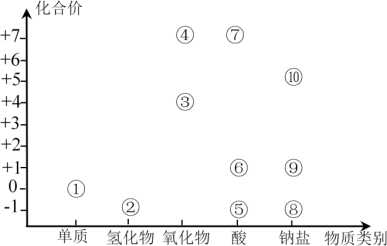
【推荐1】利用氯元素价类二维图可以从不同角度研究含氯物质的性质及其转化关系。图中①~⑩均含氯元素。回答下列问题:___________ ,⑦的电离方程式为___________ 。
(2)②属于___________ (填“电解质”或“非电解质”)。
(3)⑤与⑨混合可产生①,反应的离子方程式为___________ 。
(4)①可与热的浓NaOH溶液反应生成⑧和⑩,该反应中氧化产物与还原产物个数之比为___________ 。
(5)含⑨的溶液可作为水处理剂除去水中的杂质离子。例如它可使酸性废水中的 转化为N2,反应的离子方程式为
转化为N2,反应的离子方程式为___________ 。
(2)②属于
(3)⑤与⑨混合可产生①,反应的离子方程式为
(4)①可与热的浓NaOH溶液反应生成⑧和⑩,该反应中氧化产物与还原产物个数之比为
(5)含⑨的溶液可作为水处理剂除去水中的杂质离子。例如它可使酸性废水中的
 转化为N2,反应的离子方程式为
转化为N2,反应的离子方程式为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐2】磺酰氯( )可用于制造锂电池正极活性物质。实验室可利用
)可用于制造锂电池正极活性物质。实验室可利用 和
和 在活性炭催化下反应制取少量
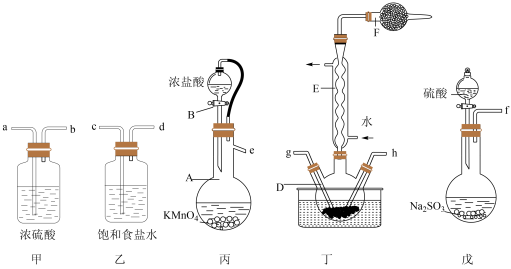
在活性炭催化下反应制取少量 ,装置如图(部分夹持装置已省略)。
,装置如图(部分夹持装置已省略)。
已知:①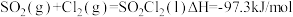
② 熔点为﹣54.1℃,沸点69.1℃,常温较稳定。遇水剧烈水解,100℃以上易分解。回答下列问题:
熔点为﹣54.1℃,沸点69.1℃,常温较稳定。遇水剧烈水解,100℃以上易分解。回答下列问题:
(1)仪器A的名称是______ 。
(2)装置丙中发生反应的离子反应方程式为______ ,上述仪器正确的连接顺序是e→______ →g,h←______ ←f(填仪器接口字母编号,仪器可重复使用)。
(3)装置丁中三颈烧瓶置于冷水浴中,其原因是______ 。
(4)某实验小组利用该装置消耗了氯气1120mL(已转化为标准状况, 足量),最后得到纯净的磺酰氯4.0g,则磺酰氯的产率为
足量),最后得到纯净的磺酰氯4.0g,则磺酰氯的产率为______ (结果保留三位有效数字)。
 )可用于制造锂电池正极活性物质。实验室可利用
)可用于制造锂电池正极活性物质。实验室可利用 和
和 在活性炭催化下反应制取少量
在活性炭催化下反应制取少量 ,装置如图(部分夹持装置已省略)。
,装置如图(部分夹持装置已省略)。
已知:①
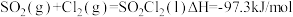
②
 熔点为﹣54.1℃,沸点69.1℃,常温较稳定。遇水剧烈水解,100℃以上易分解。回答下列问题:
熔点为﹣54.1℃,沸点69.1℃,常温较稳定。遇水剧烈水解,100℃以上易分解。回答下列问题:(1)仪器A的名称是
(2)装置丙中发生反应的离子反应方程式为
(3)装置丁中三颈烧瓶置于冷水浴中,其原因是
(4)某实验小组利用该装置消耗了氯气1120mL(已转化为标准状况,
 足量),最后得到纯净的磺酰氯4.0g,则磺酰氯的产率为
足量),最后得到纯净的磺酰氯4.0g,则磺酰氯的产率为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐3】某强酸性溶液X含有 、
、 、
、 、
、 、
、 、
、 、
、 、
、 、
、 、
、 中的一种或几种,取该溶液进行连续实验,实验内容如图。
中的一种或几种,取该溶液进行连续实验,实验内容如图。
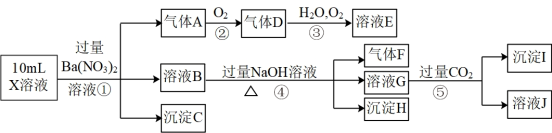
根据以上信息,回答下列问题:
(1)反应③的化学方程式为___________ 。
(2)沉淀C、H和气体F的化学式分别为__________ 。
(3)写出有关反应的离子方程式。
①中生成A:___________ 。
⑤:___________ 。
(4)上述离子中,溶液X中肯定不含有的离子是________ ,可能含有的离子是______ 。
 、
、 、
、 、
、 、
、 、
、 、
、 、
、 、
、 、
、 中的一种或几种,取该溶液进行连续实验,实验内容如图。
中的一种或几种,取该溶液进行连续实验,实验内容如图。
根据以上信息,回答下列问题:
(1)反应③的化学方程式为
(2)沉淀C、H和气体F的化学式分别为
(3)写出有关反应的离子方程式。
①中生成A:
⑤:
(4)上述离子中,溶液X中肯定不含有的离子是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐1】请用下列装置设计一个实验,证明Cl2的氧化性比I2的氧化性强。
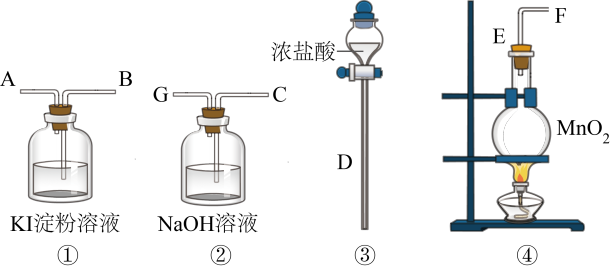
请回答下列问题:
(1)圆底烧瓶中发生反应的化学方程式为___________ 。
(2)证明Cl2比I2的氧化性强的实验现象是___________ ,反应的离子方程式是___________ 。
(3)装置②的作用是___________ 。
(4)若要证明Cl2的氧化性比Br2强,则需做的改动是___________ 。

请回答下列问题:
(1)圆底烧瓶中发生反应的化学方程式为
(2)证明Cl2比I2的氧化性强的实验现象是
(3)装置②的作用是
(4)若要证明Cl2的氧化性比Br2强,则需做的改动是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐2】氯的含氧酸盐具有较强的氧化性,能够杀菌消毒,在预防新冠疫情中起到重要作用。某化学兴趣小组用氯气和相应的碱溶液反应制取NaClO和KClO3,制备装置如图所示(部分加持仪器略去)。已知:氯气与碱反应,温度较高时生成 ,温度较低时生成ClO-。
,温度较低时生成ClO-。
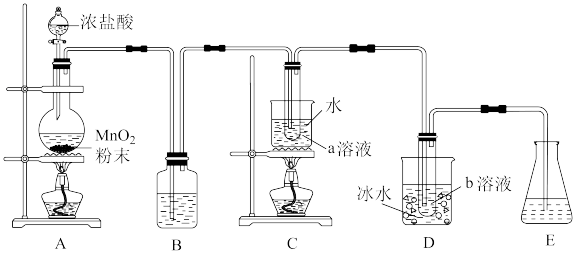
(1)盛装浓盐酸的仪器名称是___________ 。
(2)写出装置A烧瓶中反应的化学方程式并用双线桥表示电子的转移情况___________ 。
(3)b溶液是___________ ,原因是___________ 。
(4)E中可选用试剂有___________(填标号)。
(5)用氯气对饮用水消毒副作用多,产生影响人体健康有机氯衍生物。可用氯气制取高铁酸钠净水:____Fe3++_____(______)+______Cl2→_____ +_____+_____H2O,补全缺项,并配平上述离子方程式
+_____+_____H2O,补全缺项,并配平上述离子方程式___________ ;
(6)如果缺少装置B,对制取NaClO和KClO3的影响是__________ 。
 ,温度较低时生成ClO-。
,温度较低时生成ClO-。
(1)盛装浓盐酸的仪器名称是
(2)写出装置A烧瓶中反应的化学方程式并用双线桥表示电子的转移情况
(3)b溶液是
(4)E中可选用试剂有___________(填标号)。
| A.饱和Na2CO3溶液 | B.浓H2SO4 |
| C.饱和NaCl溶液 | D.NaOH溶液 |
 +_____+_____H2O,补全缺项,并配平上述离子方程式
+_____+_____H2O,补全缺项,并配平上述离子方程式(6)如果缺少装置B,对制取NaClO和KClO3的影响是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐3】水合肼(N2H4∙H2O)可用作抗氧剂等,常用尿素[CO(NH2)2]和NaClO 溶液反应制备水合肼与无水Na2SO3.已知:①Cl2+2OH-=ClO- +Cl- +H2O是放热反应;②N2H4∙H2O沸点118℃,具有强还原性,能与NaClO剧烈反应生成氮气。
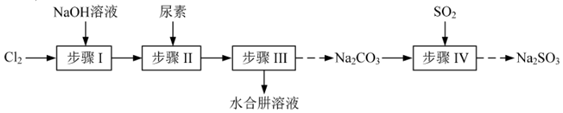
I.制备NaClO溶液
(1)步骤I制备NaClO溶液时,若温度超过40℃,有副反应发生生成 NaClO3,该副反应的离子方程式为_______ 。为了避免副反应的发生除了用冰水浴降温,还可以采取的措施有_______ 。
II.制取水合肼:合成N2H4∙H2O的装置如图1所示。
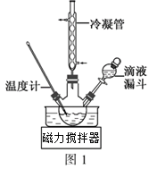
(2)图1中NaClO碱性溶液与尿素CO(NH2)2水溶液在40℃以下反应一段时间后,再迅速升温至110℃继续反应。实验中通过滴液漏斗滴加的溶液是_______ (填“NaClO碱性溶液”或“CO(NH2)2水溶液”);使用冷凝管的目的是_______ 。
(3)三颈烧瓶中反应的化学方程式_______ 。
III.步骤IV用步骤III得到的副产品Na2CO3制备无水Na2SO3,水溶液中H2SO3、 、
、 随pH的分布如图2所示,Na2SO3的溶解度曲线如图3所示。
随pH的分布如图2所示,Na2SO3的溶解度曲线如图3所示。
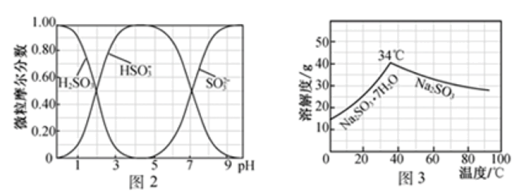
(4)边搅拌边向Na2CO3溶液中通入SO2制备NaHSO3溶液,实验中当溶液pH约为_______ 停止通SO2。
(5)请补充完整由NaHSO3溶液制备无水Na2SO3的实验方案:边搅拌边向NaHSO3溶液中滴加NaOH溶液,测量溶液pH,pH约为10时,停止滴加NaOH溶液,加热浓缩溶液至有大量晶体析出,_______ ,用少量无水乙醇洗涤,干燥,密封包装。

I.制备NaClO溶液
(1)步骤I制备NaClO溶液时,若温度超过40℃,有副反应发生生成 NaClO3,该副反应的离子方程式为
II.制取水合肼:合成N2H4∙H2O的装置如图1所示。

(2)图1中NaClO碱性溶液与尿素CO(NH2)2水溶液在40℃以下反应一段时间后,再迅速升温至110℃继续反应。实验中通过滴液漏斗滴加的溶液是
(3)三颈烧瓶中反应的化学方程式
III.步骤IV用步骤III得到的副产品Na2CO3制备无水Na2SO3,水溶液中H2SO3、
 、
、 随pH的分布如图2所示,Na2SO3的溶解度曲线如图3所示。
随pH的分布如图2所示,Na2SO3的溶解度曲线如图3所示。
(4)边搅拌边向Na2CO3溶液中通入SO2制备NaHSO3溶液,实验中当溶液pH约为
(5)请补充完整由NaHSO3溶液制备无水Na2SO3的实验方案:边搅拌边向NaHSO3溶液中滴加NaOH溶液,测量溶液pH,pH约为10时,停止滴加NaOH溶液,加热浓缩溶液至有大量晶体析出,
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐1】下图是硫酸试剂瓶标签上的内容:

(1)某化学兴趣小组进行硫酸性质的实验探究时,需要490mL 4.6mol·L-1的稀硫酸,现要配制该浓度的溶液所需的玻璃仪器除量筒、烧杯、玻璃棒、胶头滴管外,还需要__________ (填仪器名称);需要量取98%浓硫酸____________ mL进行配制;
(2)配制溶液时有如下操作:a.稀释溶解b.摇匀c.洗涤d.冷却e.量取f.将溶液移至容量瓶g.定容,实验操作顺序正确的是( ) 。
A. e→a→f→d→c→f→g→b B. e→a→d→f→c→f→g→b
C. e→a→f→d→c→f→b→g D. e→a→d→f→c→f→b→g
(3)下列为配制过程中部分操作的示意图,其中有错误的是____ (填序号);
(4)在配制4.6mol·L-1稀硫酸的过程中,下列情况会引起配制所得的硫酸溶液物质的量浓度偏高的是___ ;
A.未经冷却趁热将溶液注入容量瓶中 B.容量瓶洗涤后,未干燥处理
C.定容时仰视观察液面 D.未洗涤烧杯和玻璃棒
(5)为中和100mL 2.3 mol·L-1KOH溶液后显中性,需要加入________ mL 4.6mol·L-1稀硫酸。

(1)某化学兴趣小组进行硫酸性质的实验探究时,需要490mL 4.6mol·L-1的稀硫酸,现要配制该浓度的溶液所需的玻璃仪器除量筒、烧杯、玻璃棒、胶头滴管外,还需要
(2)配制溶液时有如下操作:a.稀释溶解b.摇匀c.洗涤d.冷却e.量取f.将溶液移至容量瓶g.定容,实验操作顺序正确的是
A. e→a→f→d→c→f→g→b B. e→a→d→f→c→f→g→b
C. e→a→f→d→c→f→b→g D. e→a→d→f→c→f→b→g
(3)下列为配制过程中部分操作的示意图,其中有错误的是
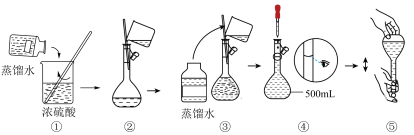
(4)在配制4.6mol·L-1稀硫酸的过程中,下列情况会引起配制所得的硫酸溶液物质的量浓度偏高的是
A.未经冷却趁热将溶液注入容量瓶中 B.容量瓶洗涤后,未干燥处理
C.定容时仰视观察液面 D.未洗涤烧杯和玻璃棒
(5)为中和100mL 2.3 mol·L-1KOH溶液后显中性,需要加入
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐2】根据所学知识,回答下列问题:
(1)0.5mol 的质量为
的质量为_______ g;200mL含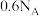 个
个 的
的 溶液中溶质的物质的量浓度为
溶液中溶质的物质的量浓度为_______  ,溶质的物质的量为
,溶质的物质的量为_______ mol。
(2)4.6g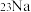 含有的中子的物质的量为
含有的中子的物质的量为_______ mol。
(3)用 的NaOH溶液吸收0.1mol
的NaOH溶液吸收0.1mol  制取简易消毒液,发生反应的化学方程式为
制取简易消毒液,发生反应的化学方程式为_______ ,若 恰好被完全吸收,消耗NaOH溶液的体积为
恰好被完全吸收,消耗NaOH溶液的体积为_______ mL。
(4)某学生欲用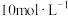 的浓盐酸和蒸馏水配制500mL物质的量浓度为
的浓盐酸和蒸馏水配制500mL物质的量浓度为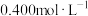 的稀盐酸。
的稀盐酸。
①该学生需要量取_______ mL上述浓盐酸进行配制。
②某同学观察液面时如图所示,对所配溶液的浓度将有何影响?_______ (填“偏高”、“偏低”或“无影响”,下同)。

③若出现如下情况,对所配溶液的浓度将有何影响?
a.没有进行洗涤操作;_______ ;
b.加蒸馏水时不慎超过了刻度线:_______ 。
(1)0.5mol
 的质量为
的质量为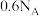 个
个 的
的 溶液中溶质的物质的量浓度为
溶液中溶质的物质的量浓度为 ,溶质的物质的量为
,溶质的物质的量为(2)4.6g
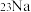 含有的中子的物质的量为
含有的中子的物质的量为(3)用
 的NaOH溶液吸收0.1mol
的NaOH溶液吸收0.1mol  制取简易消毒液,发生反应的化学方程式为
制取简易消毒液,发生反应的化学方程式为 恰好被完全吸收,消耗NaOH溶液的体积为
恰好被完全吸收,消耗NaOH溶液的体积为(4)某学生欲用
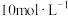 的浓盐酸和蒸馏水配制500mL物质的量浓度为
的浓盐酸和蒸馏水配制500mL物质的量浓度为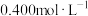 的稀盐酸。
的稀盐酸。①该学生需要量取
②某同学观察液面时如图所示,对所配溶液的浓度将有何影响?

③若出现如下情况,对所配溶液的浓度将有何影响?
a.没有进行洗涤操作;
b.加蒸馏水时不慎超过了刻度线:
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐3】硫代硫酸钠俗名大苏打,可用以除去自来水中的氧气,也可和稀硫酸发生反应: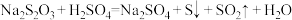 ,已知某硫代硫酸钠溶液试剂瓶体部分标签如图所示,请回答下列问题:
,已知某硫代硫酸钠溶液试剂瓶体部分标签如图所示,请回答下列问题:
(1)该试剂 (摩尔质量:
(摩尔质量: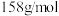 )溶液的物质的量浓度为
)溶液的物质的量浓度为_______ 。
(2)某同学欲用 (摩尔质量:
(摩尔质量: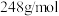 )固体配制60mL与该试剂物质的量浓度相同的溶液,需要用托盘天平称量
)固体配制60mL与该试剂物质的量浓度相同的溶液,需要用托盘天平称量 固体的质量为
固体的质量为_______ g。所用到的主要仪器除如图所示外,还需要的玻璃仪器有_______ 。

(3)该同学用 (密度为
(密度为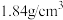 )的浓硫酸配制100mL
)的浓硫酸配制100mL 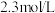 的稀硫酸用于实验,需用浓硫酸的体积为
的稀硫酸用于实验,需用浓硫酸的体积为_______ mL。
(4)若所配制的稀硫酸浓度偏小,则下列可能的原因分析中正确的是_______ (填序号)
①配制前,容量瓶中有少量蒸馏水
②用量筒量取浓硫酸时俯视刻度线
②定容时俯视容量瓶刻度线
④加水时超过容量瓶刻度线,再用胶头滴管吸出
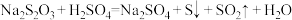 ,已知某硫代硫酸钠溶液试剂瓶体部分标签如图所示,请回答下列问题:
,已知某硫代硫酸钠溶液试剂瓶体部分标签如图所示,请回答下列问题:| 大苏打 【有效成分】  【规格】  【质量分数】 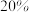 【密度】 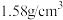 |
 (摩尔质量:
(摩尔质量: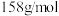 )溶液的物质的量浓度为
)溶液的物质的量浓度为(2)某同学欲用
 (摩尔质量:
(摩尔质量: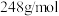 )固体配制60mL与该试剂物质的量浓度相同的溶液,需要用托盘天平称量
)固体配制60mL与该试剂物质的量浓度相同的溶液,需要用托盘天平称量 固体的质量为
固体的质量为
(3)该同学用
 (密度为
(密度为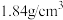 )的浓硫酸配制100mL
)的浓硫酸配制100mL 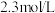 的稀硫酸用于实验,需用浓硫酸的体积为
的稀硫酸用于实验,需用浓硫酸的体积为(4)若所配制的稀硫酸浓度偏小,则下列可能的原因分析中正确的是
①配制前,容量瓶中有少量蒸馏水
②用量筒量取浓硫酸时俯视刻度线
②定容时俯视容量瓶刻度线
④加水时超过容量瓶刻度线,再用胶头滴管吸出
您最近一年使用:0次



