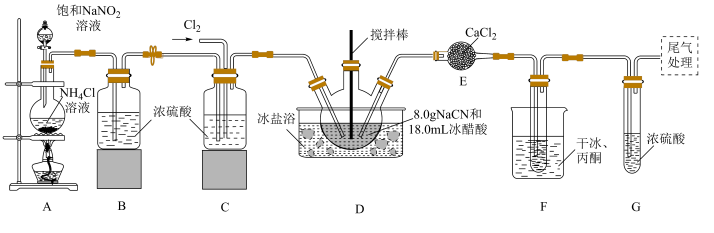
氯化氰(CNCl),又名氯甲氰,是重要的化工中间体,在农药、医药、化工助剂等方面有着广泛的应用。某小组制备氯化氰并探究其性质,实验装置如图所示。回答下列问题:
已知:①CNCl的熔点为−6.5℃,沸点为13.1℃,可溶于水并与水反应;NaCN具有较强的还原性。
②合成原理:在−10℃~−5℃条件下,Cl2+NaCN=NaCl+CNCl。
(1)N2可用装置A制备。盛放饱和NaNO2溶液的仪器名称为___________ ,写出装置A中发生反应的化学方程式:___________ 。
(2)装置F中干冰和丙酮的作用是降低温度,此时干冰___________ (填“升华”或“凝华”);装置G的作用是___________ 。
(3)实验中,先向D中通入___________ (填“N2”或“Cl2”),此操作的目的是___________ 。
(4)实验中必须保持温度在−10~−5℃,若高于−5℃,CNCl与NaCN反应产生NaCl和与卤素性质相似的气体___________ (填化学式)。
(5)向盛有少量Na2S溶液的试管中通入CNCl,然后向其中滴入一滴FeCl3溶液,溶液显红色,其原因是___________ (用离子方程式说明)。

已知:①CNCl的熔点为−6.5℃,沸点为13.1℃,可溶于水并与水反应;NaCN具有较强的还原性。
②合成原理:在−10℃~−5℃条件下,Cl2+NaCN=NaCl+CNCl。
(1)N2可用装置A制备。盛放饱和NaNO2溶液的仪器名称为
(2)装置F中干冰和丙酮的作用是降低温度,此时干冰
(3)实验中,先向D中通入
(4)实验中必须保持温度在−10~−5℃,若高于−5℃,CNCl与NaCN反应产生NaCl和与卤素性质相似的气体
(5)向盛有少量Na2S溶液的试管中通入CNCl,然后向其中滴入一滴FeCl3溶液,溶液显红色,其原因是
更新时间:2023-10-08 16:07:54
|
相似题推荐
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐1】 在化工生产中有重要作用,实验小组用下图装置制备
在化工生产中有重要作用,实验小组用下图装置制备 。请回答下列问题。
。请回答下列问题。

已知:① ,
, ,
,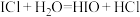
② 、
、 易溶于正己烷(分子式:
易溶于正己烷(分子式: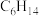 ,沸点:69℃)
,沸点:69℃)
③ 的正己烷溶液呈橙红色,
的正己烷溶液呈橙红色,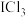 的正己烷溶液呈黄色
的正己烷溶液呈黄色
(1)装置A中反应的化学方程式为_______ 。
(2)仪器a的名称为_______ ,该装置的作用是_______ 。
(3)为使 和
和 充分反应,并溶解在正己烷中,对装置A进行的操作为
充分反应,并溶解在正己烷中,对装置A进行的操作为_______ 。
(4)从B、C、D、E、F中选择合适的装置制备 ,装置正确的连接顺序为A→
,装置正确的连接顺序为A→_______ 。
(5)制备 时,反应温度控制在30~40℃,采用的加热方法是
时,反应温度控制在30~40℃,采用的加热方法是_______ ,当观察到C中的颜色变为_______ 色时,停止加热A装置。
(6)制备 时,
时,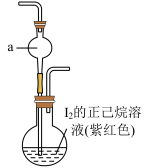 优于
优于 (加热装置已略)的原因有
(加热装置已略)的原因有_______ (答一条即可)。
 在化工生产中有重要作用,实验小组用下图装置制备
在化工生产中有重要作用,实验小组用下图装置制备 。请回答下列问题。
。请回答下列问题。
已知:①
 ,
, ,
,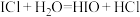
②
 、
、 易溶于正己烷(分子式:
易溶于正己烷(分子式: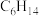 ,沸点:69℃)
,沸点:69℃)③
 的正己烷溶液呈橙红色,
的正己烷溶液呈橙红色,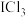 的正己烷溶液呈黄色
的正己烷溶液呈黄色(1)装置A中反应的化学方程式为
(2)仪器a的名称为
(3)为使
 和
和 充分反应,并溶解在正己烷中,对装置A进行的操作为
充分反应,并溶解在正己烷中,对装置A进行的操作为(4)从B、C、D、E、F中选择合适的装置制备
 ,装置正确的连接顺序为A→
,装置正确的连接顺序为A→(5)制备
 时,反应温度控制在30~40℃,采用的加热方法是
时,反应温度控制在30~40℃,采用的加热方法是(6)制备
 时,
时, 优于
优于 (加热装置已略)的原因有
(加热装置已略)的原因有
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
【推荐2】如图是“金字塔”式元素周期表的一部分,图上标有ⅥA族和几种元素的位置。请用准确的化学符号和用语回答下列问题:
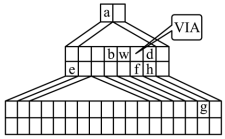
(1)g元素在周期表中的位置___________ ,用一个离子方程式表示h元素和g元素非金属性的强弱___________
(2)w的最低价氢化物与最高价氧化物对应的水化物反应的化学方程式为___________ ;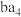 分子的空间构型是
分子的空间构型是___________
(3)d、e、f的简单离子的半径由大到小是:___________ ;
(4)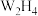 为二元弱碱,
为二元弱碱,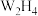 与硫酸形成的酸式盐的化学式为
与硫酸形成的酸式盐的化学式为___________ 。
(5)BrCl属于卤素互化物,性质与 相似。写出BrCl与氢氧化钠溶液反应的化学方程式:
相似。写出BrCl与氢氧化钠溶液反应的化学方程式:___________ ;
(6)下列说法不正确 的是___________。

(1)g元素在周期表中的位置
(2)w的最低价氢化物与最高价氧化物对应的水化物反应的化学方程式为
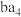 分子的空间构型是
分子的空间构型是(3)d、e、f的简单离子的半径由大到小是:
(4)
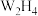 为二元弱碱,
为二元弱碱,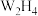 与硫酸形成的酸式盐的化学式为
与硫酸形成的酸式盐的化学式为(5)BrCl属于卤素互化物,性质与
 相似。写出BrCl与氢氧化钠溶液反应的化学方程式:
相似。写出BrCl与氢氧化钠溶液反应的化学方程式:(6)下列说法
| A.元素最高正价与最低负价绝对值相等的元素一定处于第IVA族 |
| B.第5周期第VA族元素的原子序数为65 |
| C.h形成的最简单氢化物比f形成的最简单氢化物的稳定性高 |
| D.周期表中当某元素的周期序数大于其族序数时,该元素可能属于金属或非金属 |
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐3】某小组设计实验制备溴单质,装置如图所示。回答下列问题:___________ (填名称),装置B的作用是___________ 。
(2)补充装置C,画出装置图并注明试剂名称___________ 。
(3)装置A中生成溴单质的化学方程式为___________ 。(副产物有 、
、 ,经检验产物中没有
,经检验产物中没有 生成)
生成)
(4)实验完毕后,利用如图装置提取溴单质。已知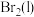 、
、 的沸点依次为
的沸点依次为 、
、 。先收集的物质是
。先收集的物质是___________ (填化学式)。 被称为拟卤素单质,具有卤素相似的性质。为了探究
被称为拟卤素单质,具有卤素相似的性质。为了探究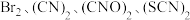 的氧化性强弱,进行实验,实验操作及现象如下:
的氧化性强弱,进行实验,实验操作及现象如下:
已知:拟卤素单质及钾盐水溶液均为无色。
①如果氧化产物为 ,写出操作乙中反应的离子方程式:
,写出操作乙中反应的离子方程式:___________ 。
②某同学得出结论,氧化性: 。该结论
。该结论___________ (填“科学”或“不科学”),理由是___________ (如果填科学,此问不填)。

(2)补充装置C,画出装置图并注明试剂名称
(3)装置A中生成溴单质的化学方程式为
 、
、 ,经检验产物中没有
,经检验产物中没有 生成)
生成)(4)实验完毕后,利用如图装置提取溴单质。已知
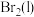 、
、 的沸点依次为
的沸点依次为 、
、 。先收集的物质是
。先收集的物质是
 被称为拟卤素单质,具有卤素相似的性质。为了探究
被称为拟卤素单质,具有卤素相似的性质。为了探究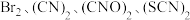 的氧化性强弱,进行实验,实验操作及现象如下:
的氧化性强弱,进行实验,实验操作及现象如下:| 实验操作 | 现象 | |
| 甲 | 向 溶液中滴加几滴溴水,振荡 溶液中滴加几滴溴水,振荡 | 溶液不褪色 |
| 乙 | 向 溶液中滴加溴水,振荡 溶液中滴加溴水,振荡 | 溶液变为无色 |
| 丙 | 向 溶液中滴加溴水,振荡 溶液中滴加溴水,振荡 | 溶液褪色 |
①如果氧化产物为
 ,写出操作乙中反应的离子方程式:
,写出操作乙中反应的离子方程式:②某同学得出结论,氧化性:
 。该结论
。该结论
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐1】PCl3是一种重要的化工原料,实验室用如图装置制取PCl3。已知PCl3的熔点是-112℃,沸点是75.5℃,极易水解,受热易被氧气氧化。
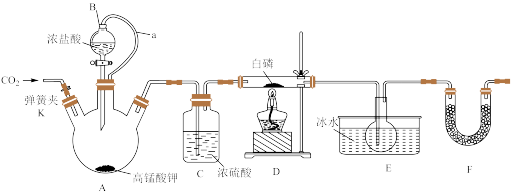
请回答下列问题:
(1)实验开始前的操作依次是:①组装仪器,②_________ ,③加药品,④__________ ,⑤最后点燃酒精灯。
(2)导管a的作用是________ ;F装置的作用是__________ 。
(3)测定产品纯度,步骤如下:
i.称取5.00g产品,溶于水配成100mL溶液(发生反应:PCl3+3H2O=H3PO3+3HCl);
ii.取上述溶液25.00mL,加入20.00mL 0.4000mol/L碘水,充分氧化H3PO3;
iii.以淀粉溶液为指示剂,用0.0500mol/L硫代硫酸钠溶液滴定ii中所得溶液,发生的反应为I2+2 =
= +2I-,消耗硫代硫酸钠溶液12.00mL。
+2I-,消耗硫代硫酸钠溶液12.00mL。
①滴定终点时的现象是____________ 。
②该产品的纯度为____________ 。

请回答下列问题:
(1)实验开始前的操作依次是:①组装仪器,②
(2)导管a的作用是
(3)测定产品纯度,步骤如下:
i.称取5.00g产品,溶于水配成100mL溶液(发生反应:PCl3+3H2O=H3PO3+3HCl);
ii.取上述溶液25.00mL,加入20.00mL 0.4000mol/L碘水,充分氧化H3PO3;
iii.以淀粉溶液为指示剂,用0.0500mol/L硫代硫酸钠溶液滴定ii中所得溶液,发生的反应为I2+2
 =
= +2I-,消耗硫代硫酸钠溶液12.00mL。
+2I-,消耗硫代硫酸钠溶液12.00mL。①滴定终点时的现象是
②该产品的纯度为
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
【推荐2】以硫铁矿烧渣(主要成分是Fe3O4、Fe2O3、FeO和二氧化硅等)制备绿矾 (FeSO4·7H2O)的流程图如下:
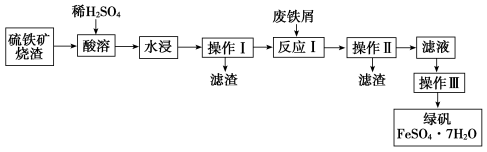
请回答下列问题:
(1)为加快烧渣的酸溶速率可采取的措施是________________________ (答两点即可)。
(2)Fe3O4的俗名是________ ,写出酸溶时Fe2O3溶解的离子方程式 ___________________ 。
(3)检验“反应Ⅰ”已经完全反应的最佳试剂为________ (填序号)。
a.酸性KMnO4溶液 b.氨水 c.硫氰化钾溶液 d.铁氰化钾溶液
(4)为测量所得绿矾中铁元素的质量分数,某实验小组进行了以下实验:取W g绿矾配制成100mL溶液,用________ (填“酸式”或“碱式”)滴定管从中取出20.00 mL溶液放入锥形瓶中待用,滴定时,用________ (填“酸式”或“碱式”)滴定管盛装标准K2Cr2O7溶液,滴定时,左手________ ,右手______________ ,眼睛注视________ ,当达到滴定终点时,消耗0.010mol·L-1的K2Cr2O7 23.20 mL,发生反应的离子方程式是_________________________ ,铁元素的质量分数为________ (用含有W的式子表示)。如果配制绿矾溶液时,没有洗涤烧杯和玻璃棒,造成所测铁元素 的质量分数________ (填“偏大”“偏小”或“无影响”),滴定前读取盛有标准K2Cr2O7溶液的滴定管数据正确,滴定终点时,仰视读数,造成所测铁元素的质量分数________ (填“偏大”“偏小”或“无影响”)。

请回答下列问题:
(1)为加快烧渣的酸溶速率可采取的措施是
(2)Fe3O4的俗名是
(3)检验“反应Ⅰ”已经完全反应的最佳试剂为
a.酸性KMnO4溶液 b.氨水 c.硫氰化钾溶液 d.铁氰化钾溶液
(4)为测量所得绿矾中铁元素的质量分数,某实验小组进行了以下实验:取W g绿矾配制成100mL溶液,用
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
【推荐3】工业上用难溶于水的碳酸锶(SrCO3)粉末为原料(含少量钡和铁的化合物)制备高纯六水氯化锶晶体(SrCl2·6H2O),其过程为:

已知:Ⅰ.有关氢氧化物沉淀的pH:
Ⅱ.SrCl2·6H2O晶体在61℃时开始失去结晶水,100℃时失去全部结晶水。
(1)操作①需要加快反应速率,措施有充分搅拌和____________________ (写一种)。碳酸锶与盐酸反应的离子方程式________________________________ 。
(2)在步骤②~③的过程中,将溶液的pH值由1调节至_______ ;宜用的试剂为_______ 。
A.1.5 B.3.7 C.9.7 D.氨水 E.氢氧化锶粉末 F.碳酸钠晶体
(3)操作③中所得滤渣的主要成分是_______________________ (填化学式)。
(4)工业上用热风吹干六水氯化锶,适宜的温度是_______ 。
A.50~60℃ B.80~100℃ C.100℃以上
(5)步骤⑥宜选用的无机洗涤剂是_______________ 。

已知:Ⅰ.有关氢氧化物沉淀的pH:
| 氢氧化物 | Fe(OH)3 | Fe(OH)2 |
| 开始沉淀的pH | 1.5 | 6.5 |
| 沉淀完全的pH | 3.7 | 9.7 |
Ⅱ.SrCl2·6H2O晶体在61℃时开始失去结晶水,100℃时失去全部结晶水。
(1)操作①需要加快反应速率,措施有充分搅拌和
(2)在步骤②~③的过程中,将溶液的pH值由1调节至
A.1.5 B.3.7 C.9.7 D.氨水 E.氢氧化锶粉末 F.碳酸钠晶体
(3)操作③中所得滤渣的主要成分是
(4)工业上用热风吹干六水氯化锶,适宜的温度是
A.50~60℃ B.80~100℃ C.100℃以上
(5)步骤⑥宜选用的无机洗涤剂是
您最近一年使用:0次



