下列离子方程式或电极反应式书写错误的是
A.用铁作电极电解饱和NaCl溶液:2Cl-+2H2O 2OH-+H2↑+Cl2↑ 2OH-+H2↑+Cl2↑ |
| B.碱性锌锰电池正极的电极反应:MnO2+H2O+e-= MnO(OH)+OH- |
| C.用K3[Fe(CN)6]检验Fe2+的离子方程式:K++[Fe(CN)6]3-+Fe2+=KFe[Fe(CN)6] ↓ |
D.铅蓄电池充电时阴极的电极反应:PbSO4(s)+2e-= Pb(s)+SO (aq) (aq) |
更新时间:2023-10-09 22:56:24
|
相似题推荐
单选题
|
适中
(0.64)
【推荐1】下列离子方程式正确的是
| A.澄清的石灰水与稀盐酸反应Ca(OH)2 + 2H+=== Ca2+ + 2H2O |
| B.钠与水的反应Na + 2H2O === Na+ +2OH -+ H2 ↑ |
| C.硫酸氢钠溶液与少量氢氧化钡溶液混合:2H+ + SO42-+ Ba2+ + 2OH-=== BaSO4↓ + 2H2O |
D.向沸水中滴加FeCl3溶液制备Fe(OH)3胶体:Fe3++3H2O Fe(OH)3↓+3H+ Fe(OH)3↓+3H+ |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】室温下,通过下列实验探究0.1mol·L−1NaHCO3和0.1mol·L−1Na2CO3溶液的性质。
下列说法正确的是
| 实验1: | 用pH试纸测得0.1mol·L−1Na2CO3溶液pH约为12 |
| 实验2: | 两溶液中分别加入等体积的0.1mol·L−1CaCl2溶液,都产生白色沉淀 |
| 实验3: | 0.1mol·L−1NaHCO3与0.1mol·L−1Ba(OH)2溶液等体积混合,产生白色沉淀 |
| 实验4: | 向两溶液中不断滴加0.1mol·L−1HCl溶液,至不再产生气体 |
A.0.1mol·L−1Na2CO3溶液中存在c(OH-)=c(H+)+c( )+c(H2CO3) )+c(H2CO3) |
| B.实验2中CaCl2溶液滴入后,两试管中溶液pH均降低 |
C.实验3中的离子方程式为:Ba2++2OH-+2 =BaCO3↓+ =BaCO3↓+ +2H2O +2H2O |
D.实验4中完全反应后,两试管中溶液中都存在:c(H+)+c(Na+)=c(Cl-)+c(OH-)+c( )+c( )+c( ) ) |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】下列离子方程式书写错误的是
A. 溶于氢碘酸: 溶于氢碘酸: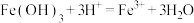 |
B. 溶液与等物质的量 溶液与等物质的量 反应: 反应: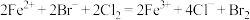 |
C.向小苏打溶液中加入过量的澄清石灰水: |
D.硫酸氢钠溶液与足量氢氧化钡溶液混合: |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】下列离子方程式正确的是
A.用惰性电极电解饱和氯化钠溶液:2Cl- + 2H+  H2↑ + Cl2↑ H2↑ + Cl2↑ |
| B.向Al2(SO4)3溶液中加入过量的NH3·H2O:Al3+ + 4NH3·H2O ═ AlO2-+ 4NH4+ + 2H2O |
| C.苯酚钠溶液中通入少量CO2:CO2 + H2O + 2C6H5O-→ 2C6H5OH + 2 CO32- |
| D.Na2SO3溶液使酸性KMnO4溶液褪色:5SO32- + 6H+ + 2MnO4- ═ 5SO42-+ 2Mn2+ + 3H2O |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】现在污水治理越来越引起人们重视,可以通过膜电池除去废水中的乙酸钠和对氯苯酚( ),其原理如下图所示,下列说法正确的是
),其原理如下图所示,下列说法正确的是

 ),其原理如下图所示,下列说法正确的是
),其原理如下图所示,下列说法正确的是
| A.该装置为电解装置,B为阳极 |
| B.电子从A极沿导线经小灯泡流向B极 |
C.A极的电极反应式为 +e-+ H+=Cl-+ +e-+ H+=Cl-+ |
| D.当外电路中有0.1 mol e-转移时,A极区增加的H+的个数为0.05NA |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】柔性屏手机开始崭露头脚。某柔性屏手机的柔性电池以碳纳米管作电极材料,以吸收ZnSO4溶液的有机高聚物为固态电解质,其电池总反应为:MnO2+ Zn+(1+
Zn+(1+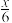 )H2O+
)H2O+ ZnSO4
ZnSO4  MnOOH+
MnOOH+ ZnSO4·3Zn(OH)2·xH2O,其电池结构如图1所示,图2是有机高聚物的结构片段。下列说法中,正确的是
ZnSO4·3Zn(OH)2·xH2O,其电池结构如图1所示,图2是有机高聚物的结构片段。下列说法中,正确的是

 Zn+(1+
Zn+(1+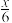 )H2O+
)H2O+ ZnSO4
ZnSO4  MnOOH+
MnOOH+ ZnSO4·3Zn(OH)2·xH2O,其电池结构如图1所示,图2是有机高聚物的结构片段。下列说法中,正确的是
ZnSO4·3Zn(OH)2·xH2O,其电池结构如图1所示,图2是有机高聚物的结构片段。下列说法中,正确的是
| A.充电时,含有锌膜的碳纳米管纤维一端连接电源正极 |
| B.放电时,电极的正极反应为:MnO2+e-+H+=MnOOH |
| C.充电时,Zn2+移向Zn膜 |
| D.氢键是一种特殊的化学键,键能大于共价键,能使高聚物更稳定 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】下列用来表示物质变化的化学用语中,正确的是
| A.电解饱和食盐水:2Cl-+2H2O=H2↑+Cl2↑+2OH- |
B.铅蓄电池充电时阳极反应式为:PbSO4–2e-+2H2O=PbO2+4H++SO |
| C.氢氧燃料电池在碱性介质中的负极反应式:O2+2H2O+4e-=4OH- |
| D.钢铁发生电化学腐蚀的负极反应式:Fe–3e-=Fe3+ |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】乙醛酸是一种重要的化工中间体,可用如下图所示的电化学装置合成。图中的双极膜中间层中的H2O解离为H+和OH-,并在直流电场作用下分别向两极迁移。下列说法正确的是


| A.KBr在上述电化学合成过程中只起电解质的作用 |
B.阳极上的反应式为: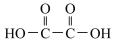   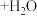 |
| C.制得1mol乙醛酸,理论上外电路中迁移了2mol电子 |
| D.双极膜中间层中的H+在外电场作用下向铅电极方向迁移 |
您最近一年使用:0次





