在催化剂作用下,向容积为1L的容器中加入1molX和3molY,发生反应: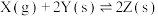 ,平衡时和反应10min时X的转化率α(X)随温度的变化分别如曲线Ⅰ、Ⅱ所示。下列说法正确的是
,平衡时和反应10min时X的转化率α(X)随温度的变化分别如曲线Ⅰ、Ⅱ所示。下列说法正确的是
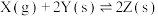 ,平衡时和反应10min时X的转化率α(X)随温度的变化分别如曲线Ⅰ、Ⅱ所示。下列说法正确的是
,平衡时和反应10min时X的转化率α(X)随温度的变化分别如曲线Ⅰ、Ⅱ所示。下列说法正确的是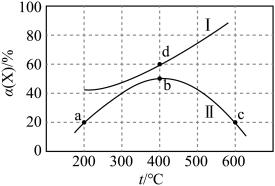
| A.使用更高效的催化剂,可以使b点移动到d点 |
| B.bc段变化可能是由于升高温度平衡逆向移动 |
C.0~10min的平均反应速率: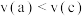 |
D.保持温度和体积不变,向d点体系中再充入1molX,再次达平衡时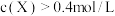 |
更新时间:2023-10-10 15:47:24
|
相似题推荐
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】共价键断键方式有两种,均裂和异裂,例如, 均裂:
均裂: ,
, 异裂:
异裂: 。含有单电子的基团属于自由基,例如Br·为溴自由基,自由基参加的有机反应分三个阶段完成,第一阶段是产生自由基的反应;溴与甲基环戊烷生成1-甲基-1-溴环戊烷的反应属于自由基反应,其第二阶段反应的反应历程可表示为:
。含有单电子的基团属于自由基,例如Br·为溴自由基,自由基参加的有机反应分三个阶段完成,第一阶段是产生自由基的反应;溴与甲基环戊烷生成1-甲基-1-溴环戊烷的反应属于自由基反应,其第二阶段反应的反应历程可表示为:
(1)
(2)
其中能量变化如图所示。下列说法错误的是

 均裂:
均裂: ,
, 异裂:
异裂: 。含有单电子的基团属于自由基,例如Br·为溴自由基,自由基参加的有机反应分三个阶段完成,第一阶段是产生自由基的反应;溴与甲基环戊烷生成1-甲基-1-溴环戊烷的反应属于自由基反应,其第二阶段反应的反应历程可表示为:
。含有单电子的基团属于自由基,例如Br·为溴自由基,自由基参加的有机反应分三个阶段完成,第一阶段是产生自由基的反应;溴与甲基环戊烷生成1-甲基-1-溴环戊烷的反应属于自由基反应,其第二阶段反应的反应历程可表示为:(1)

(2)

其中能量变化如图所示。下列说法错误的是

| A.该反应阶段进行时,溴自由基不断减少 |
| B.反应(1)为该反应阶段的决速步骤 |
| C.升温不利于该反应阶段 |
| D.仅凭反应(1)与反应(2)的活化能不能计算该反应阶段的焓变 |
您最近一年使用:0次
【推荐2】下列实验中,对应的现象以及结论都正确的是
| 选项 | 实验 | 现象 | 结论 |
| A | 向2支盛有5 mL不同浓度NaHSO3溶液的试管中,同时加入2 mL 5% H2O2溶液 | 观察并比较产生气泡的快慢 | 浓度大的反应速率快 |
| B | 取 Al 和Fe2O3 完全反应后固体,溶于足量稀硫酸,滴加 KSCN 溶液 | 溶液不变红 | 反应后固体中可能含有 Fe2O3 |
| C | 将湿润的淀粉-KI 试纸放入含有红棕色气体的集气瓶中 | 试纸变蓝 | 该气体为 NO2 ,具有氧化性 |
| D | 将少量 Fe(NO3)2 加水溶解后,滴加稀硫酸酸化,再滴加 KSCN 溶液 | 溶液呈血红色 | Fe(NO3)2 已变质 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐3】碘在科研与生活中有重要应用。某兴趣小组用 淀粉溶液
淀粉溶液

 等式剂,探究反应条件对化学反应速率的影响。
等式剂,探究反应条件对化学反应速率的影响。
已知: (慢)
(慢)
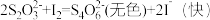
结合表中数据判断下列说法错误的是
 淀粉溶液
淀粉溶液

 等式剂,探究反应条件对化学反应速率的影响。
等式剂,探究反应条件对化学反应速率的影响。已知:
 (慢)
(慢)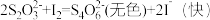
结合表中数据判断下列说法错误的是
| 实验编号 | Ⅰ | Ⅱ | Ⅲ | Ⅳ | Ⅴ | |
试剂用量/ |  | 10.0 | 5.0 | 2.5 | 10.0 | 10.0 |
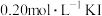 | 10.0 | 10.0 | 10.0 | 5.0 | 2.5 | |
 | 4.0 | 4.0 | 4.0 | 4.0 | 4.0 | |
 淀粉溶液 淀粉溶液 | 2.0 | 2.0 | 2.0 | 2.0 | 2.0 | |
| 蒸馏水 | 0.0 | a | 7.5 | b | 7.5 | |
显色时间 | 35 | 21 | 123 | 56 | 107 | |
A.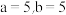 |
B.实验Ⅰ中,用 表示的反应速率为 表示的反应速率为 |
| C.反应液初始浓度越大,反应时间越短,平均反应速率越大 |
D.为确保能观察到蓝色,需满足的关系为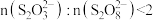 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐1】为探究温度对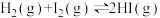 的影响,其他条件相同时,将1molH2(g)和1molI2(g)充入体积为2L的恒容密闭容器中,测得HI(g)的物质的量分数随时间变化的实验数据如表:
的影响,其他条件相同时,将1molH2(g)和1molI2(g)充入体积为2L的恒容密闭容器中,测得HI(g)的物质的量分数随时间变化的实验数据如表:
下列说法正确的是
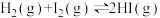 的影响,其他条件相同时,将1molH2(g)和1molI2(g)充入体积为2L的恒容密闭容器中,测得HI(g)的物质的量分数随时间变化的实验数据如表:
的影响,其他条件相同时,将1molH2(g)和1molI2(g)充入体积为2L的恒容密闭容器中,测得HI(g)的物质的量分数随时间变化的实验数据如表:| 时间/min | 0 | 20 | 40 | 60 | 80 | 100 | |
| HI(g)的物质的量分数 |  | 0 | 0.50 | 0.68 | 0.76 | 0.80 | 0.80 |
 | 0 | 0.60 | 0.72 | 0.75 | 0.75 | 0.75 | |
A. 温度下,该反应可能在70min时已达到平衡状态 温度下,该反应可能在70min时已达到平衡状态 |
B. 温度下,0~20min内用H2表示的平均反应速率为0.15mol•L-1•min-1 温度下,0~20min内用H2表示的平均反应速率为0.15mol•L-1•min-1 |
C.由表中数据推测,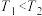 |
| D.由表中数据可知,温度越高,该化学反应的限度越大 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】在容积不变的某2L密闭容器中,充入H2和N2各5mol的混合气体,在一定条件下,5min后反应达到平衡,此时容器内压强是反应前的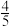 .则下列说法正确的是
.则下列说法正确的是
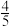 .则下列说法正确的是
.则下列说法正确的是| A.从反应开始到平衡时,用H2表示平均反应速率为0.15mol/(L·min) |
| B.反应达到平衡时,NH3的物质的量浓度是0.5mol/L |
| C.反应达到平衡时,N2和H2的物质的量之比为1∶3 |
| D.5min内H2与N2的反应速率之比为3∶1 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐3】T℃时,在2L密闭容器中使X(g)与Y(g)发生反应生成Z(g)。反应过程中X、Y、Z的物质的量的变化如图1所示;若保持其他条件不变,温度分别为T1和T2时,Z的百分含量与时间的关系如图2所示,则下列结论正确的是


A.容器中发生的反应可表示为3X(g)+Y(g) 2Z(g) 2Z(g) |
| B.反应进行的前3min内,用X表示的反应速率v(X)=0.2 mol·L-1·min-1 |
| C.若改变反应条件,使反应进程如图3所示,则改变的条件是增大压强 |
| D.保持其他条件不变,升高温度,反应的化学平衡常数K增大 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】研究催化剂对 反应速率的影响。恒温、恒容时,
反应速率的影响。恒温、恒容时,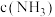 随时间的变化如下。
随时间的变化如下。
下列说法不正确 的是
 反应速率的影响。恒温、恒容时,
反应速率的影响。恒温、恒容时,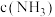 随时间的变化如下。
随时间的变化如下。 | 0 | 20 | 40 | 60 | 80 |
| 催化剂Ⅰ | 2.40 | 2.00 | 1.60 | 1.20 | 0.80 |
| 催化剂Ⅱ | 2.40 | 1.60 | 0.80 | 0.40 | 0.40 |
A.使用催化剂Ⅰ,0~20min的平均反应速率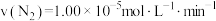 |
B.使用催化剂Ⅱ,达平衡后容器内的压强是初始时的 倍 倍 |
| C.相同条件下,使用催化剂Ⅱ可使该反应的活化能降低更多,反应更快 |
| D.相同条件下,使用催化剂Ⅱ可使该反应的化学平衡常数更大 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】向体积为10L的恒容密闭容器中通入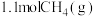 和
和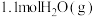 制备
制备 ,反应原理为
,反应原理为
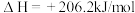 。在不同温度(
。在不同温度(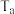 、
、 )下测得容器中
)下测得容器中 随时间的变化曲线如图所示。
随时间的变化曲线如图所示。
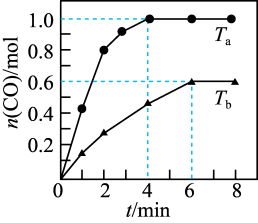
下列说法正确的是
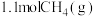 和
和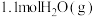 制备
制备 ,反应原理为
,反应原理为
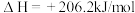 。在不同温度(
。在不同温度(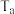 、
、 )下测得容器中
)下测得容器中 随时间的变化曲线如图所示。
随时间的变化曲线如图所示。
下列说法正确的是
A.温度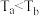 |
B.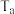 时, 时, 的平衡转化率 的平衡转化率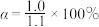 |
C. 时,平衡后再充入 时,平衡后再充入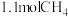 ,平衡常数增大 ,平衡常数增大 |
D. 时,若改为恒温恒压容器,平衡时 时,若改为恒温恒压容器,平衡时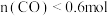 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐3】在恒温恒压下,某一体积可变的密闭容器中发生反应A(g)+B(g) C(g) ΔH<0,t1时达到平衡后,在t2时改变某一条件,其反应过程如图所示。下列说法正确的是
C(g) ΔH<0,t1时达到平衡后,在t2时改变某一条件,其反应过程如图所示。下列说法正确的是

 C(g) ΔH<0,t1时达到平衡后,在t2时改变某一条件,其反应过程如图所示。下列说法正确的是
C(g) ΔH<0,t1时达到平衡后,在t2时改变某一条件,其反应过程如图所示。下列说法正确的是
| A.I、II两过程达到平衡时,A的体积分数:I>II |
| B.t2时改变的条件是向密闭容器中加入物质C |
| C.0~t2时,v正>v逆 |
| D.I、II两过程达到平衡时,平衡常数:K(I)<K(II) |
您最近一年使用:0次



