完成下列问题。
Ⅰ.单质、氧化物、酸、碱、盐,这些不同类别的物质之间反应时可以生成盐,某同学构建了如图所示的知识网络图。
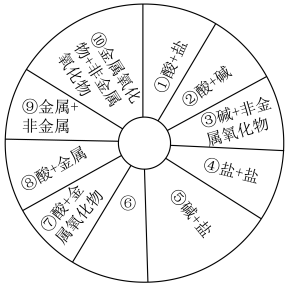
(1)请写一种符合图中组合⑥关系的化学方程式(要求组合⑥不能与图中已有组合重复,为四大基本反应类型)___________ 。
(2) 可看成由
可看成由 和FeO组成,请写出
和FeO组成,请写出 与盐酸反应的离子方程式:
与盐酸反应的离子方程式:___________ 。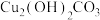 可看成由
可看成由 和
和 组成,请写出
组成,请写出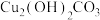 与盐酸反应的化学方程式:
与盐酸反应的化学方程式:___________ 。
(3)一种阳离子与多种酸根离子构成的盐称为“混盐”,如氯化硝酸钙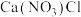 ;而“复盐”则是指含有多种简单阳离子和一种酸根阴离子的盐,如
;而“复盐”则是指含有多种简单阳离子和一种酸根阴离子的盐,如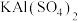 ,据此下列各化合物中属于混盐的是
,据此下列各化合物中属于混盐的是___________ (填序号,下同),属于复盐的是___________ 。
A. B.
B.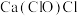
C. D.
D.
Ⅱ.铁是人类较早使用的金属之一,回答下列问题。
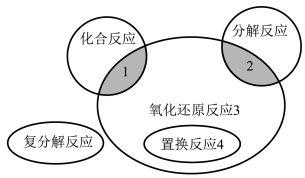
(4)氧化还原反应与四大基本反应类型的关系如图所示,请写出一个属于区域3的有铁单质生成的化学方程式:___________ 。
(5)已知氧化性: ,若向
,若向 和
和 的混合溶液中加入一定量铁粉,最终有固体剩余,则下列说法中正确的是___________。
的混合溶液中加入一定量铁粉,最终有固体剩余,则下列说法中正确的是___________。
(6)水热法制备直径为1-100nm的颗粒Y(化合物),反应原理为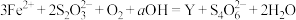 ,下列说法中正确的___________。
,下列说法中正确的___________。
(7) 主要用于饮用水消毒净化、城市生活污水和工业污水处理。湿法制备高铁酸钾(
主要用于饮用水消毒净化、城市生活污水和工业污水处理。湿法制备高铁酸钾( )是在碱性环境中进行,反应体系中有六种反应微粒:
)是在碱性环境中进行,反应体系中有六种反应微粒: 、
、 、
、 、
、 、
、 、
、 。请依据上述信息,写出并配平湿法制高铁酸钾的离子方程式:
。请依据上述信息,写出并配平湿法制高铁酸钾的离子方程式:___________ 。
Ⅰ.单质、氧化物、酸、碱、盐,这些不同类别的物质之间反应时可以生成盐,某同学构建了如图所示的知识网络图。

(1)请写一种符合图中组合⑥关系的化学方程式(要求组合⑥不能与图中已有组合重复,为四大基本反应类型)
(2)
 可看成由
可看成由 和FeO组成,请写出
和FeO组成,请写出 与盐酸反应的离子方程式:
与盐酸反应的离子方程式: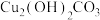 可看成由
可看成由 和
和 组成,请写出
组成,请写出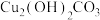 与盐酸反应的化学方程式:
与盐酸反应的化学方程式:(3)一种阳离子与多种酸根离子构成的盐称为“混盐”,如氯化硝酸钙
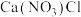 ;而“复盐”则是指含有多种简单阳离子和一种酸根阴离子的盐,如
;而“复盐”则是指含有多种简单阳离子和一种酸根阴离子的盐,如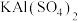 ,据此下列各化合物中属于混盐的是
,据此下列各化合物中属于混盐的是A.
 B.
B.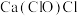
C.
 D.
D.
Ⅱ.铁是人类较早使用的金属之一,回答下列问题。
(4)氧化还原反应与四大基本反应类型的关系如图所示,请写出一个属于区域3的有铁单质生成的化学方程式:

(5)已知氧化性:
 ,若向
,若向 和
和 的混合溶液中加入一定量铁粉,最终有固体剩余,则下列说法中正确的是___________。
的混合溶液中加入一定量铁粉,最终有固体剩余,则下列说法中正确的是___________。| A.固体中一定有铜 | B.固体中一定有铁 |
C.溶液中一定有 | D.溶液中一定有 |
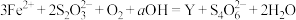 ,下列说法中正确的___________。
,下列说法中正确的___________。A. |
B. 、 、 都发生还原反应 都发生还原反应 |
| C.将Y均匀分散到水中形成的体系具有丁达尔效应 |
D.每有3个 参加反应,反应中转移电子总数目为6个 参加反应,反应中转移电子总数目为6个 |
 主要用于饮用水消毒净化、城市生活污水和工业污水处理。湿法制备高铁酸钾(
主要用于饮用水消毒净化、城市生活污水和工业污水处理。湿法制备高铁酸钾( )是在碱性环境中进行,反应体系中有六种反应微粒:
)是在碱性环境中进行,反应体系中有六种反应微粒: 、
、 、
、 、
、 、
、 、
、 。请依据上述信息,写出并配平湿法制高铁酸钾的离子方程式:
。请依据上述信息,写出并配平湿法制高铁酸钾的离子方程式:
更新时间:2023-10-12 15:08:57
|
相似题推荐
填空题
|
适中
(0.65)
【推荐1】2022年1月,南太平洋岛国汤加境内发生了“21世纪至今最剧烈的火山喷发”,对该国造成了严重的破坏。火山喷发过程部分化学反应如下:
①
②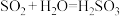
③
(1)在上述方程式涉及的物质中,能与盐酸反应的氧化物有_______ (填化学式),属于酸的有_______ (填化学式)。
(2) 与
与 具有某些相似的化学性质,写出用NaOH溶液吸收
具有某些相似的化学性质,写出用NaOH溶液吸收 的化学方程式:
的化学方程式:_______ 。
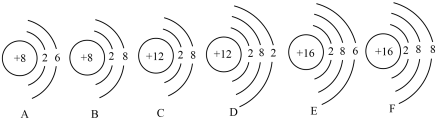
(3)下列粒子结构示意图中,表示S的是_______ (填字母),表示 的是
的是_______ (填字母)。
(4) 是火山爆发过程中产生的酸性气体,属于二元弱酸,其饱和溶液的pH约为4。
是火山爆发过程中产生的酸性气体,属于二元弱酸,其饱和溶液的pH约为4。
①一个 分子中含有
分子中含有_______ 个原子,其中H元素与S元素的质量比为_______ 。
②将 气体通入石蕊试液中,试液由紫色变为
气体通入石蕊试液中,试液由紫色变为_______ 色。
③ 称为正盐,
称为正盐, 称为酸式盐,写出
称为酸式盐,写出 的一种酸式盐的化学式:
的一种酸式盐的化学式:_______ 。
①

②
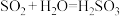
③

(1)在上述方程式涉及的物质中,能与盐酸反应的氧化物有
(2)
 与
与 具有某些相似的化学性质,写出用NaOH溶液吸收
具有某些相似的化学性质,写出用NaOH溶液吸收 的化学方程式:
的化学方程式:(3)下列粒子结构示意图中,表示S的是
 的是
的是
(4)
 是火山爆发过程中产生的酸性气体,属于二元弱酸,其饱和溶液的pH约为4。
是火山爆发过程中产生的酸性气体,属于二元弱酸,其饱和溶液的pH约为4。①一个
 分子中含有
分子中含有②将
 气体通入石蕊试液中,试液由紫色变为
气体通入石蕊试液中,试液由紫色变为③
 称为正盐,
称为正盐, 称为酸式盐,写出
称为酸式盐,写出 的一种酸式盐的化学式:
的一种酸式盐的化学式:
您最近半年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】根据物质的组成、结构、性质进行分类,可预测物质的性质及变化
(1) 是普通玻璃的主要成分,与
是普通玻璃的主要成分,与 一样是酸性氧化物,写出
一样是酸性氧化物,写出 溶于KOH溶液的化学反应方程式
溶于KOH溶液的化学反应方程式_______ 。
(2)物质与水发生的复分解反应称为水解反应。例如: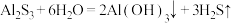 。根据上述观点,写出
。根据上述观点,写出 水解产物的化学式为
水解产物的化学式为_______ 和_______ 。
(3) 固体(黑色)可以写成
固体(黑色)可以写成 ,属于
,属于_______ (填“混合物”或“纯净物”)。将其加入适量盐酸,所发生反应的化学方程式为_______ 。
(4)亚磷酸 分子中虽有三个H原子,已知它与氢氧化钠反只能生成两种盐,请问它属于
分子中虽有三个H原子,已知它与氢氧化钠反只能生成两种盐,请问它属于_______ 元酸,生成的两种盐的化学式为_______ 、_______ 。
(1)
 是普通玻璃的主要成分,与
是普通玻璃的主要成分,与 一样是酸性氧化物,写出
一样是酸性氧化物,写出 溶于KOH溶液的化学反应方程式
溶于KOH溶液的化学反应方程式(2)物质与水发生的复分解反应称为水解反应。例如:
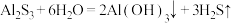 。根据上述观点,写出
。根据上述观点,写出 水解产物的化学式为
水解产物的化学式为(3)
 固体(黑色)可以写成
固体(黑色)可以写成 ,属于
,属于(4)亚磷酸
 分子中虽有三个H原子,已知它与氢氧化钠反只能生成两种盐,请问它属于
分子中虽有三个H原子,已知它与氢氧化钠反只能生成两种盐,请问它属于
您最近半年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】回答下列问题
(1)现有下列物质:①SO2 ②石墨 ③氨水 ④液氯 ⑤H2SO4 ⑥盐酸 ⑦漂白粉 ⑧含氧40%的氧化镁 ⑨CuSO4·5H2O ⑩熔融NaCl
其中属于纯净物的是___________ (填序号,下同);属于电解质的是___________ ;属于非电解质的是___________ ,能导电的是___________ 。
(2)已知Be(OH)2与Al(OH)3都属于两性氢氧化物,写出Be(OH)2分别与NaOH溶液、盐酸反应的化学方程式:___________ 、___________ 。
(1)现有下列物质:①SO2 ②石墨 ③氨水 ④液氯 ⑤H2SO4 ⑥盐酸 ⑦漂白粉 ⑧含氧40%的氧化镁 ⑨CuSO4·5H2O ⑩熔融NaCl
其中属于纯净物的是
(2)已知Be(OH)2与Al(OH)3都属于两性氢氧化物,写出Be(OH)2分别与NaOH溶液、盐酸反应的化学方程式:
您最近半年使用:0次
填空题
|
适中
(0.65)
【推荐2】氢化铝锂(LiAlH4)、硼氢化钠(NaBH4)在有机合成中应用广泛。回答下列问题:
(1)工业上制备氢化铝锂方法是:首先高温高压合成氢化铝钠,然后与氯化锂反应,相关化学方程式为Na+Al+2H2 NaAlH4;NaAlH4+LiCl
NaAlH4;NaAlH4+LiCl LiAlH4+NaCl。上述反应涉及的基本反应类型分别为
LiAlH4+NaCl。上述反应涉及的基本反应类型分别为_______ 、_______ 。
(2)NaBH4的电子式为_______ ,其与水反应生成NaBO2,该反应的化学方程式为_______ 。
(3)还原能力(单位质量转移电子数):LiAlH4_______ (填“>”“=”或“<")NaBH4。
(4)工业上湿法合成NaBH4路线如下:

①"合成”步骤中常将NaH分散到矿物油中再与硼酸三甲酯[化学式:B(OCH3)3,易溶于矿物油中]反应,其目的是_______ 。
②“合成”反应的化学方程式为_______ 。
(1)工业上制备氢化铝锂方法是:首先高温高压合成氢化铝钠,然后与氯化锂反应,相关化学方程式为Na+Al+2H2
 NaAlH4;NaAlH4+LiCl
NaAlH4;NaAlH4+LiCl LiAlH4+NaCl。上述反应涉及的基本反应类型分别为
LiAlH4+NaCl。上述反应涉及的基本反应类型分别为(2)NaBH4的电子式为
(3)还原能力(单位质量转移电子数):LiAlH4
(4)工业上湿法合成NaBH4路线如下:

①"合成”步骤中常将NaH分散到矿物油中再与硼酸三甲酯[化学式:B(OCH3)3,易溶于矿物油中]反应,其目的是
②“合成”反应的化学方程式为
您最近半年使用:0次
填空题
|
适中
(0.65)
【推荐3】实验室制取氯气的反应原理为: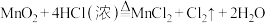 ,据此回答下列问题:
,据此回答下列问题:
(1)氧化剂与还原剂的个数之比_______ 。
(2)实验室制取氯气时,下列装置能达到相应实验目的的是_______ 。
(3)有一种“地康法”制取氯气的反应原理如下图所示:
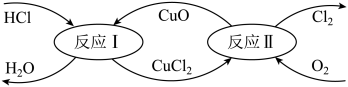
①写出反应Ⅰ的化学方程式_______ 。
②反应Ⅱ属于_______ 反应(填基本反应类型)。
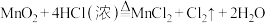 ,据此回答下列问题:
,据此回答下列问题:(1)氧化剂与还原剂的个数之比
(2)实验室制取氯气时,下列装置能达到相应实验目的的是
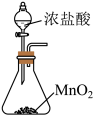 | 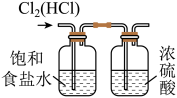 |  | 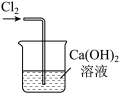 |
A.制备 | B.除去 中的HCl 中的HCl | C.收集 | D.尾气处理 |
(3)有一种“地康法”制取氯气的反应原理如下图所示:

①写出反应Ⅰ的化学方程式
②反应Ⅱ属于
您最近半年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】回答下列问题
(1)已知亚磷酸(H3PO3)为二元弱酸,则(Na2HPO3)溶液中,各离子浓度的大小关系为___________
(2)常温下,将NaOH溶液滴加到亚磷酸(H3PO3)溶液中,混合溶液的pH与离子浓度变化的关系如图所示,则表示 的是曲线
的是曲线___________ (填“Ⅰ”或“Ⅱ”),亚磷酸(H3PO3)的Ka1=___________

(3)常温时,0.1 mol/LNH4Al(SO4)2溶液的pH=3。
①
___________ mol/L。
②80℃时, 溶液的pH小于3,请从平衡移动的角度分析导致pH随温度变化的原因是
溶液的pH小于3,请从平衡移动的角度分析导致pH随温度变化的原因是___________ 。
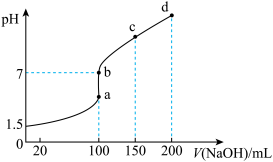
(4)常温时,向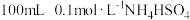 溶液中滴加
溶液中滴加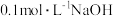 溶液,得到的溶液pH与NaOH溶液体积的关系曲线如图所示。
溶液,得到的溶液pH与NaOH溶液体积的关系曲线如图所示。
①向 溶液中滴加NaOH溶液到a点的过程中,发生反应的离子方程式为
溶液中滴加NaOH溶液到a点的过程中,发生反应的离子方程式为___________ 。
②图中a、b、c、d点中水的电离程度最小的是___________ 。
(1)已知亚磷酸(H3PO3)为二元弱酸,则(Na2HPO3)溶液中,各离子浓度的大小关系为
(2)常温下,将NaOH溶液滴加到亚磷酸(H3PO3)溶液中,混合溶液的pH与离子浓度变化的关系如图所示,则表示
 的是曲线
的是曲线
(3)常温时,0.1 mol/LNH4Al(SO4)2溶液的pH=3。
①

②80℃时,
 溶液的pH小于3,请从平衡移动的角度分析导致pH随温度变化的原因是
溶液的pH小于3,请从平衡移动的角度分析导致pH随温度变化的原因是(4)常温时,向
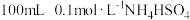 溶液中滴加
溶液中滴加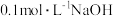 溶液,得到的溶液pH与NaOH溶液体积的关系曲线如图所示。
溶液,得到的溶液pH与NaOH溶液体积的关系曲线如图所示。①向
 溶液中滴加NaOH溶液到a点的过程中,发生反应的离子方程式为
溶液中滴加NaOH溶液到a点的过程中,发生反应的离子方程式为②图中a、b、c、d点中水的电离程度最小的是

您最近半年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】现有以下物质:①NaOH溶液;②液氨;③BaCO3固体;④熔融KHSO4;⑤Fe(OH)3胶体;⑥铜;⑦CO2;⑧CH3COOH;⑨蔗糖;⑩矿泉水请回答下列问题:
(1)以上物质中属于混合物的是_______ (填序号),以上物质中属于电解质的是_______ (填序号);以上纯净物中能导电的是_______ (填序号)。
(2)在小烧杯中加入20 mL蒸馏水,加热至沸腾后,向沸水中滴入几滴饱和FeCl3溶液,继续煮沸至溶液呈红褐色,即制得Fe(OH)3胶体。证明制备出Fe(OH)3胶体的操作方法是_______
(3)写出④在水溶液中的电离方程式_______ 。
(4)在①溶液中缓缓通入过量的CO2可生成酸式盐,写出反应的离子方程式_______ 。
(1)以上物质中属于混合物的是
(2)在小烧杯中加入20 mL蒸馏水,加热至沸腾后,向沸水中滴入几滴饱和FeCl3溶液,继续煮沸至溶液呈红褐色,即制得Fe(OH)3胶体。证明制备出Fe(OH)3胶体的操作方法是
(3)写出④在水溶液中的电离方程式
(4)在①溶液中缓缓通入过量的CO2可生成酸式盐,写出反应的离子方程式
您最近半年使用:0次
填空题
|
适中
(0.65)
真题
【推荐1】Ⅰ.请回答:
(1)H2O2的电子式___________ 。
(2)镁燃烧不能用CO2灭火,用化学方程式表示其理由___________ 。
(3)在AgCl沉淀中加入KBr溶液,白色沉淀转化为淡黄色沉淀,写出反应的离子方程式___________ 。
(4)完成以下氧化还原反应的离子方程式:___________
( ) +( )C2O
+( )C2O +___________=( )Mn2++( )CO2↑+___________
+___________=( )Mn2++( )CO2↑+___________
Ⅱ.化合物甲和NaAlH4都是重要的还原剂。一定条件下金属钠和H2反应生成甲。甲与水反应可产生H2,甲与AlCl3反应可得到NaAlH4.将4.80g甲加热至完全分解,得到金属钠和2.24 L(已折算成标准状况)的H2。
请推测并回答:
(5)甲的化学式___________ 。
(6)甲与AlCl3反应得到NaAlH4的化学方程式___________ 。
(7)NaAlH4与水发生氧化还原反应的化学方程式___________ 。
(8)甲在无水条件下可作为某些钢铁制品的脱锈剂(铁锈的成分表示为Fe2O3),脱锈过程发生反应的化学方程式___________ 。
(9)某同学认为:用惰性气体赶尽反应体系中的空气,将铁和盐酸反应后的气体经浓硫酸干燥,再与金属钠反应,得到固体物质即为纯净的甲;取该固体物质与水反应,若能产生H2,即可证明得到的甲一定是纯净的。判断该同学设想的制备和验纯方法的合理性并说明理由___________ 。
(1)H2O2的电子式
(2)镁燃烧不能用CO2灭火,用化学方程式表示其理由
(3)在AgCl沉淀中加入KBr溶液,白色沉淀转化为淡黄色沉淀,写出反应的离子方程式
(4)完成以下氧化还原反应的离子方程式:
( )
 +( )C2O
+( )C2O +___________=( )Mn2++( )CO2↑+___________
+___________=( )Mn2++( )CO2↑+___________Ⅱ.化合物甲和NaAlH4都是重要的还原剂。一定条件下金属钠和H2反应生成甲。甲与水反应可产生H2,甲与AlCl3反应可得到NaAlH4.将4.80g甲加热至完全分解,得到金属钠和2.24 L(已折算成标准状况)的H2。
请推测并回答:
(5)甲的化学式
(6)甲与AlCl3反应得到NaAlH4的化学方程式
(7)NaAlH4与水发生氧化还原反应的化学方程式
(8)甲在无水条件下可作为某些钢铁制品的脱锈剂(铁锈的成分表示为Fe2O3),脱锈过程发生反应的化学方程式
(9)某同学认为:用惰性气体赶尽反应体系中的空气,将铁和盐酸反应后的气体经浓硫酸干燥,再与金属钠反应,得到固体物质即为纯净的甲;取该固体物质与水反应,若能产生H2,即可证明得到的甲一定是纯净的。判断该同学设想的制备和验纯方法的合理性并说明理由
您最近半年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】完成下列问题。
(1)将下列化学方程式配平___________ 。
_______KI+_______H2SO4=_______I2+______H2S+______KHSO4+______H2O
(2)反应8NH3+3Cl2=6NH4Cl+N2中氧化剂与还原剂的质量之比为___________ 。
(3)已知:酸性环境中,Fe2+被 氧化,生成Fe3+和NO气体,请写出对应的离子方程式:
氧化,生成Fe3+和NO气体,请写出对应的离子方程式:_______ ;
(4)R2O 离子在一定条件下可以把Mn2+离子氧化为
离子在一定条件下可以把Mn2+离子氧化为 若反应后R2O
若反应后R2O 离子变为RO
离子变为RO 离子,又知反应中氧化剂和还原剂的个数之比为5:2,则n值为
离子,又知反应中氧化剂和还原剂的个数之比为5:2,则n值为___________ ,R2O 中R的化合价是
中R的化合价是___________ 价。
(5)根据反应14CuSO4+5FeS2+12H2O=7Cu2S+5FeSO4+12H2SO4,可知当有300gFeS2参加反应时,被氧化的硫元素的质量为___________ g。
(1)将下列化学方程式配平
_______KI+_______H2SO4=_______I2+______H2S+______KHSO4+______H2O
(2)反应8NH3+3Cl2=6NH4Cl+N2中氧化剂与还原剂的质量之比为
(3)已知:酸性环境中,Fe2+被
 氧化,生成Fe3+和NO气体,请写出对应的离子方程式:
氧化,生成Fe3+和NO气体,请写出对应的离子方程式:(4)R2O
 离子在一定条件下可以把Mn2+离子氧化为
离子在一定条件下可以把Mn2+离子氧化为 若反应后R2O
若反应后R2O 离子变为RO
离子变为RO 离子,又知反应中氧化剂和还原剂的个数之比为5:2,则n值为
离子,又知反应中氧化剂和还原剂的个数之比为5:2,则n值为 中R的化合价是
中R的化合价是(5)根据反应14CuSO4+5FeS2+12H2O=7Cu2S+5FeSO4+12H2SO4,可知当有300gFeS2参加反应时,被氧化的硫元素的质量为
您最近半年使用:0次
填空题
|
适中
(0.65)
【推荐3】碳形成的化合物种类繁多,硅是构成地壳岩石的主要元素。碳在自然界有两种稳定的同位素,有关数据如下表:
请列出碳元素近似相对原子质量的计算式_____________________________________ 。
(1)Si原子的14个电子排布在_______ 个能级上;与硅元素同周期、其原子核外有2个未成对电子的元素的最外层电子排布式为_____________ 。
(2)SiO2用途广泛,以下叙述错误的是______________ 。
a.SiO2是二氧化硅的分子式 b.SiO2中1个Si原子结合4个O原子
c.SiO2是酸性氧化物 d.SiO2熔沸点较高,属于原子晶体
(3)通常状况下,SiF4呈气态。以下叙述正确的是___________ 。
a.Si原子难以形成Si4+ b.SiF4是有极性键的非极性分子
c.固态SiF4是原子晶体 d.相同压强时,SiF4的沸点高于SiCl4
(4)Fe3O4可以写成FeO•Fe2O3,也可写成盐的形式:Fe[Fe2O4]。Pb3O4中含+2价的Pb和+4价的Pb,请将Pb3O4写成两种氧化物的形式___________ ,写成盐的形式__________ 。
(5)Pb的+2价化合物稳定,+4价的Pb能氧化浓盐酸生成Cl2。写出Pb3O4与盐酸反应的化学方程式____________________________________________ 。
| 同位素 | 相对原子质量 | 丰度(原子分数) |
| 12C | 12(整数,相对原子质量的基准) | 0.9893 |
| 13C | 13.003354826 | 0.0107 |
请列出碳元素近似相对原子质量的计算式
(1)Si原子的14个电子排布在
(2)SiO2用途广泛,以下叙述错误的是
a.SiO2是二氧化硅的分子式 b.SiO2中1个Si原子结合4个O原子
c.SiO2是酸性氧化物 d.SiO2熔沸点较高,属于原子晶体
(3)通常状况下,SiF4呈气态。以下叙述正确的是
a.Si原子难以形成Si4+ b.SiF4是有极性键的非极性分子
c.固态SiF4是原子晶体 d.相同压强时,SiF4的沸点高于SiCl4
(4)Fe3O4可以写成FeO•Fe2O3,也可写成盐的形式:Fe[Fe2O4]。Pb3O4中含+2价的Pb和+4价的Pb,请将Pb3O4写成两种氧化物的形式
(5)Pb的+2价化合物稳定,+4价的Pb能氧化浓盐酸生成Cl2。写出Pb3O4与盐酸反应的化学方程式
您最近半年使用:0次