盖斯定律是化学热力学发展的基础,下列不能应用盖斯定律解决的问题是
| A.比较Al与Fe燃烧热的大小 |
| B.比较CH3OH与CH4燃烧热大小 |
| C.比较S(s)与S(g)在空气中燃烧的热效应大小 |
| D.比较氢氧化钠分别与盐酸和氢氟酸中和反应的热效应大小 |
更新时间:2023-10-12 15:22:13
|
相似题推荐
单选题
|
较难
(0.4)
名校
解题方法
【推荐1】 教授研究了铑
教授研究了铑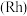 配合物催化醛酮氢化反应,提出的反应机理如图所示,1、2、3、4四种反应的反应热分别为
配合物催化醛酮氢化反应,提出的反应机理如图所示,1、2、3、4四种反应的反应热分别为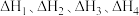 ,下列说法错误的是
,下列说法错误的是
 教授研究了铑
教授研究了铑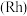 配合物催化醛酮氢化反应,提出的反应机理如图所示,1、2、3、4四种反应的反应热分别为
配合物催化醛酮氢化反应,提出的反应机理如图所示,1、2、3、4四种反应的反应热分别为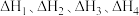 ,下列说法错误的是
,下列说法错误的是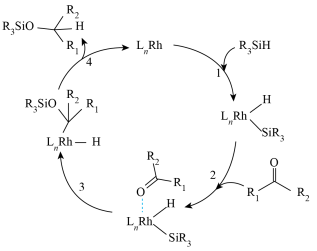
A.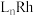 在氢化反应中作催化剂 在氢化反应中作催化剂 |
B.该机理的总反应的反应热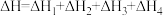 |
| C.若步骤②为决速步骤,则其活化能最大 |
D.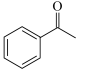 与 与 发生上述反应可生成 发生上述反应可生成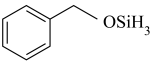 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
【推荐2】下列图示与对应的叙述不相符合 的是
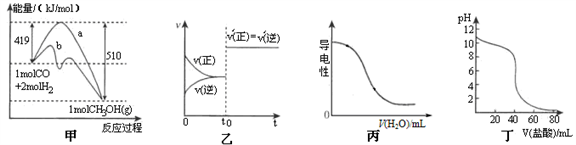
A.图甲表示工业上用CO生产甲醇的反应CO(g)+2H2(g) CH3OH(g)。该反应的△H=-91.kJ·mol-1 CH3OH(g)。该反应的△H=-91.kJ·mol-1 |
| B.图乙表示已达平衡的某反应,在t0时改变某一条件后反应速率随时间变化,则改变的条件可能是加入催化剂 |
| C.图丙表示向0.1 mol·L–1的氨水溶液中逐渐加水时溶液的导电性变化 |
| D.图丁表示盐酸滴加到0.1mol·L-1某碱溶液得到的滴定曲线,用已知浓度盐酸滴定未知浓度该碱时最好选取酚酞作指示剂 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
【推荐3】在恒温条件下,向盛有足量NaCl(s)的2L恒容密闭容器中加入0.2molNO2、0.2molNO和0.1molCl2,发生如下两个反应:
①2NO2(g)+NaCl(s) NaNO3(s)+ClNO(g) △H1<0 K1
NaNO3(s)+ClNO(g) △H1<0 K1
②2NO(g)+Cl2(g) 2ClNO(g) △H2<0 K2
2ClNO(g) △H2<0 K2
10分钟时反应达到平衡,测得体系的压强减少20%,10分钟内用ClNO(g)表示的平均反应速率v(ClNO)=7.5×10-3mol·L-1·min-1。下列说法正确的是
①2NO2(g)+NaCl(s)
 NaNO3(s)+ClNO(g) △H1<0 K1
NaNO3(s)+ClNO(g) △H1<0 K1②2NO(g)+Cl2(g)
 2ClNO(g) △H2<0 K2
2ClNO(g) △H2<0 K210分钟时反应达到平衡,测得体系的压强减少20%,10分钟内用ClNO(g)表示的平均反应速率v(ClNO)=7.5×10-3mol·L-1·min-1。下列说法正确的是
| A.平衡后c(NO)=2.5×10-2mol·L-1 |
| B.平衡时NO2的转化率为50% |
| C.其它条件保持不变,反应在绝热条件下进行,则平衡常数K2增大 |
D.反应4NO2(g)+2NaCl(s)  2NaNO3(s)+2NO(g)+Cl2(g)的平衡常数为 2NaNO3(s)+2NO(g)+Cl2(g)的平衡常数为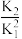 |
您最近一年使用:0次



