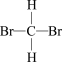
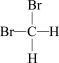
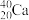现有7个化学符号:①18O;②2H;③32S8;④23Na;⑤14N;⑥16O;⑦1H2;⑧12C60;⑨32S2
(1)互为同位素的是_______ ;互为同素异形体的是_______ 。
(2)写出NaOH的电子式_______ ;NH3的结构式 _______ 。
(3)请用电子式表示NaCl 的形成过程:_______ 。
(4)现有以下物质:①H2;②Na2O2;③NaOH;④H2O2;⑤CaCl2;⑥NH4NO3;⑦H2S。其中既有离子键,又有非极性共价键构成的物质是_______ (填序号,下同),属于共价化合物的是_______ 。
(1)互为同位素的是
(2)写出NaOH的电子式
(3)请用电子式表示NaCl 的形成过程:
(4)现有以下物质:①H2;②Na2O2;③NaOH;④H2O2;⑤CaCl2;⑥NH4NO3;⑦H2S。其中既有离子键,又有非极性共价键构成的物质是
22-23高一下·重庆长寿·期中 查看更多[2]
更新时间:2023-09-16 13:18:51
|
相似题推荐
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】请回答下列问题:
(1)漂粉精的主要成分的化学式___________ ;
(2)NaCN各原子均满足8电子稳定结构。写出NaCN的电子式___________ ;
(3)用一个化学方程式说明Fe3+与Cl-和SCN-两种微粒结合能力的强弱___________ 。
(1)漂粉精的主要成分的化学式
(2)NaCN各原子均满足8电子稳定结构。写出NaCN的电子式
(3)用一个化学方程式说明Fe3+与Cl-和SCN-两种微粒结合能力的强弱
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】人体必需的一些元素在周期表中的分布情况如下:______ 。 是一种绿色氧化剂,电子式为
是一种绿色氧化剂,电子式为________ 。
(2)钠离子和氯离子可以帮助我们维持机体的电解质平衡。常温下,将 通入水中,可以得到一种具有漂白性的分子,写出它的结构式
通入水中,可以得到一种具有漂白性的分子,写出它的结构式________ 。
(3)硒(Se)具有抗氧化、增强人体抵抗力的功效。Se在元素周期表中的位置是________ ,原子序数为____ 。
(4)铁、铬、锰在人体内含量微乎其微,但对维持内分泌平衡和身体基础代谢有重要作用。向少量酸性 溶液中加入
溶液中加入 溶液,发生反应的离子方程式为
溶液,发生反应的离子方程式为___________ 。
(5)前四周期同族元素的某种性质X随核电荷数的变化趋势如图所示,则下列说法正确的是_______(填字母)。

 是一种绿色氧化剂,电子式为
是一种绿色氧化剂,电子式为(2)钠离子和氯离子可以帮助我们维持机体的电解质平衡。常温下,将
 通入水中,可以得到一种具有漂白性的分子,写出它的结构式
通入水中,可以得到一种具有漂白性的分子,写出它的结构式(3)硒(Se)具有抗氧化、增强人体抵抗力的功效。Se在元素周期表中的位置是
(4)铁、铬、锰在人体内含量微乎其微,但对维持内分泌平衡和身体基础代谢有重要作用。向少量酸性
 溶液中加入
溶液中加入 溶液,发生反应的离子方程式为
溶液,发生反应的离子方程式为(5)前四周期同族元素的某种性质X随核电荷数的变化趋势如图所示,则下列说法正确的是_______(填字母)。
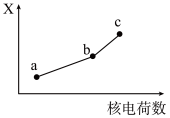
| A.若a、b、c表示氧族元素,则X表示对应氢化物的沸点 |
| B.若a、b、c表示卤族元素,则X表示对应简单离子的还原性 |
| C.若a、b、c表示第ⅠA族元素,则X表示对应离子的氧化性 |
| D.若a、b、c表示第ⅡA族元素,则X表示最高价氧化物对应水化物的碱性 |
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】离子型金属氢化物LiH、NaH、LiAlH4、NaBH4等,具有强还原性,也可作生氢剂。
(1)Na核外不同能量的电子数之比为:_____ (按能量由低至高的顺序)。
(2)将Li+、H-、H+、O2-按半径由小到大的排列顺序为_____ 。
(3)1个BH 中含
中含_____ 电子,补写一个与BH 电子数相同且带一个单位负电荷的离子的电子式:
电子数相同且带一个单位负电荷的离子的电子式: 、
、_____ 。
(4)两种硼化物的熔点如表所示:
两物质熔点差异的原因是_____ 。
(1)Na核外不同能量的电子数之比为:
(2)将Li+、H-、H+、O2-按半径由小到大的排列顺序为
(3)1个BH
 中含
中含 电子数相同且带一个单位负电荷的离子的电子式:
电子数相同且带一个单位负电荷的离子的电子式: 、
、(4)两种硼化物的熔点如表所示:
| 硼氢化物 | NaBH4 | Al(BH4)3 |
| 熔点/℃ | 400 | -64.5 |
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】请按要求填空:
(1)简单原子的原子结构可用下图形象地表示:
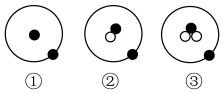
其中“●”表示质子或电子,“〇”表示中子,则下列有关①②③的叙述正确的是_______(填字母,下同)。
(2)科学家已发现一种新型氢分子 ,则相同条件下,等质量的
,则相同条件下,等质量的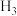 和
和 相同的是_______。
相同的是_______。
(3)与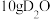 含有相同电子数的
含有相同电子数的 在标准状况下的体积是
在标准状况下的体积是_______ 。
(4)已知: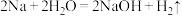 ,将
,将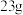 钠与过量的重水
钠与过量的重水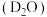 反应,产生气体的质量是
反应,产生气体的质量是_______ 。
(1)简单原子的原子结构可用下图形象地表示:

其中“●”表示质子或电子,“〇”表示中子,则下列有关①②③的叙述正确的是_______(填字母,下同)。
| A.①②③是三种不同的核素 | B.①②③具有相同的质量数 |
| C.①②③互为同位素 | D.①②③核外电子数不同 |
 ,则相同条件下,等质量的
,则相同条件下,等质量的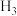 和
和 相同的是_______。
相同的是_______。| A.分子数 | B.原子数 | C.体积 | D.电子数 |
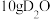 含有相同电子数的
含有相同电子数的 在标准状况下的体积是
在标准状况下的体积是(4)已知:
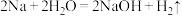 ,将
,将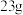 钠与过量的重水
钠与过量的重水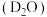 反应,产生气体的质量是
反应,产生气体的质量是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】将下列物质进行分类:(填编号)
A.O2和O3 B.CH2=CH-CH3和CH2=CH-CH2-CH3 C.液氯和氯气 D.淀粉和纤维素 E.葡萄糖和果糖 F. C和
C和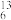 C G.C2H5OH和CH3OCH3 H.
C G.C2H5OH和CH3OCH3 H. 和
和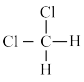 I.CH3CH2CH2CH3和
I.CH3CH2CH2CH3和 J.
J.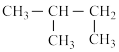 和
和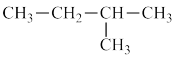
(1)互为同位素的是____ 。
(2)互为同素异形体的是____ 。
(3)互为同分异构体的是____ 。
(4)互为同系物的是____ 。
(5)同一物质是____ 。
A.O2和O3 B.CH2=CH-CH3和CH2=CH-CH2-CH3 C.液氯和氯气 D.淀粉和纤维素 E.葡萄糖和果糖 F.
 C和
C和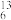 C G.C2H5OH和CH3OCH3 H.
C G.C2H5OH和CH3OCH3 H. 和
和 I.CH3CH2CH2CH3和
I.CH3CH2CH2CH3和 J.
J.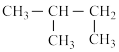 和
和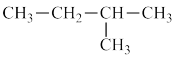
(1)互为同位素的是
(2)互为同素异形体的是
(3)互为同分异构体的是
(4)互为同系物的是
(5)同一物质是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】Ⅰ.现有下列基本粒子:1H、2H、3H、1H+、230Th、232Th、24Na、24Mg、O2、O3、14N、14C,请回答下列问题:
(1)有________ 种不同的核素。互为同素异形体的粒子为______________ 。
(2)碳的同位素12C、13C、14C与氧的同位素16O、17O、18O可化合生成二氧化碳,可得二氧化碳分子的种数为__________ ;可得相对分子质量不同的二氧化碳分子种数为______ 。
Ⅱ.现有下列8种物质:①CaCl2②NH4Cl③K2O2④Ba(OH)2⑤N2⑥HBr⑦MgO⑧CH4。试用以上编号填空:
(1)只有非极性键的是___________________ 。
(2)既有离子键又有极性键的是____________________ 。
(3)属于共价化合物的是__________________ 。
(1)有
(2)碳的同位素12C、13C、14C与氧的同位素16O、17O、18O可化合生成二氧化碳,可得二氧化碳分子的种数为
Ⅱ.现有下列8种物质:①CaCl2②NH4Cl③K2O2④Ba(OH)2⑤N2⑥HBr⑦MgO⑧CH4。试用以上编号填空:
(1)只有非极性键的是
(2)既有离子键又有极性键的是
(3)属于共价化合物的是
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】次磷酸钠(NaH2PO2)广泛应用于化学镀镍,次磷酸钠的生产与镀镍过程如下:
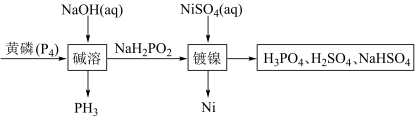
据此回答下列问题:
(1)红磷与黄磷之间的关系为_______ 。
(2)次磷酸钠中磷元素的化合价为_______ 。
(3)写出碱溶过程的化学反应方程式_______ ,该反应中氧化剂与还原剂物质的量之比为_______ 。
(4)已知次磷酸钠中的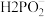 为四面体结构,请写出
为四面体结构,请写出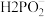 的结构式
的结构式_______ ,次磷酸钠NaH2PO2为_______ (填“酸式盐”、“碱式盐”、“正盐”)。

据此回答下列问题:
(1)红磷与黄磷之间的关系为
(2)次磷酸钠中磷元素的化合价为
(3)写出碱溶过程的化学反应方程式
(4)已知次磷酸钠中的
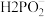 为四面体结构,请写出
为四面体结构,请写出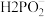 的结构式
的结构式
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】按要求对下列物质进行分类:
① 与
与 ;②
;② 与
与 ;③苯和甲苯;④
;③苯和甲苯;④ 与
与 ⑤
⑤ 与
与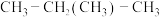 ;⑥
;⑥ 与
与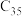 ;⑦金刚石和石墨⑧乙烯和丙烯;⑨乙醇和乙酸;⑩乙醇与甲醚(
;⑦金刚石和石墨⑧乙烯和丙烯;⑨乙醇和乙酸;⑩乙醇与甲醚(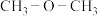 )
)
(1)互为同位素的是_______ (填编号,下同);
(2)互为同分异构体的是_______ 。
(3)互为同种物质的是_______ 。
(4)互为同系物的是_______ 。
(5)互为同素异形体的是_______ 。
①
 与
与 ;②
;② 与
与 ;③苯和甲苯;④
;③苯和甲苯;④ 与
与 ⑤
⑤ 与
与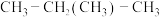 ;⑥
;⑥ 与
与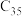 ;⑦金刚石和石墨⑧乙烯和丙烯;⑨乙醇和乙酸;⑩乙醇与甲醚(
;⑦金刚石和石墨⑧乙烯和丙烯;⑨乙醇和乙酸;⑩乙醇与甲醚(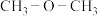 )
)(1)互为同位素的是
(2)互为同分异构体的是
(3)互为同种物质的是
(4)互为同系物的是
(5)互为同素异形体的是
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】回答下列问题
(1)实验数据表明氯化铝在2.02×105Pa时熔点为190℃,且在180℃时即开始升华,由此推测它应该是___________ 化合物(填“离子”或“共价”)。
(2)导电性实验发现熔化的氯化铝不导电,则固态氯化铝是___________ 晶体。
(3)实验测得氯化铝蒸汽的密度折算成标准状况下为11.92g/L,则氯化铝的分子式为___________ ,在氯化铝晶体中,基本微粒间以范德华力结合,微粒内以___________ 相互结合。
(4)通过以上的实验与讨论可以得出的有关结论___________。
(1)实验数据表明氯化铝在2.02×105Pa时熔点为190℃,且在180℃时即开始升华,由此推测它应该是
(2)导电性实验发现熔化的氯化铝不导电,则固态氯化铝是
(3)实验测得氯化铝蒸汽的密度折算成标准状况下为11.92g/L,则氯化铝的分子式为
(4)通过以上的实验与讨论可以得出的有关结论___________。
| A.离子键与共价键之间可以相互转化 |
| B.金属元素与非金属元素之间产生的化合物不一定是离子化合物 |
| C.AlCl3是一个分子式 |
| D.只有非金属的原子之间才能形成共价键 |
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】(1)用电子式表示H2O和MgBr2的形成过程:___ 、___ 。
(2)H2O以___ 键结合,MgBr2以___ 键结合。(填极性键、非极性键、离子键)
(2)H2O以
您最近一年使用:0次

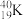 和
和