火箭推进器中装有还原剂液态肼(N2H4)和氧化剂过氧化氢(H2O2),当它们混合时,即产生大量氮气和水蒸气,并放出大量热。已知0.4mol液态肼与足量过氧化氢反应,生成氮气和水蒸气,放出256.65kJ的热量。回答下列问题:
(1)过氧化氢的电子式是___________ 。
(2)该反应的热化学方程式为___________ 。
(3)实验室可用次氯酸钠溶液与氨气反应制备液态肼,已知生成物之一是常见的盐,则反应的化学方程式为___________ 。
(4)在微生物作用的条件下,NH 经过两步反应被氧化成NO
经过两步反应被氧化成NO 。两步反应的能量变化示意图如下:
。两步反应的能量变化示意图如下:
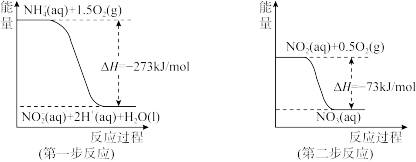
①第一步反应是___________ (填“放热”或“吸热”)反应,判断依据是___________ 。
②1 mol NH (aq)全部氧化成NO
(aq)全部氧化成NO (aq)的反应热ΔH是
(aq)的反应热ΔH是___________ 。
(5)已知: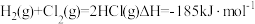 ,几种化学键的键能如下表所示,则a=
,几种化学键的键能如下表所示,则a=___________ 。
(1)过氧化氢的电子式是
(2)该反应的热化学方程式为
(3)实验室可用次氯酸钠溶液与氨气反应制备液态肼,已知生成物之一是常见的盐,则反应的化学方程式为
(4)在微生物作用的条件下,NH
 经过两步反应被氧化成NO
经过两步反应被氧化成NO 。两步反应的能量变化示意图如下:
。两步反应的能量变化示意图如下:
①第一步反应是
②1 mol NH
 (aq)全部氧化成NO
(aq)全部氧化成NO (aq)的反应热ΔH是
(aq)的反应热ΔH是(5)已知:
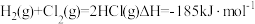 ,几种化学键的键能如下表所示,则a=
,几种化学键的键能如下表所示,则a=| 共价键 | H-H | Cl-Cl | H-Cl |
键能/( ) ) | 436 | 247 | a |
更新时间:2023-10-24 21:05:04
|
相似题推荐
填空题
|
适中
(0.65)
【推荐1】按要求填写:
(1)CH4的空间构型是______ ,H2O的电子式为______ 。
(2)2020年中国火箭发射次数世界第一,N2H4(肼,氢为+1价)常用作火箭燃料,其传统的制备方法发生的离子反应如下:ClO-+2NH3=N2H4+Cl-+H2O
①上述反应的氧化剂可以为______ (填编号)
A. NaClO B. HClO C.两者均可
②若反应消耗4.48 L NH3(标准状况下),此时转移电子数______ 。
(3)写出NaOH溶液中通入足量CO2的离子方程式为______ 。
(1)CH4的空间构型是
(2)2020年中国火箭发射次数世界第一,N2H4(肼,氢为+1价)常用作火箭燃料,其传统的制备方法发生的离子反应如下:ClO-+2NH3=N2H4+Cl-+H2O
①上述反应的氧化剂可以为
A. NaClO B. HClO C.两者均可
②若反应消耗4.48 L NH3(标准状况下),此时转移电子数
(3)写出NaOH溶液中通入足量CO2的离子方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】元素X、Y、Z、M、R均为短周期主族元素,且原子序数依次增大。已知:Y为地壳中含量最多的元素;M原子的最外层电子数与次外层电子数之比为3:4;R-、Z+、X+的离子半径逐渐减小;化合物XR常温下为气体。请回答下列问题:
(1)M元素周期表中的位置为____ ;Z+的结构示意图为____ 。
(2)写出X、Y、R按原子个数之比1:1:1形成的化合物的电子式:____ 。
(3)X与Y可分别形成10电子分子和18电子分子,写出18电子分子转化成10电子分子的化学方程式:____ 。
(4)R的非金属性强于M的,下列能证明这一事实的是____ (填字母)。
(1)M元素周期表中的位置为
(2)写出X、Y、R按原子个数之比1:1:1形成的化合物的电子式:
(3)X与Y可分别形成10电子分子和18电子分子,写出18电子分子转化成10电子分子的化学方程式:
(4)R的非金属性强于M的,下列能证明这一事实的是
| A.常温下的R单质熔沸点比M单质的高 |
| B.R的简单氢化物比M的更稳定 |
| C.一定条件下,R和M的单质都能与NaOH溶液反应 |
| D.最高价氧化物对应水化物的酸性强弱:R>M |
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】物质的组成与结构决定了物质的性质与变化。回答下列问题:
(1)写出如图对应有机物的结构式___________ 。
(2)CH2=CH2的电子式为___________ ,与其相邻的同系物最多有___________ 个原子共平面,工业上利用乙烯制取乙醇反应的化学方程式是___________ 。
(3)某烷烃相对分子质量为72,其一氯代物有四种,它的结构简式是___________ 。
(4)聚氯乙烯(PVC)是生活中常用的塑料,写出由氯乙烯合成聚氯乙烯的化学方程式___________ 。
(5)煤焦油是通过煤的干馏获得的重要的化工原料,其中的甲苯通过下图一系列变化可制得苯甲酸。已知苯甲醇结构简式为 。
。
①A中官能团的名称为___________ 。
②写出下列反应的化学方程式:
A→B___________ 。
A+C___________ 。
③54gA(A的相对分子质量为108)与122gC(C的相对分子质量为122)反应,如果实际得到酯的产率是60%,则可得酯的质量是___________ 。
(1)写出如图对应有机物的结构式

(2)CH2=CH2的电子式为
(3)某烷烃相对分子质量为72,其一氯代物有四种,它的结构简式是
(4)聚氯乙烯(PVC)是生活中常用的塑料,写出由氯乙烯合成聚氯乙烯的化学方程式
(5)煤焦油是通过煤的干馏获得的重要的化工原料,其中的甲苯通过下图一系列变化可制得苯甲酸。已知苯甲醇结构简式为
 。
。
①A中官能团的名称为
②写出下列反应的化学方程式:
A→B
A+C
③54gA(A的相对分子质量为108)与122gC(C的相对分子质量为122)反应,如果实际得到酯的产率是60%,则可得酯的质量是
您最近一年使用:0次
填空题
|
适中
(0.65)
真题
【推荐1】[选修2—化学与技术]
Ⅰ下列有关海水综合利用的说法正确的是__________
Ⅱ
铁在自然界分别广泛,在工业、农业和国防科技中有重要应用。
回答下列问题:
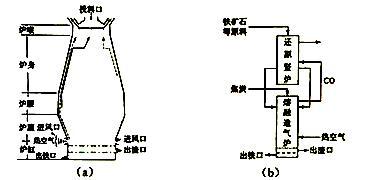
(1)用铁矿石(赤铁矿)冶炼生铁的高炉如图(a)所示。原料中除铁矿石和焦炭外含有_____ 。除去铁矿石中脉石(主要成分为SiO2)的化学反应方程式为_________________ 、__________________ ;高炉排出气体的主要成分有N2、CO2和____ (填化学式)。
(2)已知:①Fe2O3 (s)+3C(s)="2Fe(s)+3CO(g)" ΔH=+494kJ·mol-1
②CO(g)+ O2(g)=CO2(g) ΔH=-283kJ·mol-1
O2(g)=CO2(g) ΔH=-283kJ·mol-1
③C(s)+ O2(g)=CO(g) ΔH=-110kJ·mol-1
O2(g)=CO(g) ΔH=-110kJ·mol-1
则反应Fe2O3 (s)+3 C(s)+ O2(g)=2Fe(s)+3CO2 (g) 的ΔH=
O2(g)=2Fe(s)+3CO2 (g) 的ΔH=____ kJ·mol-1。理论上反应_____ 放出的热量足以供给反应____ 所需的热量(填上述方程式序号)
(3)有人设计出“二步熔融还原法”炼铁工艺,其流程如图(b)所示,其中,还原竖炉相当于高炉的_____ 部分,主要反应的化学方程式为______________________ ;熔融造气炉相当于高炉的_____ 部分。
(4)铁矿石中常含有硫,使高炉气中混有SO2污染空气,脱SO2的方法是_________ 。
Ⅰ下列有关海水综合利用的说法正确的是
| A.电解饱和食盐水可制得金属钠 | B.海带提碘只涉及物理变化 |
| C.海水提溴涉及到氧化还原反应 | D.海水提镁涉及到复分解反应 |
Ⅱ
铁在自然界分别广泛,在工业、农业和国防科技中有重要应用。

回答下列问题:
(1)用铁矿石(赤铁矿)冶炼生铁的高炉如图(a)所示。原料中除铁矿石和焦炭外含有
(2)已知:①Fe2O3 (s)+3C(s)="2Fe(s)+3CO(g)" ΔH=+494kJ·mol-1
②CO(g)+
 O2(g)=CO2(g) ΔH=-283kJ·mol-1
O2(g)=CO2(g) ΔH=-283kJ·mol-1③C(s)+
 O2(g)=CO(g) ΔH=-110kJ·mol-1
O2(g)=CO(g) ΔH=-110kJ·mol-1则反应Fe2O3 (s)+3 C(s)+
 O2(g)=2Fe(s)+3CO2 (g) 的ΔH=
O2(g)=2Fe(s)+3CO2 (g) 的ΔH=(3)有人设计出“二步熔融还原法”炼铁工艺,其流程如图(b)所示,其中,还原竖炉相当于高炉的
(4)铁矿石中常含有硫,使高炉气中混有SO2污染空气,脱SO2的方法是
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】(1)已知热化学方程式H2(g)+ O2(g)=H2O(g) ΔH=-241.8kJ·mol-1,该正反应的活化能为167.2kJ·mol-1,则其逆反应的活化能为
O2(g)=H2O(g) ΔH=-241.8kJ·mol-1,该正反应的活化能为167.2kJ·mol-1,则其逆反应的活化能为_________ kJ·mol-1
(2)某温度下,在一个2L的密闭容器中,加入4molA和2molB进行如下反应:3A(g)+2B(g) 4C(?)+2D(?)。反应一段时间后达到平衡,测得生成1.6molC,且反应的前后压强之比为5:4(相同的温度下测量),平衡后加入C,B的平衡转化率
4C(?)+2D(?)。反应一段时间后达到平衡,测得生成1.6molC,且反应的前后压强之比为5:4(相同的温度下测量),平衡后加入C,B的平衡转化率_________ (增大、减少、不变)。
 O2(g)=H2O(g) ΔH=-241.8kJ·mol-1,该正反应的活化能为167.2kJ·mol-1,则其逆反应的活化能为
O2(g)=H2O(g) ΔH=-241.8kJ·mol-1,该正反应的活化能为167.2kJ·mol-1,则其逆反应的活化能为(2)某温度下,在一个2L的密闭容器中,加入4molA和2molB进行如下反应:3A(g)+2B(g)
 4C(?)+2D(?)。反应一段时间后达到平衡,测得生成1.6molC,且反应的前后压强之比为5:4(相同的温度下测量),平衡后加入C,B的平衡转化率
4C(?)+2D(?)。反应一段时间后达到平衡,测得生成1.6molC,且反应的前后压强之比为5:4(相同的温度下测量),平衡后加入C,B的平衡转化率
您最近一年使用:0次
【推荐3】含碳的化合物之间很容易发生转化。请回答下列问题:
(1)有机物 M 在有光的时候很容易转化成 N,其过程如下:
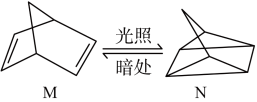
M 到 N 过程中,光能转化为__________ 能;其中较稳定的物质是_____________ (用 M、N 回答)。
(2)已知(l)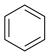 的燃烧热为3267.5kJ·mol-1,
的燃烧热为3267.5kJ·mol-1,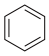 (l)+6O2(g)═6CO2(g)+3H2(g)△H=akJ·mol-1,则 a
(l)+6O2(g)═6CO2(g)+3H2(g)△H=akJ·mol-1,则 a__________ -3267.5(填“>”、“<”或“=”)。
(3)在标准状态即压力为 100kPa,一定温度下,由元素最稳定的单质生成生成 1mol 纯化合物时的反应热称为该化合物的标准摩尔生成焓(△H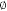 )。已知 100kPa,一定温度下:
)。已知 100kPa,一定温度下:
Fe2 O 3(s)+3C(石墨)=2Fe(s)+3CO(g) △H=+490.0 kJ·mol-1
CO(g)+1/2O2(g)=CO2 (g) △H=-280.0kJ·mol-1
C(石墨)+O 2 ( g)=CO2 (g) △H=-390.5kJ·mol-1
则 Fe2O3的标准摩尔生成焓△H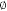 =
=______________ 。
(1)有机物 M 在有光的时候很容易转化成 N,其过程如下:

M 到 N 过程中,光能转化为
(2)已知(l)
 的燃烧热为3267.5kJ·mol-1,
的燃烧热为3267.5kJ·mol-1, (l)+6O2(g)═6CO2(g)+3H2(g)△H=akJ·mol-1,则 a
(l)+6O2(g)═6CO2(g)+3H2(g)△H=akJ·mol-1,则 a(3)在标准状态即压力为 100kPa,一定温度下,由元素最稳定的单质生成生成 1mol 纯化合物时的反应热称为该化合物的标准摩尔生成焓(△H
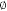 )。已知 100kPa,一定温度下:
)。已知 100kPa,一定温度下:Fe2 O 3(s)+3C(石墨)=2Fe(s)+3CO(g) △H=+490.0 kJ·mol-1
CO(g)+1/2O2(g)=CO2 (g) △H=-280.0kJ·mol-1
C(石墨)+O 2 ( g)=CO2 (g) △H=-390.5kJ·mol-1
则 Fe2O3的标准摩尔生成焓△H
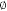 =
=
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】根据已知信息,按要求写出指定反应的热化学方程式
(1)LiH可作飞船的燃料,已知下列反应:
①2Li(s)+H2(g)=2LiH(s) ΔH=-182kJ·mol-1
②2H2(g)+O2(g)=2H2O(l) ΔH=-572kJ·mol-1
③4Li(s)+O2(g)=2Li2O(s) ΔH=-1196kJ·mol-1
试写出LiH在O2中燃烧的热化学方程式:____________ 。
(2)工业上制取硝酸铵的流程图如下所示:
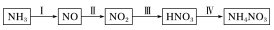
已知:4NO(g)+4NH3(g)+O2(g)⇌4N2(g)+6H2O(g) ΔH=-1745.2kJ·mol-1;
6NO(g)+4NH3(g)⇌5N2(g)+6H2O(g) ΔH=-1925.2kJ·mol-1。
则反应I的热化学方程式可表示为_______ 。
(3)饮用水中的 主要来自于
主要来自于 。已知在微生物的作用下,
。已知在微生物的作用下, 经过两步反应被氧化成
经过两步反应被氧化成 。两步反应的能量变化示意图如下:
。两步反应的能量变化示意图如下:
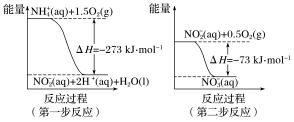
1mol 全部被氧化成
全部被氧化成 的热化学方程式为
的热化学方程式为_______ 。
(1)LiH可作飞船的燃料,已知下列反应:
①2Li(s)+H2(g)=2LiH(s) ΔH=-182kJ·mol-1
②2H2(g)+O2(g)=2H2O(l) ΔH=-572kJ·mol-1
③4Li(s)+O2(g)=2Li2O(s) ΔH=-1196kJ·mol-1
试写出LiH在O2中燃烧的热化学方程式:
(2)工业上制取硝酸铵的流程图如下所示:

已知:4NO(g)+4NH3(g)+O2(g)⇌4N2(g)+6H2O(g) ΔH=-1745.2kJ·mol-1;
6NO(g)+4NH3(g)⇌5N2(g)+6H2O(g) ΔH=-1925.2kJ·mol-1。
则反应I的热化学方程式可表示为
(3)饮用水中的
 主要来自于
主要来自于 。已知在微生物的作用下,
。已知在微生物的作用下, 经过两步反应被氧化成
经过两步反应被氧化成 。两步反应的能量变化示意图如下:
。两步反应的能量变化示意图如下:
1mol
 全部被氧化成
全部被氧化成 的热化学方程式为
的热化学方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】(1)已知3N2H4(l) 4NH3(g)+N2(g) △H = —336.6kJ/mol,
4NH3(g)+N2(g) △H = —336.6kJ/mol,
N2(g)+3H2(g) 2NH3(g) △H = —92.4kJ/mol,
2NH3(g) △H = —92.4kJ/mol,
则N2H4(g) N2(g)+2H2(g) △H =
N2(g)+2H2(g) △H = ________________ 。
(2)写出下列物质的电离方程式:
①NaHSO4___________________________________ ,
②K2SO4_____________ ,
③NH4NO3___________________________ 。
(3)写出下列物质的电子式:
Na2S:_________ ; CO2:_________ 。
 4NH3(g)+N2(g) △H = —336.6kJ/mol,
4NH3(g)+N2(g) △H = —336.6kJ/mol,N2(g)+3H2(g)
 2NH3(g) △H = —92.4kJ/mol,
2NH3(g) △H = —92.4kJ/mol,则N2H4(g)
 N2(g)+2H2(g) △H =
N2(g)+2H2(g) △H = (2)写出下列物质的电离方程式:
①NaHSO4
②K2SO4
③NH4NO3
(3)写出下列物质的电子式:
Na2S:
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】(1)捕碳技术(主要指捕获CO2)在降低温室气体排放中具有重要的作用。目前NH3和(NH4)2CO3已经被用作工业捕碳剂,它们与CO2可发生如下可逆反应。
反应Ⅰ:2NH3(l)+H2O(l)+CO2(g) (NH4)2CO3(aq)ΔH1
(NH4)2CO3(aq)ΔH1
反应Ⅱ:NH3(l)+H2O(l)+CO2(g) NH4HCO3(aq)ΔH2
NH4HCO3(aq)ΔH2
反应Ⅲ:(NH4)2CO3(aq)+H2O(l)+CO2(g) 2NH4HCO3(aq)ΔH3
2NH4HCO3(aq)ΔH3
则ΔH3与ΔH1、ΔH2之间的关系是:ΔH3=________ 。
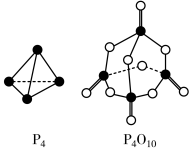
(2)白磷与氧气反应生成P4O10固体。下表所示是部分化学键的键能参数:
根据如图的分子结构和有关数据通过计算写出该反应的热化学方程式为________ 。
反应Ⅰ:2NH3(l)+H2O(l)+CO2(g)
 (NH4)2CO3(aq)ΔH1
(NH4)2CO3(aq)ΔH1反应Ⅱ:NH3(l)+H2O(l)+CO2(g)
 NH4HCO3(aq)ΔH2
NH4HCO3(aq)ΔH2反应Ⅲ:(NH4)2CO3(aq)+H2O(l)+CO2(g)
 2NH4HCO3(aq)ΔH3
2NH4HCO3(aq)ΔH3则ΔH3与ΔH1、ΔH2之间的关系是:ΔH3=
(2)白磷与氧气反应生成P4O10固体。下表所示是部分化学键的键能参数:
| 化学键 | P—P | P—O | P=O | O=O |
| 键能/kJ·mol-1 | a | b | c | d |
根据如图的分子结构和有关数据通过计算写出该反应的热化学方程式为

您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】由化学能转变的热能仍然是人类目前使用的最主要能源之一。回答下列问题:
(1)CH3OH是优质液体燃料。在25℃、101kPa下,每充分燃烧1gCH3OH并恢复到原状态,会释放22.68kJ的热量。请写出表示CH3OH燃烧热的热化学反应方程式:___________ 。
(2)利用CO和H2在催化剂的作用下合成CH3OH,发生的主反应为CO(g)+2H2(g) CH3OH(g)△H1,已知键能是指断裂1mol化学键所需要吸收的能量。相关化学键的键能数据如下:(其中CO中的碳氧键为C
CH3OH(g)△H1,已知键能是指断裂1mol化学键所需要吸收的能量。相关化学键的键能数据如下:(其中CO中的碳氧键为C O)
O)
由此计算△H1=_______ kJ·mol-1。
(3)纳米级Cu2O由于具有优良的催化性能而受到关注。已知:
2Cu(s)+ O2(g)=Cu2O(s) △H=-169 kJ·mol-1
O2(g)=Cu2O(s) △H=-169 kJ·mol-1
C(s)+ O2(g)=CO(g) △H=-110.5 kJ·mol-1
O2(g)=CO(g) △H=-110.5 kJ·mol-1
2Cu(s)+O2(g)=2CuO(s) △H=-314 kJ·mol-1
则工业上用炭粉在高温条件下还原CuO制取Cu2O和CO的热化学方程式为_______ 。
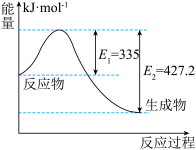
(4)N2和H2反应生成2 mol NH3的过程中能量变化如图所示,计算该反应中每生成1 mol NH3放出热量为______ 。若起始时向容器内放入1 mol N2和3 mol H2,达平衡时有20%的N2转化,则反应中放出的热量为_______ 。
(1)CH3OH是优质液体燃料。在25℃、101kPa下,每充分燃烧1gCH3OH并恢复到原状态,会释放22.68kJ的热量。请写出表示CH3OH燃烧热的热化学反应方程式:
(2)利用CO和H2在催化剂的作用下合成CH3OH,发生的主反应为CO(g)+2H2(g)
 CH3OH(g)△H1,已知键能是指断裂1mol化学键所需要吸收的能量。相关化学键的键能数据如下:(其中CO中的碳氧键为C
CH3OH(g)△H1,已知键能是指断裂1mol化学键所需要吸收的能量。相关化学键的键能数据如下:(其中CO中的碳氧键为C O)
O)| 化学键 | H—H | C—O | C O O | H—O | C—H |
| E/(kJ‧mol-1) | 436 | 343 | 1076 | 465 | 413 |
由此计算△H1=
(3)纳米级Cu2O由于具有优良的催化性能而受到关注。已知:
2Cu(s)+
 O2(g)=Cu2O(s) △H=-169 kJ·mol-1
O2(g)=Cu2O(s) △H=-169 kJ·mol-1C(s)+
 O2(g)=CO(g) △H=-110.5 kJ·mol-1
O2(g)=CO(g) △H=-110.5 kJ·mol-12Cu(s)+O2(g)=2CuO(s) △H=-314 kJ·mol-1
则工业上用炭粉在高温条件下还原CuO制取Cu2O和CO的热化学方程式为
(4)N2和H2反应生成2 mol NH3的过程中能量变化如图所示,计算该反应中每生成1 mol NH3放出热量为

您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】(前两空每空2分,后三空每空3分,共13分)氮气与氢气合成氨是化学工业中极为重要的反应,其热化学方程式可表示为:N2(g)+3H2(g) 2NH3(g) ΔH=-92 kJ·mol-1。请回答下列问题:
2NH3(g) ΔH=-92 kJ·mol-1。请回答下列问题:
(1)取1 mol N2(g)和3 mol H2(g)放在一密闭容器中,在催化剂存在时进行反应,测得反应放出的热量___ (填“大于”“等于”或“小于”)92 kJ,原因 是______________ ;若加入催化剂,ΔH___ (填“变大”“变小”或“不变”)。
(2)已知:破坏1 mol N≡N键、1 mol H—H键需要吸收的能量分别为:946 kJ、436 kJ,则破坏1 mol N—H键需要吸收的能量为_____ kJ。
(3)N2H4可视为NH3分子中的一个H被—NH2取代的产物。发射卫星用N2H4(g)为燃料,NO2为氧化剂,生成N2和H2O(g)。
已知:N2(g)+2O2(g) 2NO2(g) ΔH1=+67.7 kJ·mol-1
2NO2(g) ΔH1=+67.7 kJ·mol-1
N2H4(g)+O2(g) N2(g)+2H2O(g)ΔH2=-534 kJ·mol-1。
N2(g)+2H2O(g)ΔH2=-534 kJ·mol-1。
则:1 mol N2H4与NO2完全反应的热化学方程式为______________________ 。
 2NH3(g) ΔH=-92 kJ·mol-1。请回答下列问题:
2NH3(g) ΔH=-92 kJ·mol-1。请回答下列问题:(1)取1 mol N2(g)和3 mol H2(g)放在一密闭容器中,在催化剂存在时进行反应,测得反应放出的热量
(2)已知:破坏1 mol N≡N键、1 mol H—H键需要吸收的能量分别为:946 kJ、436 kJ,则破坏1 mol N—H键需要吸收的能量为
(3)N2H4可视为NH3分子中的一个H被—NH2取代的产物。发射卫星用N2H4(g)为燃料,NO2为氧化剂,生成N2和H2O(g)。
已知:N2(g)+2O2(g)
 2NO2(g) ΔH1=+67.7 kJ·mol-1
2NO2(g) ΔH1=+67.7 kJ·mol-1N2H4(g)+O2(g)
 N2(g)+2H2O(g)ΔH2=-534 kJ·mol-1。
N2(g)+2H2O(g)ΔH2=-534 kJ·mol-1。则:1 mol N2H4与NO2完全反应的热化学方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】研究氮原子的结构及其化合物具有重要意义
(1)氮原子的基态电子排布式为_______ 。
(2)NH3的电子式_______ 。
(3)实验室制备NH3化学方程式是_______ 。
(4)①工业合成的NH3化学方程式是_______ 。
②i.合成氨工业中,合成塔中每产生2 mol NH3,放出92.2 kJ热量
ii.氮气和氢气断裂其共价键吸收的能量如图:

请计算:1 mol N-H键断裂吸收的能量约等于_______ kJ。
(5)工业上以NH3为原料合成硝酸的路线如图,写出相关反应的化学方程式

①_______ 。②_______ 。③_______ 。
(1)氮原子的基态电子排布式为
(2)NH3的电子式
(3)实验室制备NH3化学方程式是
(4)①工业合成的NH3化学方程式是
②i.合成氨工业中,合成塔中每产生2 mol NH3,放出92.2 kJ热量
ii.氮气和氢气断裂其共价键吸收的能量如图:

请计算:1 mol N-H键断裂吸收的能量约等于
(5)工业上以NH3为原料合成硝酸的路线如图,写出相关反应的化学方程式

①
您最近一年使用:0次



