Ⅰ.回答下列问题
(1)写出铅酸蓄电池放电时负极电极反应:___________
Ⅱ.如图所示的装置中,若通入直流电5min时,铜电极质量增加21.6g,试回答:
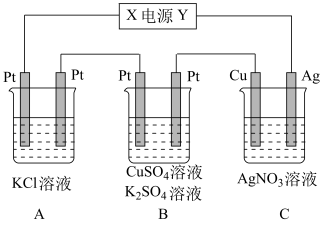
(2)电源为碱性氢氧燃料电池,则电源电极X的电极反应式为___________
(3)若A中KCl足量且溶液的体积也是200mL,电解后,溶液的OH-的物质的量浓度为___________ mol/L(假设电解前后溶液的体积无变化);
(4)通电5min后,B中共收集2240mL气体(标准状况),溶液体积为200mL,则通电前CuSO4溶液的物质的量浓度为___________ (设电解前后溶液体积无变化),若要使 装置溶液要恢复到电解前的状态,需要加入的物质以及相应的物质的量正确的是
装置溶液要恢复到电解前的状态,需要加入的物质以及相应的物质的量正确的是___________ 。
A.0.05molCuO B.0.05molCuO和0.025molH2O
C.0.05molCu(OH)2 D.0.05molCuCO3和0.05molH2O
(1)写出铅酸蓄电池放电时负极电极反应:
Ⅱ.如图所示的装置中,若通入直流电5min时,铜电极质量增加21.6g,试回答:

(2)电源为碱性氢氧燃料电池,则电源电极X的电极反应式为
(3)若A中KCl足量且溶液的体积也是200mL,电解后,溶液的OH-的物质的量浓度为
(4)通电5min后,B中共收集2240mL气体(标准状况),溶液体积为200mL,则通电前CuSO4溶液的物质的量浓度为
 装置溶液要恢复到电解前的状态,需要加入的物质以及相应的物质的量正确的是
装置溶液要恢复到电解前的状态,需要加入的物质以及相应的物质的量正确的是A.0.05molCuO B.0.05molCuO和0.025molH2O
C.0.05molCu(OH)2 D.0.05molCuCO3和0.05molH2O
更新时间:2023/09/29 10:07:39
|
相似题推荐
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】氧化还原反应不管在工业生产还是在日常生活中都随处可见,可以用于实现化学能到电能的转化,还可用于测定某一溶液的物质的量浓度。
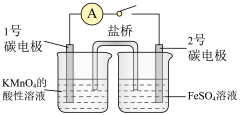
(1)已知当电路闭合后,左侧烧杯中溶液逐渐褪色,试使用半反应的形式解释原因___________ 。
(2)使用该装置时,有人发现右侧溶液在未闭合电路时已出现变色现象,试根据 的性质选择合适的溶液配制方法:
的性质选择合适的溶液配制方法:___________ 。

(1)已知当电路闭合后,左侧烧杯中溶液逐渐褪色,试使用半反应的形式解释原因
(2)使用该装置时,有人发现右侧溶液在未闭合电路时已出现变色现象,试根据
 的性质选择合适的溶液配制方法:
的性质选择合适的溶液配制方法:
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】I.利用催化氧化反应将 转化为
转化为 是工业上生产硫酸的关键步骤,发生反应,
是工业上生产硫酸的关键步骤,发生反应, 。请回答下列问题:
。请回答下列问题:
(1)某次实验中,在容积为 的恒温密闭容器中通入
的恒温密闭容器中通入 和
和 ,反应过程中部分物质的物质的量随反应时间的变化如图所示。
,反应过程中部分物质的物质的量随反应时间的变化如图所示。

① 时,
时,
_______ (填“>”、“>”或“=”) 。
。
②用 的浓度变化表示
的浓度变化表示 内反应的平均速率是
内反应的平均速率是_______ 。
③反应达到平衡时, 的体积分数为20%,则
的体积分数为20%,则
_______  。
。
(2)下列情况能够说明该反应达到化学平衡状态的是_______(填字母)。
II.某种燃料电池的工作原理示意图如图所示,a、b均为惰性电极。

(3)①使用时,空气从_______ (填“A”或“B”)口通入。
②假设使用的“燃料”是甲醇 ,a极的电极反应式为
,a极的电极反应式为_______ 。
 转化为
转化为 是工业上生产硫酸的关键步骤,发生反应,
是工业上生产硫酸的关键步骤,发生反应, 。请回答下列问题:
。请回答下列问题:(1)某次实验中,在容积为
 的恒温密闭容器中通入
的恒温密闭容器中通入 和
和 ,反应过程中部分物质的物质的量随反应时间的变化如图所示。
,反应过程中部分物质的物质的量随反应时间的变化如图所示。
①
 时,
时,
 。
。②用
 的浓度变化表示
的浓度变化表示 内反应的平均速率是
内反应的平均速率是③反应达到平衡时,
 的体积分数为20%,则
的体积分数为20%,则
 。
。(2)下列情况能够说明该反应达到化学平衡状态的是_______(填字母)。
A. |
| B.恒温恒容时,混合气体的密度不再随时间变化 |
C. 的物质的量不再变化 的物质的量不再变化 |
D.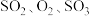 三者的浓度之比为2∶1∶2 三者的浓度之比为2∶1∶2 |
II.某种燃料电池的工作原理示意图如图所示,a、b均为惰性电极。

(3)①使用时,空气从
②假设使用的“燃料”是甲醇
 ,a极的电极反应式为
,a极的电极反应式为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】I.如图所示是一个电化学装置的示意图。

请回答下列问题:
(1)图中甲池是_______ (填“原电池”、“电解池”或“电镀池”)。
(2)A(石墨)电极的名称是_______ (填“正极”、“负极”、“阴极”或“阳极”)。
(3)若把KOH溶液换成熔融Al2O3,传导O2-,写出通入CH3OH的电极的电极反应式:_______ 。
(4)乙池中反应的化学方程式为_______ 。
(5)当乙池中B极质量增加5.4g时,甲池中理论上消耗O2的体积为_______ L(标准状况),此时丙池中某电极析出1.6g某金属,则丙池中的某盐溶液可能是_______ (填字母)。
A.MgSO4 B.CuSO4 C.NaCl D.AgNO3
II.某课外活动小组进行电化学实验,请回答下列问题:
(6)该小组运用工业上离子交换膜法制烧碱的原理,用如下图所示装置电解K2SO4溶液。
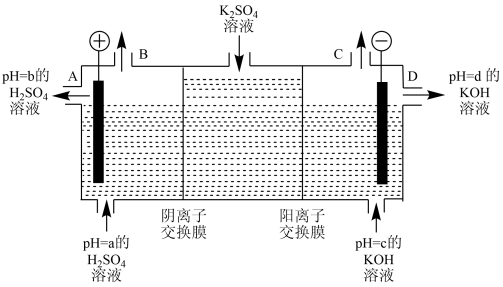
①该电解槽的阳极反应式为_______ ,通过阴离子交换膜的离子数_______ (填“>”“<”或“=”)通过阳离子交换膜的离子数;
②电解一段时间后,C口与B口产生气体的质量比为_______ 。

请回答下列问题:
(1)图中甲池是
(2)A(石墨)电极的名称是
(3)若把KOH溶液换成熔融Al2O3,传导O2-,写出通入CH3OH的电极的电极反应式:
(4)乙池中反应的化学方程式为
(5)当乙池中B极质量增加5.4g时,甲池中理论上消耗O2的体积为
A.MgSO4 B.CuSO4 C.NaCl D.AgNO3
II.某课外活动小组进行电化学实验,请回答下列问题:
(6)该小组运用工业上离子交换膜法制烧碱的原理,用如下图所示装置电解K2SO4溶液。

①该电解槽的阳极反应式为
②电解一段时间后,C口与B口产生气体的质量比为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】甲醇是重要的工业原料和燃料。
(1)甲醇燃料电池(DMFC)为现代便携式电子产品提供了电能。在以KOH为电解质的甲醇燃料电池中,CH3OH在电源_______ (填“正”或“负”)极反应,当电路中转移0.6mol电子时,消耗CH3OH的物质的量是_______ ;该电池工作一段时间后,电解质溶液的pH_______ (填“增大”“减小”或“不变”)。
(2)利用甲醇通过惰性电解法先获得α-羟基缩酮,α-羟基缩酮再在酸性条件下水解得到一种食品增香剂3-羟基丁酮,其原理如图所示。
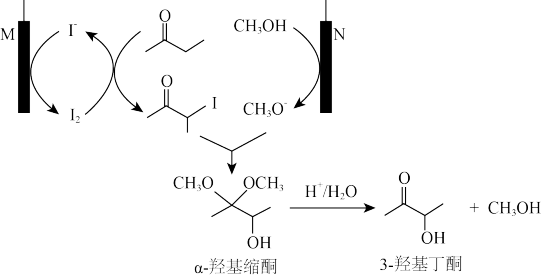
①M极上发生_______ (填“氧化反应”或“还原反应”)。
②N为电解池的_______ 极(填“阴”或“阳”),电极反应式是_______ 。
③此法合成3-羟基丁酮的总反应式是_______ (不用写反应条件)。
(1)甲醇燃料电池(DMFC)为现代便携式电子产品提供了电能。在以KOH为电解质的甲醇燃料电池中,CH3OH在电源
(2)利用甲醇通过惰性电解法先获得α-羟基缩酮,α-羟基缩酮再在酸性条件下水解得到一种食品增香剂3-羟基丁酮,其原理如图所示。

①M极上发生
②N为电解池的
③此法合成3-羟基丁酮的总反应式是
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】如图为一个电化学过程的示意图。

请回答下列问题:
(1)通入CH3OH一极的电极反应式为__________________________ 。
(2)乙池是铜的精炼池,则A电极的材料是___________ ,B极的电极反应式为___________________ 。
(3)丙池含有0.01molKCl的溶液100mL,假如电路中转移了0.02mole-,则阳极产生的气体在标准状况下的体积是_______________ 。
(4)丙池中滴有酚酞,实验开始后观察到的现象是__________________________ ,写出丙池的总反应方程式_________________________ 。

请回答下列问题:
(1)通入CH3OH一极的电极反应式为
(2)乙池是铜的精炼池,则A电极的材料是
(3)丙池含有0.01molKCl的溶液100mL,假如电路中转移了0.02mole-,则阳极产生的气体在标准状况下的体积是
(4)丙池中滴有酚酞,实验开始后观察到的现象是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】燃料电池和锂离子电池在生产生活中占据重要地位,甲醇是常见的燃料电池原料,CO2催化氢化可合成甲醇。反应为:CO2(g)+3H2(g) CH3OH(g)+H2O(g),该反应为吸热反应。完成下列填空:
CH3OH(g)+H2O(g),该反应为吸热反应。完成下列填空:
(1)以上合成甲醇的反应说明反应物的总能量____ (填“大于”“小于”“等于”)生成物的总能量。
(2)CH3OH作为燃料电池的____ (填“正极”或“负极”)反应物,若以KOH溶液为电解质溶液,则该电极反应方程式为____ 。
(3)在1L容器中充入1molCO2和3molH2,反应5min后,达到平衡状态,气体的总物质的量变为原来的75%,则0~5min内,H2的平均反应速率为____ ,CO2的平衡转化率为____ 。
 CH3OH(g)+H2O(g),该反应为吸热反应。完成下列填空:
CH3OH(g)+H2O(g),该反应为吸热反应。完成下列填空:(1)以上合成甲醇的反应说明反应物的总能量
(2)CH3OH作为燃料电池的
(3)在1L容器中充入1molCO2和3molH2,反应5min后,达到平衡状态,气体的总物质的量变为原来的75%,则0~5min内,H2的平均反应速率为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】某课外小组分别用如图所示装置对原电池和电解原理进行实验探究。
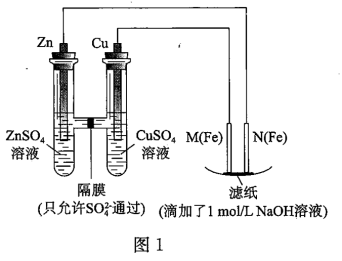
请回答:
Ⅰ.用如图1所示装置进行第一组实验。
(1)在保证电极反应不变的情况下,不能替代Cu做电极的是___________ (填字母序号)。
A.铝 B.石墨 C.银 D.铂
(2)M极发生反应的电极反应式为___________ ;
(3)实验过程中,SO
___________ (填“从左向右”、“从右向左”或“不”)移动;滤纸上能观察到的现象有___________ ,写出产生此现象的反应方程式:___________ ;
Ⅱ.用如图2所示装置进行第二组实验。实验过程中,两极均有气体产生,Y极区溶液逐渐变成紫红色;停止实验,铁电极明显变细,电解液仍然澄清。查阅资料发现,高铁酸根(FeO )在溶液中呈紫红色。
)在溶液中呈紫红色。
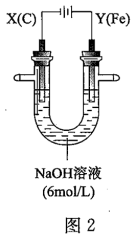
(4)电解过程中,X极区溶液的pH___________ (填“增大”、“减小”或“不变”);
(5)电解过程中,Y极发生的电极反应为___________ 和4OH--4e-=2H2O+O2↑,若在X极收集到672mL气体,在Y极收集到168mL气体(均已折算为标准状况时气体体积),则Y电极(铁电极)质量减少___________ g。
(6)在碱性锌电池中,用高铁酸钾作为正极材料,电池总反应为:2K2FeO4+3Zn=Fe2O3+ZnO+2K2ZnO2该电池正极的电极反应式为___________ 。

请回答:
Ⅰ.用如图1所示装置进行第一组实验。
(1)在保证电极反应不变的情况下,不能替代Cu做电极的是
A.铝 B.石墨 C.银 D.铂
(2)M极发生反应的电极反应式为
(3)实验过程中,SO

Ⅱ.用如图2所示装置进行第二组实验。实验过程中,两极均有气体产生,Y极区溶液逐渐变成紫红色;停止实验,铁电极明显变细,电解液仍然澄清。查阅资料发现,高铁酸根(FeO
 )在溶液中呈紫红色。
)在溶液中呈紫红色。
(4)电解过程中,X极区溶液的pH
(5)电解过程中,Y极发生的电极反应为
(6)在碱性锌电池中,用高铁酸钾作为正极材料,电池总反应为:2K2FeO4+3Zn=Fe2O3+ZnO+2K2ZnO2该电池正极的电极反应式为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】电化学处理:用电解法降解NO ,其原理如下图所示。
,其原理如下图所示。
电源正极为________ (填“A”或“B”),阴极反应式为_____ 。

 ,其原理如下图所示。
,其原理如下图所示。电源正极为

您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】绿色甲醇 是2023年杭州亚运会主火炬燃料,制备绿色甲醇分为三个阶段:利用可再生能源制绿氢、
是2023年杭州亚运会主火炬燃料,制备绿色甲醇分为三个阶段:利用可再生能源制绿氢、 的捕集、
的捕集、 和
和 一步法制甲醇。
一步法制甲醇。
(1)磁场辅助光电分解水制氢的工作原理如下[磁场辅助光照电极材料促使单位时间内产生更多的“电子”和“空穴”( ,具有强氧化性),驱动并加快电极反应]。
,具有强氧化性),驱动并加快电极反应]。______ (填“阴”或“阳”)极。
②理论上生成的气体M与N的质量之比为______ 。
③在酸性介质中生成M的电极反应式为______ 。
(2)工业上从高炉气中捕集 的示意图如图所示。
的示意图如图所示。 溶液从塔顶喷洒,这样做的优点是
溶液从塔顶喷洒,这样做的优点是____________ 。
②若从“吸收塔”出来的盐溶液中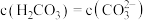 ,则该溶液的pH为
,则该溶液的pH为______
[该条件下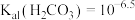 、
、 ,不考虑其他因素对pH的影响]。
,不考虑其他因素对pH的影响]。
③为研究温度对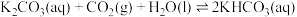 的影响,将一定量的
的影响,将一定量的 溶液置于密闭容器中,并充入一定量的
溶液置于密闭容器中,并充入一定量的 气体,保持其他初始实验条件不变,分别在不同温度下,经过相同时间测得
气体,保持其他初始实验条件不变,分别在不同温度下,经过相同时间测得 气体的浓度如图所示:
气体的浓度如图所示: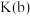
______ 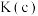 (填“>”“<”或“=”);
(填“>”“<”或“=”); 温度范围内,容器内
温度范围内,容器内 气体浓度呈减小的趋势,其原因是
气体浓度呈减小的趋势,其原因是______ 。
 是2023年杭州亚运会主火炬燃料,制备绿色甲醇分为三个阶段:利用可再生能源制绿氢、
是2023年杭州亚运会主火炬燃料,制备绿色甲醇分为三个阶段:利用可再生能源制绿氢、 的捕集、
的捕集、 和
和 一步法制甲醇。
一步法制甲醇。(1)磁场辅助光电分解水制氢的工作原理如下[磁场辅助光照电极材料促使单位时间内产生更多的“电子”和“空穴”(
 ,具有强氧化性),驱动并加快电极反应]。
,具有强氧化性),驱动并加快电极反应]。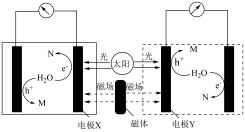
②理论上生成的气体M与N的质量之比为
③在酸性介质中生成M的电极反应式为
(2)工业上从高炉气中捕集
 的示意图如图所示。
的示意图如图所示。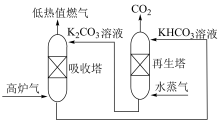
 溶液从塔顶喷洒,这样做的优点是
溶液从塔顶喷洒,这样做的优点是②若从“吸收塔”出来的盐溶液中
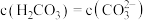 ,则该溶液的pH为
,则该溶液的pH为[该条件下
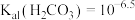 、
、 ,不考虑其他因素对pH的影响]。
,不考虑其他因素对pH的影响]。③为研究温度对
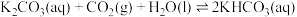 的影响,将一定量的
的影响,将一定量的 溶液置于密闭容器中,并充入一定量的
溶液置于密闭容器中,并充入一定量的 气体,保持其他初始实验条件不变,分别在不同温度下,经过相同时间测得
气体,保持其他初始实验条件不变,分别在不同温度下,经过相同时间测得 气体的浓度如图所示:
气体的浓度如图所示: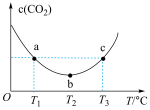
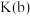
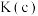 (填“>”“<”或“=”);
(填“>”“<”或“=”); 温度范围内,容器内
温度范围内,容器内 气体浓度呈减小的趋势,其原因是
气体浓度呈减小的趋势,其原因是
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】新型高效的甲烷燃料电池采用铂为电极材料,两电极上分别通入CH4和O2,电解质溶液为KOH溶液。某研究小组以甲烷燃料电池(装置甲)为电源,模拟氯碱工业生产原理,装置如图所示。请回答以下问题:

(1)B、D的电极名称分别是______ 、______ 。
(2)C极可以选用的材料是______ (填标号)。
(3)该装置开始工作时,Cl-向______ 极(填“C”或“D”)移动,工作一段时间后观察到D极的现象是______ ,C极发生的电极反应为______ 。
(4)甲装置中K+向______ 极(填“A”或“B”)移动,A极发生的电极反应为______ 。
(5)装置甲、乙中的电解质溶液足量,当电路中通过0.4mol电子时,气体a、b的总物质的量与气体c、d的总物质的量之比为______ 。
(6)若以装置甲为电源,要在铁器上镀铜,则铁器应连接______ (填“A”或“B”)极。

(1)B、D的电极名称分别是
(2)C极可以选用的材料是
| A.铁棒 | B.银棒 | C.石墨棒 | D.铜棒 |
(3)该装置开始工作时,Cl-向
(4)甲装置中K+向
(5)装置甲、乙中的电解质溶液足量,当电路中通过0.4mol电子时,气体a、b的总物质的量与气体c、d的总物质的量之比为
(6)若以装置甲为电源,要在铁器上镀铜,则铁器应连接
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】 在传统的电解氯化氢回收氯气技术的基础上,科学家最近采用碳基电极材料设计了一种新的工艺方案,主要包括电化学过程和化学过程,如下图所示:
在传统的电解氯化氢回收氯气技术的基础上,科学家最近采用碳基电极材料设计了一种新的工艺方案,主要包括电化学过程和化学过程,如下图所示:

负极区发生的反应有_________  写反应方程式
写反应方程式 。电路中转移
。电路中转移 电子,需消耗氧气
电子,需消耗氧气__________ 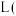 标准状况
标准状况 。
。
 电解法转化
电解法转化 可实现
可实现 资源化利用。电解
资源化利用。电解 制HCOOH的原理示意图如下。
制HCOOH的原理示意图如下。

 写出阴极
写出阴极 还原为
还原为 的电极反应式:
的电极反应式:________ 。
 电解一段时间后,阳极区的
电解一段时间后,阳极区的 溶液浓度降低,其原因是
溶液浓度降低,其原因是_____ 。
 可利用太阳能光伏电池电解水制高纯氢,工作示意图如下。通过控制开关连接
可利用太阳能光伏电池电解水制高纯氢,工作示意图如下。通过控制开关连接 或
或 ,可交替得到
,可交替得到 和
和 。
。

 制
制 时,连接
时,连接_______________ 。产生 的电极反应式是
的电极反应式是_________ 。
 改变开关连接方式,可得
改变开关连接方式,可得 。
。
 结合
结合 和
和 中电极3的电极反应式,说明电极3的作用:
中电极3的电极反应式,说明电极3的作用:___________ 。
 在传统的电解氯化氢回收氯气技术的基础上,科学家最近采用碳基电极材料设计了一种新的工艺方案,主要包括电化学过程和化学过程,如下图所示:
在传统的电解氯化氢回收氯气技术的基础上,科学家最近采用碳基电极材料设计了一种新的工艺方案,主要包括电化学过程和化学过程,如下图所示:
负极区发生的反应有
 写反应方程式
写反应方程式 。电路中转移
。电路中转移 电子,需消耗氧气
电子,需消耗氧气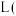 标准状况
标准状况 。
。 电解法转化
电解法转化 可实现
可实现 资源化利用。电解
资源化利用。电解 制HCOOH的原理示意图如下。
制HCOOH的原理示意图如下。
 写出阴极
写出阴极 还原为
还原为 的电极反应式:
的电极反应式: 电解一段时间后,阳极区的
电解一段时间后,阳极区的 溶液浓度降低,其原因是
溶液浓度降低,其原因是 可利用太阳能光伏电池电解水制高纯氢,工作示意图如下。通过控制开关连接
可利用太阳能光伏电池电解水制高纯氢,工作示意图如下。通过控制开关连接 或
或 ,可交替得到
,可交替得到 和
和 。
。
 制
制 时,连接
时,连接 的电极反应式是
的电极反应式是 改变开关连接方式,可得
改变开关连接方式,可得 。
。 结合
结合 和
和 中电极3的电极反应式,说明电极3的作用:
中电极3的电极反应式,说明电极3的作用:
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】I.装置如图所示,C、D、E、F、X、Y都是惰性电极,甲、乙中溶液的体积和浓度都相同(假设通电前后溶液体积不变),A、B为外接直流电源的两极。将直流电源接通后,F极附近呈红色。请回答:

(1)B极是电源的___________ 极,C极的电极反应式为___________ ,一段时间后丁中X极附近的颜色逐渐___________ (填“变深”或“变浅”)。(已知氢氧化铁胶粒带正电荷)
(2)若甲、乙装置中的C、D、E、F电极均只有一种单质生成,对应单质的物质的量之比为___________ 。
(3)现用丙装置给铜件镀银,则H应该是___________ (填“铜”或“银”)。常温下,当乙中溶液的 时(此时乙溶液体积为500 mL),丙中镀件上析出银的质量为
时(此时乙溶液体积为500 mL),丙中镀件上析出银的质量为___________ g。
(4)甲装置中发生反应的化学方程式为___________ ;乙装置中发生反应的离子方程式为___________ 。
II.通过NOx传感器可监测NOx的含量,工作原理示意图如下:

(5)Pt电极上发生的是___________ 反应(填“氧化”或“还原”)。
(6)写出NiO电极的电极反应式:___________ 。

(1)B极是电源的
(2)若甲、乙装置中的C、D、E、F电极均只有一种单质生成,对应单质的物质的量之比为
(3)现用丙装置给铜件镀银,则H应该是
 时(此时乙溶液体积为500 mL),丙中镀件上析出银的质量为
时(此时乙溶液体积为500 mL),丙中镀件上析出银的质量为(4)甲装置中发生反应的化学方程式为
II.通过NOx传感器可监测NOx的含量,工作原理示意图如下:

(5)Pt电极上发生的是
(6)写出NiO电极的电极反应式:
您最近一年使用:0次



