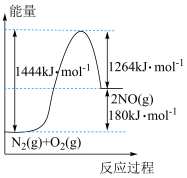
一定条件下N2(g)、O2(g)反应生成NO(g)的能量关系如图所示,下列说法错误的是

A.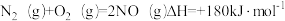 |
| B.该反应中反应物分子的每次碰撞都为有效碰撞 |
| C.正反应的活化能大于逆反应的活化能 |
| D.使用催化剂可增加单位时间内NO的产量 |
更新时间:2023-11-06 20:25:56
|
相似题推荐
单选题
|
较易
(0.85)
名校
【推荐1】2022年,我国220/120吨级烧氢液氧发动机试车成功,为我们探索星辰大海再添助力。航空航天兴趣小组查资料得知:
①2H2(g)+O2(g)=2H2O(g) △H=−483.6kJ∙mol−1
②H2O(g)=H2O(l) △H=−44kJ∙mol−1
③H−H、O=O、H−O键能分别为436 kJ∙mol−1、496 kJ∙mol−1、462 kJ∙mol−1。 经讨论得出以下结论,正确的是
①2H2(g)+O2(g)=2H2O(g) △H=−483.6kJ∙mol−1
②H2O(g)=H2O(l) △H=−44kJ∙mol−1
③H−H、O=O、H−O键能分别为436 kJ∙mol−1、496 kJ∙mol−1、462 kJ∙mol−1。 经讨论得出以下结论,正确的是

| A.若只用以上的键能数据,使可估算出H2的燃烧热 |
| B.若1 mol H2(1)燃烧生成H2O(g)时,放出的热量将高于241.8 kJ |
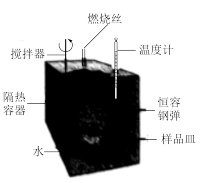
| C.若用上图所示装置,即可测出H2的燃烧热:△H=−285.8 kJ∙mol−1 |
| D.化学键断裂和形成时的能量变化是化学反应中能量变化的主要原因 |
您最近一年使用:0次
单选题
|
较易
(0.85)
【推荐2】化学反应可视为旧键断裂和新键形成的过程。化学键的键能是形成(或拆开)1 mol化学键时释放(或吸收)的能量。已知白磷和P4O6的分子结构如图所示,现提供以下化学键的键能(kJ/mol):P-P:198,P-O:360,O=O:498,则反应P4(白磷)+3O2=P4O6中消耗3 mol O2放出的热量为


| A.1368kJ | B.1498kJ | C.1638kJ | D.1683kJ |
您最近一年使用:0次
单选题
|
较易
(0.85)
【推荐1】反应2SO2(g) + O2(g) 2SO3(g) ΔH =-196.6 kJ·mol−1因SO2在催化剂表面与O2接触而得名,反应过程示意图如图:
2SO3(g) ΔH =-196.6 kJ·mol−1因SO2在催化剂表面与O2接触而得名,反应过程示意图如图:
 2SO3(g) ΔH =-196.6 kJ·mol−1因SO2在催化剂表面与O2接触而得名,反应过程示意图如图:
2SO3(g) ΔH =-196.6 kJ·mol−1因SO2在催化剂表面与O2接触而得名,反应过程示意图如图:
| A.反应①的活化能比反应②高 |
| B.使用催化剂能改变反应途径,降低反应的焓变 |
| C.图示过程中既有S-O的断裂,又有S-O的形成 |
| D.其他条件不变,升高体系的温度,该反应的平衡常数K增大 |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
【推荐2】下列说法正确的是
| A.活化分子间的碰撞一定能发生化学反应 |
| B.普通分子间的碰撞有时也能发生化学反应 |
| C.增大浓度,活化分子百分数增大 |
| D.化学反应的实质是活化分子有合适取向时的有效碰撞 |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
【推荐1】对于在一定条件下进行的化学反应,改变下列条件,可以提高反应物中的活化分子百分数的是
①升高温度②加入催化剂③增大体系压强④增大反应物浓度
①升高温度②加入催化剂③增大体系压强④增大反应物浓度
| A.①② | B.②③ | C.③④ | D.①④ |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
解题方法
【推荐2】Ni可活化 制得
制得 ,其反应历程如图所示:
,其反应历程如图所示:
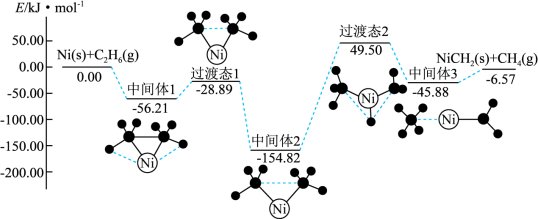
下列关于活化历程的说法正确的是
 制得
制得 ,其反应历程如图所示:
,其反应历程如图所示:
下列关于活化历程的说法正确的是
A.总反应的 |
| B.Ni是该反应的催化剂,参与反应的过程 |
| C.该反应过程中有碳氢键的断裂和形成 |
| D.总反应的速率由“中间体1→中间体2”决定 |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
【推荐1】影响化学反应速率的因素有多方面,如浓度、压强、温度、催化剂等。下列有关说法不正确的是
| A.增大体系压强不一定能加快反应速率 |
| B.增大浓度能增加反应体系中活化分子的百分数 |
| C.催化剂能改变反应的活化能 |
| D.升高温度能增加反应物分子之间的有效碰撞次数 |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
【推荐2】Burns和Dainton研究发现Cl2与CO合成COCl2的反应机理如下:
①Cl2(g)⇌2Cl•(g) 快
②CO(g)+Cl•(g)⇌COCl•(g) 快
③COCl•(g)+Cl2(g)⇌COCl2(g)+Cl•(g) 慢
反应②的速率方程为v正=k正c(CO)×c(Cl•),v逆=k逆c(COCl•)。下列说法错误的是
①Cl2(g)⇌2Cl•(g) 快
②CO(g)+Cl•(g)⇌COCl•(g) 快
③COCl•(g)+Cl2(g)⇌COCl2(g)+Cl•(g) 慢
反应②的速率方程为v正=k正c(CO)×c(Cl•),v逆=k逆c(COCl•)。下列说法错误的是
| A.反应①的活化能大于反应③的活化能 |
B.反应②的平衡常数K= |
| C.要提高合成COCl2的速率,关键是提高反应③的速率 |
| D.选择合适的催化剂能提高单位时间内COCl2的产率 |
您最近一年使用:0次

 =-44.2kJ•mol-1。若C2H5OH(l)燃烧热
=-44.2kJ•mol-1。若C2H5OH(l)燃烧热 =-QkJ/mol,则C2H4(g)的燃烧热△H为
=-QkJ/mol,则C2H4(g)的燃烧热△H为
 分两步进行:①
分两步进行:①
 ,反应过程能量变化曲线如图所示。下列说法正确的是
,反应过程能量变化曲线如图所示。下列说法正确的是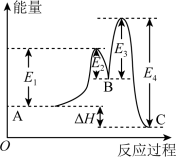
 表示反应
表示反应