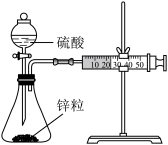
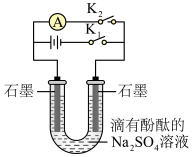
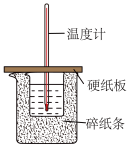
下列实验装置、操作或现象正确的是
| A | B | C | D |
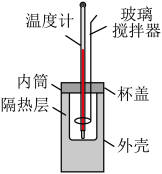 | 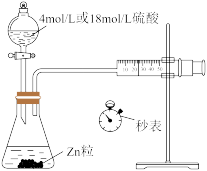 | 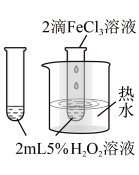 | 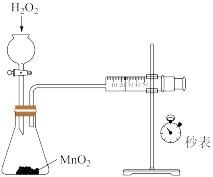 |
| 中和热的测定 | 探究浓度对反应速率的影响 | 探究催化剂对反应速率的影响 | 测定在MnO2催化作用下H2O2的分解速率 |
| A.A | B.B | C.C | D.D |
更新时间:2023-10-06 15:41:47
|
相似题推荐
单选题
|
适中
(0.65)
名校
【推荐1】下列有关化学反应原理的说法中,不正确的是
①发生化学反应的碰撞一定为有效碰撞
②难溶物的溶解度和 的大小都仅仅只受温度的影响
的大小都仅仅只受温度的影响
③某反应正方向能自发进行,则逆方向一定不能自发进行
④某溶液的pH不受温度的影响,那么该溶液一定显强酸性
⑤用盐酸滴定氨水,若选择酚酞做指示剂,则测定的结果会偏小
⑥中和热的测定实验,若量取NaOH溶液的量筒仰视读数,则所测的 偏大
偏大
①发生化学反应的碰撞一定为有效碰撞
②难溶物的溶解度和
 的大小都仅仅只受温度的影响
的大小都仅仅只受温度的影响③某反应正方向能自发进行,则逆方向一定不能自发进行
④某溶液的pH不受温度的影响,那么该溶液一定显强酸性
⑤用盐酸滴定氨水,若选择酚酞做指示剂,则测定的结果会偏小
⑥中和热的测定实验,若量取NaOH溶液的量筒仰视读数,则所测的
 偏大
偏大| A.②③ | B.①③⑤⑥ | C.①③④ | D.②③⑥ |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】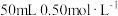 盐酸与
盐酸与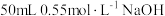 溶液进行中和反应,通过测定反应过程中所放出的热量可计算中和热,下列说法错误的是
溶液进行中和反应,通过测定反应过程中所放出的热量可计算中和热,下列说法错误的是
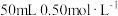 盐酸与
盐酸与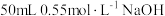 溶液进行中和反应,通过测定反应过程中所放出的热量可计算中和热,下列说法错误的是
溶液进行中和反应,通过测定反应过程中所放出的热量可计算中和热,下列说法错误的是| A.为防止混合溶液时溅出产生误差,混合时速度要慢 |
B.玻璃搅拌器材料若用铜代替,则测得的 会偏大 会偏大 |
C.用相同浓度、相同体积的醋酸溶液代替盐酸进行上述实验,测得的 会偏大 会偏大 |
D.为了保证盐酸完全被中和,采用稍过量的 溶液 溶液 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐1】室温下进行下列实验,根据实验操作和现象所得出的结论正确的是
| 选项 | 实验操作和现象 | 结论 |
| A | 向  硼酸溶液加入 硼酸溶液加入  碳酸钠后溶液无明显变化 碳酸钠后溶液无明显变化 | 硼酸与碳酸钠不反应 |
| B | 向滴有酚酞的   溶液中加水稀释至 溶液中加水稀释至 ,红色变浅 ,红色变浅 | 加水稀释时, 的水解平衡向逆反应方向移动 的水解平衡向逆反应方向移动 |
| C | 向各装有  酸性高锰酸钾溶液的两支试管中,一支加入 酸性高锰酸钾溶液的两支试管中,一支加入   溶液,另一支加入 溶液,另一支加入   溶液充分反应,记录酸性高锰酸钾褪色时间 溶液充分反应,记录酸性高锰酸钾褪色时间 | 其他条件相同时,草酸(反应物)浓度越大,反应时间越短,反应速率越大 |
| D | 用已知浓度的高锰酸钾溶液滴定白葡萄酒中未知浓度的 ,滴定到终点时仰视读数 ,滴定到终点时仰视读数 | 测得白葡萄酒 浓度偏低 浓度偏低 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】在带有活塞的密闭容器中发生反应: ,采取下列措施不能改变反应速率的是( )
,采取下列措施不能改变反应速率的是( )
 ,采取下列措施不能改变反应速率的是( )
,采取下列措施不能改变反应速率的是( )A.增加 的量 的量 | B.保持容器体积不变,增加 的量 的量 |
C.充入 ,保持容器内压强不变 ,保持容器内压强不变 | D.充入 ,保持容器体积不变 ,保持容器体积不变 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐3】根据实验操作和现象,所得到的结论错误的是
| 实验操作和现象 | 结论 | |
| A | 相同温度,用pH传感器测定SO2和CO2饱和溶液的pH,后者pH大 | 酸性:H2SO3>H2CO3 |
| B | 向5mLFeCl3溶液中滴加10mL等浓度的KI溶液,充分反应后,再滴加KSCN溶液,溶液最终变为血红色 | FeCl3溶液与KI溶液的反应为可逆反应 |
| C | 取两支试管,分别加入2mL0.2mol/L的酸性KMnO4溶液,然后分别向两支试管中加入2mL0.6mol/L和1.2mol/L的H2C2O4溶液,后者完全褪色所需时间更短 | 其他条件相同时,增大反应物浓度反应速率增大 |
| D | 将装有NO2的球形容器浸入热水中,体系颜色变深 |   |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】有科研工作者研究发现,以负载Ce-Pt-Pd氧化处理后的不锈钢丝网具有较好的催化性能,可以消除VOCs(挥发性有机化合物,如苯、甲苯、丙酮等)、 的污染,如图所示简要表示了该催化过程及反应机理。有关说法错误的是
的污染,如图所示简要表示了该催化过程及反应机理。有关说法错误的是
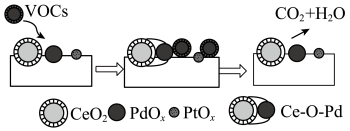
 的污染,如图所示简要表示了该催化过程及反应机理。有关说法错误的是
的污染,如图所示简要表示了该催化过程及反应机理。有关说法错误的是
| A.不锈钢丝网可增大催化剂与VOCs的接触面积 | B.氧气参与了上述催化反应 |
| C.碳原子在该催化反应中得电子 | D.该催化剂可用于机动车尾气的处理 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】在 作用下,CO与
作用下,CO与 发生如下两步基元反应,能量变化及反应历程如图所示。
发生如下两步基元反应,能量变化及反应历程如图所示。
① (慢);②
(慢);② (快)
(快)
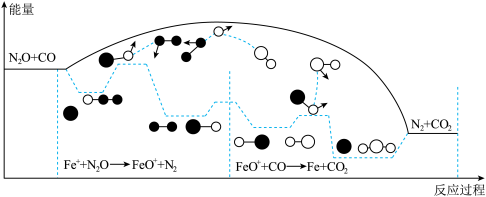
下列说法正确的是反应历程
 作用下,CO与
作用下,CO与 发生如下两步基元反应,能量变化及反应历程如图所示。
发生如下两步基元反应,能量变化及反应历程如图所示。①
 (慢);②
(慢);② (快)
(快)
下列说法正确的是反应历程
A. 改变反应历程,降低总反应的活化能,也改变了反应的 改变反应历程,降低总反应的活化能,也改变了反应的 |
B.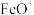 是中间产物,也作催化剂 是中间产物,也作催化剂 |
| C.总反应的化学反应速率由反应②决定 |
D.总反应中每转移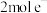 ,在标准状况下生成 ,在标准状况下生成 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐3】利用CO2与CH4制备合成气(CO、H2),可能的反应历程如图所示:
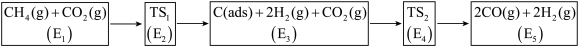
说明:
①C(ads)为吸附性活性炭,E表示方框中物质的总能量(单位:kJ•mol-1),TS表示过渡态.
②括号中为断开该化学键需要吸收的能量:C-H(413kJ•mol-1),C=O(745kJ•mol-1),CO中的化学键(1075kJ•mol-1),下列说法不正确的是
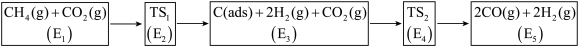
说明:
①C(ads)为吸附性活性炭,E表示方框中物质的总能量(单位:kJ•mol-1),TS表示过渡态.
②括号中为断开该化学键需要吸收的能量:C-H(413kJ•mol-1),C=O(745kJ•mol-1),CO中的化学键(1075kJ•mol-1),下列说法不正确的是
| A.若E3+E2<E4+E1,则决定速率步骤的化学方程式为CH4(g)=C(ads)+2H2(g) |
| B.制备合成气总反应的△H可表示为(E5-E1)kJ•mol-1 |
| C.若△H=+120kJ•mol-1,断开H-H需要吸收的能量为436kJ•mol-1 |
| D.使用催化剂后,CO和H2平衡产率不改变 |
您最近一年使用:0次