利用CO2与CH4制备合成气(CO、H2),可能的反应历程如图所示:
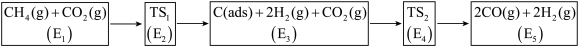
说明:
①C(ads)为吸附性活性炭,E表示方框中物质的总能量(单位:kJ•mol-1),TS表示过渡态.
②括号中为断开该化学键需要吸收的能量:C-H(413kJ•mol-1),C=O(745kJ•mol-1),CO中的化学键(1075kJ•mol-1),下列说法不正确的是
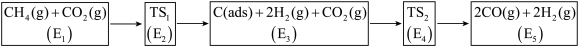
说明:
①C(ads)为吸附性活性炭,E表示方框中物质的总能量(单位:kJ•mol-1),TS表示过渡态.
②括号中为断开该化学键需要吸收的能量:C-H(413kJ•mol-1),C=O(745kJ•mol-1),CO中的化学键(1075kJ•mol-1),下列说法不正确的是
| A.若E3+E2<E4+E1,则决定速率步骤的化学方程式为CH4(g)=C(ads)+2H2(g) |
| B.制备合成气总反应的△H可表示为(E5-E1)kJ•mol-1 |
| C.若△H=+120kJ•mol-1,断开H-H需要吸收的能量为436kJ•mol-1 |
| D.使用催化剂后,CO和H2平衡产率不改变 |
更新时间:2022-12-16 14:22:32
|
相似题推荐
单选题
|
适中
(0.65)
【推荐1】分析下面的能量变化示意图,下列热化学方程式正确的是


| A.2A(g) + B(g) → 2C(g) - Q | B.2A(g) + B(g) → 2C(g) + Q |
| C.2A + B → 2C + Q | D.2C → 2A + B - Q |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】已知下列热化学方程式:
①Fe2O3(s)+3CO(g)=2Fe(s)+3CO2(g) ΔH1= -26.7kJ·mol-1
②3Fe2O3(s)+CO(g)=2Fe3O4(s)+CO2(g) ΔH2= -50.75kJ·mol-1
③Fe3O4(s)+CO(g)=3FeO(s)+CO2(g) ΔH3= -36.5 kJ·mol-1
则反应FeO(s)+CO(g)=Fe(s)+CO2(g)的焓变为
①Fe2O3(s)+3CO(g)=2Fe(s)+3CO2(g) ΔH1= -26.7kJ·mol-1
②3Fe2O3(s)+CO(g)=2Fe3O4(s)+CO2(g) ΔH2= -50.75kJ·mol-1
③Fe3O4(s)+CO(g)=3FeO(s)+CO2(g) ΔH3= -36.5 kJ·mol-1
则反应FeO(s)+CO(g)=Fe(s)+CO2(g)的焓变为
| A.+7.28kJ·mol-1 | B.−7.28kJ·mol-1 |
| C.+43.68kJ·mol-1 | D.−43.68kJ·mol-1 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】在25℃和101kPa条件下,断开1moH2(g)中的共价键要吸收436kJ的能量,断开1molCl2(g)中的共价键要吸收243kJ的能量,形成2molHCl(g)中的共价键要释放862kJ的能量。下列说法不正确的是
| A.断开1molHCl(g)中的共价键要吸收431kJ的能量 |
| B.2molH2(g)比1molH2(g)具有的能量低 |
| C.H2(g)+Cl2(g)=2HCl(g)为放热反应 |
| D.可将H2与Cl2的反应设计成原电池,既生产盐酸又回收电能 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】已知反应:
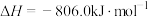 ,其他相关数据如下表:
,其他相关数据如下表:
下列说法正确的是

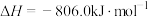 ,其他相关数据如下表:
,其他相关数据如下表:| 化学键 |  |  |  |  |
1 化学键断裂时吸收的能量/ 化学键断裂时吸收的能量/ | x | 498 | 803 | 464 |
| A.反应物的总能量小于生成物的总能量 |
B. 的燃烧热是806.0 的燃烧热是806.0 |
C. |
D.断开氧氧键形成1 氧原子需要放出能量249 氧原子需要放出能量249 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】铁的配合物离子(用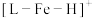 表示)催化某反应的一种反应机理和相对能量的变化情况如下图所示:
表示)催化某反应的一种反应机理和相对能量的变化情况如下图所示:
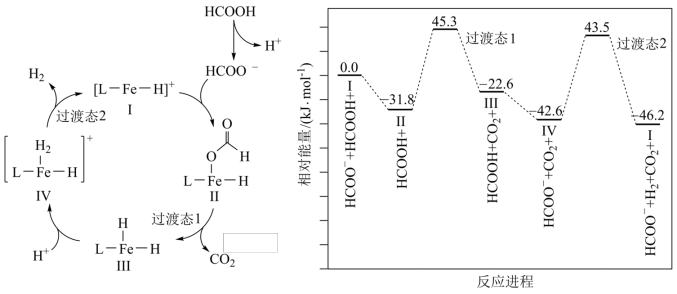
下列说法错误的是
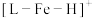 表示)催化某反应的一种反应机理和相对能量的变化情况如下图所示:
表示)催化某反应的一种反应机理和相对能量的变化情况如下图所示:
下列说法错误的是
A.该过程的热化学方程式为  |
B. 浓度过大或者过小,均导致反应速率降低 浓度过大或者过小,均导致反应速率降低 |
| C.加催化剂,可以提高该反应活化分子百分数,从而加快反应速率 |
| D.该过程的总反应速率由Ⅳ→Ⅰ步骤决定 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】对于某一化学反应,能使反应历程改变,降低化学反应的活化能,从而提高反应速率的条件是
| A.增大反应物浓度 | B.加压 | C.加催化剂 | D.升温 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐3】氟利昂是饱和碳氢化合物的卤族衍生物的总称,其破坏臭氧层的化学反应机理如下(以二氯二氟甲烷为例,二氯二氟甲烷可由四氯化碳与氟化氢在催化剂存在下、控制回流冷凝温度为﹣5℃时得到):
①CF2Cl2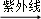 CF2Cl+Cl
CF2Cl+Cl
②Cl+O3→ClO+O2
③ClO+ClO→ClOOCl(过氧化氯)
④ClOOCl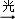 2Cl+O2
2Cl+O2
下列说法中不正确的是
①CF2Cl2
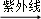 CF2Cl+Cl
CF2Cl+Cl②Cl+O3→ClO+O2
③ClO+ClO→ClOOCl(过氧化氯)
④ClOOCl
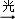 2Cl+O2
2Cl+O2下列说法中不正确的是
| A.紫外线使CF2Cl2分解产生的是臭氧生成氧气的催化剂 |
| B.反应③中的氯子与反应④中生成的氯原子化学性质相同 |
| C.ClOOCl分子中各原子最外层均达到8电子稳定结构 |
| D.气态氢化物的稳定性:HF>H2O>HCl |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】已知:A(g)+3B(g)⇌2C(g)。起始反应物为A和B,物质的量之比为1:3,且总物质的量不变,在不同压强和温度下,反应达到平衡时,体系中C的物质的量分数如下表:下列说法不正确的是( )
| 温度 物质的量分数 压强 | 400℃ | 450℃ | 500℃ | 600℃ |
| 20MPa | 0.387 | 0.274 | 0.189 | 0.088 |
| 30MPa | 0.478 | 0.359 | 0.260 | 0.129 |
| 40MPa | 0.549 | 0.429 | 0.322 | 0.169 |
| A.压强不变,降低温度,A的平衡转化率增大 |
| B.在不同温度下、压强下,平衡时C的物质的量分数可能相同 |
| C.达到平衡时,将C移出体系,正、逆反应速率均将减小 |
| D.为提高平衡时C的物质的量分数和缩短达到平衡的时间,可选择加入合适的催化剂 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】某温度下,体积一定的密闭容器中进行如下可逆反应:X(g)+Y(g)  Z(g)+W(s)(吸热反应);下列叙述正确的是
Z(g)+W(s)(吸热反应);下列叙述正确的是
 Z(g)+W(s)(吸热反应);下列叙述正确的是
Z(g)+W(s)(吸热反应);下列叙述正确的是| A.加入少量W,逆反应速率增大 |
| B.当容器中气体压强不变时,反应达到平衡 |
| C.升高温度,平衡逆向移动 |
| D.平衡后加入W,上述反应逆向移动 |
您最近一年使用:0次

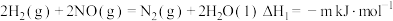 ;
; ;
;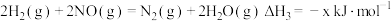 ﹔
﹔
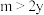
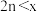
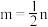


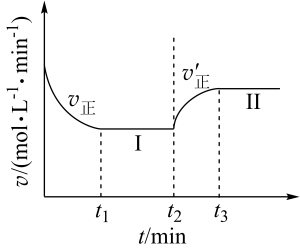
 3C(g)ΔH<0,向一恒温恒容的密闭容器中充入1molA和3molB发生反应,t1时达到平衡状态Ⅰ,在t2时改变某一条件,t3时重新达到平衡状态Ⅱ,正反应速率随时间的变化如图所示。下列说法正确的是
3C(g)ΔH<0,向一恒温恒容的密闭容器中充入1molA和3molB发生反应,t1时达到平衡状态Ⅰ,在t2时改变某一条件,t3时重新达到平衡状态Ⅱ,正反应速率随时间的变化如图所示。下列说法正确的是