下列叙述不正确的是
| A.物质发生化学变化一定会伴有能量的变化 |
| B.可逆反应的ΔH表示完全反应时的热量变化,与反应是否可逆无关 |
| C.水蒸气变为液态水时放出的能量就是该变化的反应热 |
| D.同温同压下,反应H2(g)+Cl2(g)═2HCl(g)在光照和点燃条件下的ΔH相同 |
更新时间:2023-10-06 16:28:25
|
相似题推荐
单选题
|
适中
(0.65)
【推荐1】一种制氢技术原理如图所示,下列说法错误的是
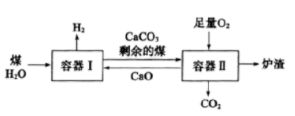

A.反应后向容器I中加入CaO能有效实现 与 与 的分离 的分离 |
B.因为容器I中还有剩余的煤,可以判断煤和 的反应为可逆反应 的反应为可逆反应 |
C.剩余的煤进入容器II,可利用其与 反应放出的热量来分解 反应放出的热量来分解 |
D.煤中含有的硫元素在容器II中最终转化为 进入炉渣 进入炉渣 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】N2与O2化合生成NO是自然界固氮的重要方式之一、如图显示了该反应中的能量变化,下列说法不正确的是


| A.N≡N键的键能很大,常温下N2性质较稳定 |
| B.完全断开1molNO中的化学键需吸收1264k能量 |
| C.该反应中产物所具有的总能量高于反应物所具有的总能量 |
| D.生成NO反应的热化学方程式为:N2(g)+O2(g)=2NO(g) △H=+180KJ/mol |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐3】1,3-丁二烯与HBr发生加成反应分两步:第一步H+进攻1,3-丁二烯生成碳正离子(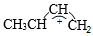 );第二步Br- 进攻碳正离子完成1,2-加成或 1,4-加成。反应进程中的能量变化如图所示。已知在0℃和40℃时,1,2-加成产物与1,4-加成产物的比例分别为70:30和15:85。下列说法正确的是
);第二步Br- 进攻碳正离子完成1,2-加成或 1,4-加成。反应进程中的能量变化如图所示。已知在0℃和40℃时,1,2-加成产物与1,4-加成产物的比例分别为70:30和15:85。下列说法正确的是
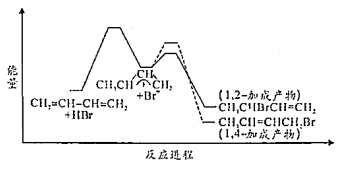
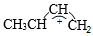 );第二步Br- 进攻碳正离子完成1,2-加成或 1,4-加成。反应进程中的能量变化如图所示。已知在0℃和40℃时,1,2-加成产物与1,4-加成产物的比例分别为70:30和15:85。下列说法正确的是
);第二步Br- 进攻碳正离子完成1,2-加成或 1,4-加成。反应进程中的能量变化如图所示。已知在0℃和40℃时,1,2-加成产物与1,4-加成产物的比例分别为70:30和15:85。下列说法正确的是
| A.1,2-加成产物比1,4-加成产物稳定 |
| B.与0℃相比,40℃时 1,3-丁二烯的平衡转化率增大 |
| C.从0℃升至40℃,1,4加成正反应速率增大,1,2加成正反应速率减小 |
| D.从0℃升至40°C,1,2加成正反应速率的增大程度小于其逆反应速率的增大程度 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐1】如图为反应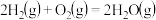 的能量变化示意图,下列说法正确的是
的能量变化示意图,下列说法正确的是

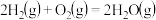 的能量变化示意图,下列说法正确的是
的能量变化示意图,下列说法正确的是 
A.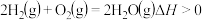 |
B.由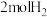 和 和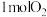 变成 变成 原子需要放出能量 原子需要放出能量 |
C. 和 和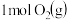 反应生成 反应生成 ,共放出 ,共放出 能量 能量 |
D.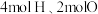 生成 生成 ,共放出 ,共放出 能量 能量 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】我国科学家在国际上首次实现二氧化碳到淀粉的全合成,对实现“碳中和”与“碳达峰”有重要意义,下列说法正确的是
| A.全合成过程一定包含能量的变化 |
| B.使用催化剂能提升全合成过程的平衡转化率 |
| C.以相同反应物合成淀粉,人工合成与自然合成两种途径反应热不相同 |
| D.全合成的第一步为吸热反应,则反应物的键能总和低于生成物的键能总和 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】一定温度下,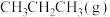 (用RH表示)的氯代和溴代反应能量图及产率关系如图(图中物质均为气态)。下列说法正确的是
(用RH表示)的氯代和溴代反应能量图及产率关系如图(图中物质均为气态)。下列说法正确的是
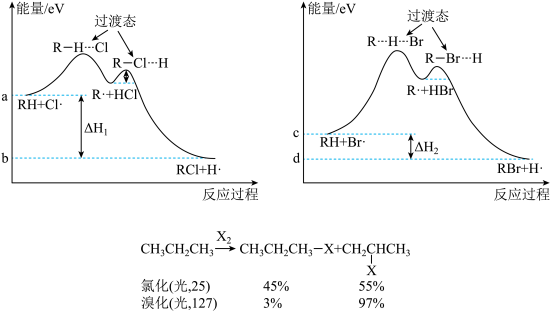
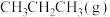 (用RH表示)的氯代和溴代反应能量图及产率关系如图(图中物质均为气态)。下列说法正确的是
(用RH表示)的氯代和溴代反应能量图及产率关系如图(图中物质均为气态)。下列说法正确的是
A. 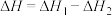 |
| B.氯代的第二步是决速反应 |
| C.以丙烷为原料制备2-丙醇时,应该选择溴代反应,然后再水解 |
D.据图像信息,可以计算 ( ( 表示键能) 表示键能) |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】下列说法正确的是
| A.在氧化还原反应中,还原剂失去电子放出的能量等于氧化剂得到电子的吸收的能量 |
| B.硝酸钾溶于水是吸热反应 |
C.相同条件下,等质量的碳按a、b两种途径完全转化,途径a与途径b放出相同的热能,途径a:C(s) CO(g)+H2(g) CO(g)+H2(g)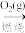 CO2(g)+H2O(g);途径b:C(s) CO2(g)+H2O(g);途径b:C(s) CO2(g) CO2(g) |
| D.2H2(g)+O2(g)=2H2O(g) ∆S1; 2H2(g)+O2(g)=2H2O(l) ∆S2;∆S1<∆S2 |
您最近一年使用:0次
【推荐3】通过以下反应均可获取H2。
① C(s) + H2O (g) =CO(g)+H2(g) ΔH1 = + 131.3 kJ·mol-1
② CH4 (g)+H2O(g) = CO(g)+3H2 (g) ΔH2 = + 206.1 kJ·mol-1
③ CO(g)+H2O(g) = CO2(g)+H2(g) ΔH3
下列说法正确的是
① C(s) + H2O (g) =CO(g)+H2(g) ΔH1 = + 131.3 kJ·mol-1
② CH4 (g)+H2O(g) = CO(g)+3H2 (g) ΔH2 = + 206.1 kJ·mol-1
③ CO(g)+H2O(g) = CO2(g)+H2(g) ΔH3
下列说法正确的是
| A.①中反应物的总能量大于生成物的总能量 |
| B.②中使用适当催化剂,可以使ΔH2减小 |
| C.由①、②计算反应CH4 (g) = C (s) + 2H2 (g) 的ΔH =-74.8 kJ·mol-1 |
| D.若知反应C (s) + CO2 (g) = 2CO (g) 的ΔH,结合ΔH1可计算出ΔH3 |
您最近一年使用:0次



