用文字阐述方法或原因
(1)比较K+和Cl-的半径大小并从原子结构的角度解释原因___________
(2)比较Na和Al的金属性强弱并从原子结构的角度解释原因___________
(1)比较K+和Cl-的半径大小并从原子结构的角度解释原因
(2)比较Na和Al的金属性强弱并从原子结构的角度解释原因
更新时间:2023-10-25 22:50:42
|
相似题推荐
填空题
|
容易
(0.94)
【推荐1】简要回答下列问题。
(1)钠原子失电子能力大于镁原子的原因是_______ 。
(2)将食品置于低温条件下,常常可以保存更长时间的原因是_______ 。
(3)盛有浓硫酸的容器敞口放置一段时间后,硫酸浓度变小的原因是_______ 。
(1)钠原子失电子能力大于镁原子的原因是
(2)将食品置于低温条件下,常常可以保存更长时间的原因是
(3)盛有浓硫酸的容器敞口放置一段时间后,硫酸浓度变小的原因是
您最近一年使用:0次
填空题
|
容易
(0.94)
【推荐2】比较下列元素的性质(用“>”、“<”表示)
(1)金属性:Li___________ Na、Mg___________ Ca、K___________ Ca
(2)非金属性:N___________ F、F___________ Cl、Si___________ P
(1)金属性:Li
(2)非金属性:N
您最近一年使用:0次
填空题
|
容易
(0.94)
名校
【推荐3】铯(Cs)元素的原子结构示意图如图所示,请据此回答以下问题:

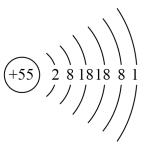
(1)铯在元素周期表中的位置是_______ 。
(2)从原子结构的角度比较并解释钠和铯元素的金属性强弱_______ 。


(1)铯在元素周期表中的位置是
(2)从原子结构的角度比较并解释钠和铯元素的金属性强弱
您最近一年使用:0次
填空题
|
容易
(0.94)
名校
【推荐1】下表列出了①~⑤五种元素在周期表中的位置:
按要求回答下列问题:
(1)元素⑥的最高正化合价是___________ 。
(2)元素⑤在周期表中的位置是___________ 。
(3)元素②和元素③的非金属性强弱关系是②___________ ③(选填“>”或“<”);表中所列六种元素的单质,常温下为有色气体的是___________ (填化学式)。
(4)①~⑥六种元素中原子半径最大 的是___________ (填元素符号)。②③两种元素的最简单氢化物中最稳定 的是___________ (填化学式)
(5)元素③与元素④能形成原子个数比为1:1的化合物 Y,Y 在常温下为固态,焰色反应为黄色,常用与呼吸面具中做供氧剂。写出Y与水反应的化学方程式:___________ 。
| 族 周期 | ⅠA | 0 | ||||||
| 1 | ① | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | |
| 2 | ② | ③ | ||||||
| 3 | ④ | ⑤ | ⑥ | |||||
按要求回答下列问题:
(1)元素⑥的最高正化合价是
(2)元素⑤在周期表中的位置是
(3)元素②和元素③的非金属性强弱关系是②
(4)①~⑥六种元素中原子半径
(5)元素③与元素④能形成原子个数比为1:1的化合物 Y,Y 在常温下为固态,焰色反应为黄色,常用与呼吸面具中做供氧剂。写出Y与水反应的化学方程式:
您最近一年使用:0次
填空题
|
容易
(0.94)
名校
解题方法
【推荐2】A、B、C、D、E、F为六种短周期主族元素原子序数依次增大。A、B能形成两种常温下均呈液态的化合物,C是短周期元素中原子半径最大的元素,D是地壳中含量最多的金属元素,B、E同主族。回答下列问题:
(1)F在元素周期表中的位置为___________
(2)B、C、D的离子半径由大到小的顺序为___________ (用离子符号表示)。
(3)由A分别和B、E、F所形成的三种化合物中,热稳定性最差的是___________ (填化学式)。
(4)B和C两元素形成的原子个数比为1:1的化合物的电子式为___________ ,该化合物所含的化学键类型为___________
(5)C的最高价氧化物对应的氢氧化物与D的最高价氧化物反应的离子方程式为:___________
(1)F在元素周期表中的位置为
(2)B、C、D的离子半径由大到小的顺序为
(3)由A分别和B、E、F所形成的三种化合物中,热稳定性最差的是
(4)B和C两元素形成的原子个数比为1:1的化合物的电子式为
(5)C的最高价氧化物对应的氢氧化物与D的最高价氧化物反应的离子方程式为:
您最近一年使用:0次



