Ⅰ.回答下列问题:
(1)在无土栽培中,配制1L内含0.5molNH4Cl、0.16molKCl、0.24molK2SO4的某营养液,若用KCl、NH4Cl、(NH4)2SO4配制,则需这三种固体的物质的量为________ 、_______ 、______ 。
(2)在反应X+2Y=R+2M中,已知R和M的摩尔质量之比为22:9,当1.6gX与Y完全反应后,生成4.4gR,则此反应中Y和M的质量之比为________ 。
(3)一种不纯的铁,已知它含有铜、铝、镁等一种或几种金属杂质,5.6g这样的铁跟足量的稀H2SO4作用,生成H22.24L(标准状况),则此铁块中一定含有的金属杂质是_______ 。
Ⅱ.实验室常用加热氯酸钾的方法制取少量氧气。
(4)请写出反应的化学方程式_______ 。
(5)现欲制取1.12L(标准状况)氧气,理论上需要消耗氯酸钾多少克?生成氯化钾物质的量多少?_______ 、________ 。
(1)在无土栽培中,配制1L内含0.5molNH4Cl、0.16molKCl、0.24molK2SO4的某营养液,若用KCl、NH4Cl、(NH4)2SO4配制,则需这三种固体的物质的量为
(2)在反应X+2Y=R+2M中,已知R和M的摩尔质量之比为22:9,当1.6gX与Y完全反应后,生成4.4gR,则此反应中Y和M的质量之比为
(3)一种不纯的铁,已知它含有铜、铝、镁等一种或几种金属杂质,5.6g这样的铁跟足量的稀H2SO4作用,生成H22.24L(标准状况),则此铁块中一定含有的金属杂质是
Ⅱ.实验室常用加热氯酸钾的方法制取少量氧气。
(4)请写出反应的化学方程式
(5)现欲制取1.12L(标准状况)氧气,理论上需要消耗氯酸钾多少克?生成氯化钾物质的量多少?
更新时间:2023-10-27 17:28:33
|
相似题推荐
计算题
|
适中
(0.65)
名校
【推荐1】回答下列问题。
(1)现有下列物质:①CO2 ②液态氯化氢 ③CH4 ④熔融NaOH ⑤NH4Cl固体 ⑥氨水
请用序号回答下列问题:能导电的是___ 。属于电解质的是___ 。属于非电解质的是___ 。
(2)K2SO4和Fe2(SO4)3的混合溶液,已知其中Fe3+的浓度为0.5mol/L,SO42-浓度为0.9mol/L,则K+的物质的量浓度为___ mol/L。
(3)1.204×1024个H2SO4分子的物质的量为___ mol,共含___ 个氢原子。将上述H2SO4溶于水配成600mL溶液,再加水稀释到1000mL,稀释后溶液的物质的量浓度为___ mol/L。
(4)15.6gNa2R2中含0.4mol的Na+,则R的相对原子质量是___ 。
(1)现有下列物质:①CO2 ②液态氯化氢 ③CH4 ④熔融NaOH ⑤NH4Cl固体 ⑥氨水
请用序号回答下列问题:能导电的是
(2)K2SO4和Fe2(SO4)3的混合溶液,已知其中Fe3+的浓度为0.5mol/L,SO42-浓度为0.9mol/L,则K+的物质的量浓度为
(3)1.204×1024个H2SO4分子的物质的量为
(4)15.6gNa2R2中含0.4mol的Na+,则R的相对原子质量是
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
解题方法
【推荐2】阿伏加 德罗常数的近似值为6.02×1023。按要求完成下列填空:
(1)1molCl2中约含有___ 个氯气分子,约含有__ 个氯原子。含有6.02×1023个氢原子的H2SO4的物质的量是___ ;
(2)某硫酸钠溶液中含有3.01×1023个Na+,则该溶液中SO42-的物质的量是___ 。
(3)2L1mol/LMgCl2中镁离子的物质的量为___ ,Cl-的物质的量浓度为___ 。
(4)三种盐的混合溶液中含有0.2molNa+、0.25molMg2+、0.4molCl-、SO42-,则SO42-的微粒个数约为___ 。
(1)1molCl2中约含有
(2)某硫酸钠溶液中含有3.01×1023个Na+,则该溶液中SO42-的物质的量是
(3)2L1mol/LMgCl2中镁离子的物质的量为
(4)三种盐的混合溶液中含有0.2molNa+、0.25molMg2+、0.4molCl-、SO42-,则SO42-的微粒个数约为
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
解题方法
【推荐1】完成下列有关物质的量的计算
(1) 个
个 分子的物质的量是
分子的物质的量是________  。
。
(2)标准状况下, 的体积是
的体积是_________ L。
(3)含有相同氧原子数的 和
和 ,其分子的质量比为
,其分子的质量比为_________ 。
(4)标准状况下, 气体溶于水配制成
气体溶于水配制成 溶液,其物质的量浓度为
溶液,其物质的量浓度为_______  。
。
(5)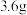 碳在一定量的氧气中完全燃烧,反应后生成
碳在一定量的氧气中完全燃烧,反应后生成 和
和 混合气体的平均摩尔质量是
混合气体的平均摩尔质量是 ,则生成的
,则生成的 的质量是
的质量是_____  。
。
(1)
 个
个 分子的物质的量是
分子的物质的量是 。
。(2)标准状况下,
 的体积是
的体积是(3)含有相同氧原子数的
 和
和 ,其分子的质量比为
,其分子的质量比为(4)标准状况下,
 气体溶于水配制成
气体溶于水配制成 溶液,其物质的量浓度为
溶液,其物质的量浓度为 。
。(5)
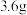 碳在一定量的氧气中完全燃烧,反应后生成
碳在一定量的氧气中完全燃烧,反应后生成 和
和 混合气体的平均摩尔质量是
混合气体的平均摩尔质量是 ,则生成的
,则生成的 的质量是
的质量是 。
。
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
【推荐2】(1)9g水与_______ g硫酸所含的分子数相等,它们所含氧原子数之比是_______ ,氢原子数之比是_______ ;
(2)已知8gA能与32gB恰好完全反应,生成22gC和一定量的D,现将16gA与70gB的混合物充分反应后,生成2molD和一定量的C,则D的摩尔质量是_______ g/mol;
(2)已知8gA能与32gB恰好完全反应,生成22gC和一定量的D,现将16gA与70gB的混合物充分反应后,生成2molD和一定量的C,则D的摩尔质量是
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐3】根据要求回答下列问题。
(1)相同质量的SO2气体和SO3气体,其分子数之比为_____ ,氧原子数之比为_____ ,相同条件下(同温同压)的体积之比为_____ ,密度之比为_____ 。
(2)SO2与O2的混合气体中,氧元素的质量分数为70%,则SO2与O2的物质的量之比是_____ ,这种混合气体的密度是同温同压下氧气密度的_____ 倍。
(3)用2.4 mol·L-1的H2SO4溶液配制100 mL浓度为0.2 mol·L-1的稀硫酸,需量取2.4 mol·L-1的H2SO4溶液的体积是_____ mL。
(4)试分析下列操作对所配溶液的浓度有何影响(填“偏高”“偏低”或“无影响”)。
①未洗涤烧杯和玻璃棒,使所配溶液浓度_____ ;
②定容时俯视刻度线,使所配溶液浓度_____ ;
③摇匀后,发现液面低于刻度线,又滴加蒸馏水,使所配溶液浓度_____ 。
(1)相同质量的SO2气体和SO3气体,其分子数之比为
(2)SO2与O2的混合气体中,氧元素的质量分数为70%,则SO2与O2的物质的量之比是
(3)用2.4 mol·L-1的H2SO4溶液配制100 mL浓度为0.2 mol·L-1的稀硫酸,需量取2.4 mol·L-1的H2SO4溶液的体积是
(4)试分析下列操作对所配溶液的浓度有何影响(填“偏高”“偏低”或“无影响”)。
①未洗涤烧杯和玻璃棒,使所配溶液浓度
②定容时俯视刻度线,使所配溶液浓度
③摇匀后,发现液面低于刻度线,又滴加蒸馏水,使所配溶液浓度
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐1】根据所学知识,回答下列问题:
(1)同温同压下,同体积的气体甲烷(CH4)和二氧化碳的密度之比为___________ 。
(2)在Na2SO4和Fe(SO4)3的混合溶液中,Na+的物质的量浓度为0.1 mol/L, 的物质的量浓度为0.5 mol/L,则混合溶液中Fe3+的物质的量浓度为
的物质的量浓度为0.5 mol/L,则混合溶液中Fe3+的物质的量浓度为___________ mol/L。
(3)实验室将11.7 g氯化钠溶于水配制成500 mL溶液,取出50 mL该溶液,取出的溶液中n(Cl-)=___________ mol,c(Na+)=___________ mol/L。
(4)已知反应: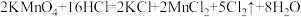 。若产生的Cl2在标准状况下的体积为5.6 L,则反应中被氧化的HCl的物质的量为
。若产生的Cl2在标准状况下的体积为5.6 L,则反应中被氧化的HCl的物质的量为___________ mol。
(1)同温同压下,同体积的气体甲烷(CH4)和二氧化碳的密度之比为
(2)在Na2SO4和Fe(SO4)3的混合溶液中,Na+的物质的量浓度为0.1 mol/L,
 的物质的量浓度为0.5 mol/L,则混合溶液中Fe3+的物质的量浓度为
的物质的量浓度为0.5 mol/L,则混合溶液中Fe3+的物质的量浓度为(3)实验室将11.7 g氯化钠溶于水配制成500 mL溶液,取出50 mL该溶液,取出的溶液中n(Cl-)=
(4)已知反应:
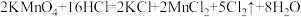 。若产生的Cl2在标准状况下的体积为5.6 L,则反应中被氧化的HCl的物质的量为
。若产生的Cl2在标准状况下的体积为5.6 L,则反应中被氧化的HCl的物质的量为
您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐2】在标准状况下进行甲、乙、丙三组实验。三组实验各取同浓度的盐酸30mL,加入同一种镁铝合金粉末,产生气体。有关数据列表如下(气体体积均为标准状况下测得):
(1)乙组实验中,盐酸_____________ (填“过量”、“适量”或“不足量”),理由是_________ 。
(2)要计算盐酸的物质的量浓度,题中可做计算依据的是____ 。
(3)合金中Mg、Al的物质的量之比为_________________ 。
(4)在丙组实验后,向容器中加入1mol/L的NaOH溶液,能使合金中的铝恰好溶解,不形成铝的沉淀,并使Mg2+刚好沉淀完全,求所加NaOH溶液的体积。(写出计算过程)_____________
| 实验序号 | 甲 | 乙 | 丙 |
| 合金质量/mg | 255 | 385 | 459 |
| 气体体积/mL | 280 | 336 | 336 |
(1)乙组实验中,盐酸
(2)要计算盐酸的物质的量浓度,题中可做计算依据的是
(3)合金中Mg、Al的物质的量之比为
(4)在丙组实验后,向容器中加入1mol/L的NaOH溶液,能使合金中的铝恰好溶解,不形成铝的沉淀,并使Mg2+刚好沉淀完全,求所加NaOH溶液的体积。(写出计算过程)
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐3】1774年,瑞典化学家舍勒发现软锰矿(主要成分是MnO2)和浓盐酸混合加热能制取氯气:MnO2+4HCl(浓) MnCl2+Cl2↑+2H2O。现将23.2g含MnO2的质量分数为75%的软锰矿石与足量10mol/L浓盐酸完全反应(杂质不参加反应)。把反应后所得溶液稀释成200ml。计算:
MnCl2+Cl2↑+2H2O。现将23.2g含MnO2的质量分数为75%的软锰矿石与足量10mol/L浓盐酸完全反应(杂质不参加反应)。把反应后所得溶液稀释成200ml。计算:
(1)生成的Cl2的体积(标准状况)____________ 。
(2)参加反应的浓盐酸的体积____________ 。
(3)稀释后溶液中MnCl2的物质的量浓度___________ 。
 MnCl2+Cl2↑+2H2O。现将23.2g含MnO2的质量分数为75%的软锰矿石与足量10mol/L浓盐酸完全反应(杂质不参加反应)。把反应后所得溶液稀释成200ml。计算:
MnCl2+Cl2↑+2H2O。现将23.2g含MnO2的质量分数为75%的软锰矿石与足量10mol/L浓盐酸完全反应(杂质不参加反应)。把反应后所得溶液稀释成200ml。计算:(1)生成的Cl2的体积(标准状况)
(2)参加反应的浓盐酸的体积
(3)稀释后溶液中MnCl2的物质的量浓度
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
解题方法
【推荐1】兴趣小组用莫尔盐[化学式为(NH4)mFe(SO4)2·6H2O(Fe为+2价)]测定KMnO4溶液的物质的量浓度的过程如下:
①称取19.6g莫尔盐配成100mL溶液。
②量取10.00mL KMnO4溶液,向其中加入足量的H2SO4进行酸化,向酸化后的溶液中逐滴滴加莫尔盐溶液,反应完全时消耗莫尔盐溶液的体积20.00mL,所发生反应的离子方程式如下:Fe2++MnO +H+→Fe3++Mn2++H2O(未配平)请回答下列问题:
+H+→Fe3++Mn2++H2O(未配平)请回答下列问题:
(1)莫尔盐(NH4)mFe(SO4)2·6H2O中m=___________ 。
(2)上述20.00mL莫尔盐溶液中 c(Fe2+)=___________ 。
(3)计算KMnO4溶液的物质的量浓度(写出计算过程)________ 。
①称取19.6g莫尔盐配成100mL溶液。
②量取10.00mL KMnO4溶液,向其中加入足量的H2SO4进行酸化,向酸化后的溶液中逐滴滴加莫尔盐溶液,反应完全时消耗莫尔盐溶液的体积20.00mL,所发生反应的离子方程式如下:Fe2++MnO
 +H+→Fe3++Mn2++H2O(未配平)请回答下列问题:
+H+→Fe3++Mn2++H2O(未配平)请回答下列问题:(1)莫尔盐(NH4)mFe(SO4)2·6H2O中m=
(2)上述20.00mL莫尔盐溶液中 c(Fe2+)=
(3)计算KMnO4溶液的物质的量浓度(写出计算过程)
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐2】工业生产粗硅的反应有:
SiO2+2C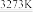 Si(粗)+2CO↑;SiO2+3C
Si(粗)+2CO↑;SiO2+3C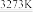 SiC+2CO↑。
SiC+2CO↑。
(1)若产品中粗硅与碳化硅的物质的量之比为1∶1,则参加反应的C 和SiO2的质量比为_____________ 。
(2)粗硅进一步制备纯硅的原理如下:
Si(粗)+2Cl2(g) SiCl4(l); SiCl4+2H2
SiCl4(l); SiCl4+2H2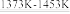 Si(纯)+4HCl。
Si(纯)+4HCl。
若上述反应中Si(粗)和SiCl4的利用率均为80%,制粗硅时有10%的SiO2转化为SiC,则生产25.2吨纯硅需纯度为75%石英砂_______________ 吨。
(3)工业上还可以通过如下图所示的流程制取纯硅:
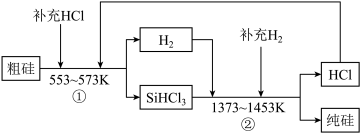
若反应①为:Si(粗)+3HCl(g)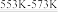 SiHCl3(l)+H2(g);
SiHCl3(l)+H2(g);
则反应②的化学方程式为____________________________ 。
假设每一轮次生产过程中,硅元素没有损失,反应①中HCl的利用率为α1,反应②中H2的利用率为α2,,若制备1mol纯硅,在第二轮次的生产中,现补充投入HCl和H2的物质的量之比是5∶1。则α1与α2的代数关系式为____________________ 。
SiO2+2C
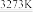 Si(粗)+2CO↑;SiO2+3C
Si(粗)+2CO↑;SiO2+3C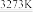 SiC+2CO↑。
SiC+2CO↑。(1)若产品中粗硅与碳化硅的物质的量之比为1∶1,则参加反应的C 和SiO2的质量比为
(2)粗硅进一步制备纯硅的原理如下:
Si(粗)+2Cl2(g)
 SiCl4(l); SiCl4+2H2
SiCl4(l); SiCl4+2H2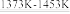 Si(纯)+4HCl。
Si(纯)+4HCl。若上述反应中Si(粗)和SiCl4的利用率均为80%,制粗硅时有10%的SiO2转化为SiC,则生产25.2吨纯硅需纯度为75%石英砂
(3)工业上还可以通过如下图所示的流程制取纯硅:

若反应①为:Si(粗)+3HCl(g)
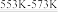 SiHCl3(l)+H2(g);
SiHCl3(l)+H2(g);则反应②的化学方程式为
假设每一轮次生产过程中,硅元素没有损失,反应①中HCl的利用率为α1,反应②中H2的利用率为α2,,若制备1mol纯硅,在第二轮次的生产中,现补充投入HCl和H2的物质的量之比是5∶1。则α1与α2的代数关系式为
您最近一年使用:0次



