原子序数由小到大排列的四种短周期元素X、Y、Z、W,四种元素的原子序数之和为32,在周期表中X是原子半径最小的元素,Y、Z左右相邻,Z、W位于同主族。
(1)X元素符号是____________ ;
(2)Z、W形成的气态氢化物的稳定性_______ >_______ (写化学式)。
(3)由X、Y、Z、W四种元素中的三种组成的一种强酸,该强酸的稀溶液能与铜反应,离子方程式为___________ 。
(4)由X、Y、Z、W四种元素组成的一种离子化合物A,已知①1mol A能与足量NaOH浓溶液反应生成标准状况下44.8L气体。②A能与盐酸反应产生气体,该气体能与氯水反应,写出该气体与氯水反应的离子方程式_____________________ 。
(5)由X、Y、Z、W和Fe五种元素组成的相对分子质量为392的化合物B,lmolB中含有6mol结晶水。对化合物B进行如下实验:
A.取B的溶液加入过量浓NaOH溶液并加热,产生白色沉淀和无色刺激性气味气体;过一段时间白色沉淀变为灰绿色,最终变为红褐色。
B.另取B的溶液,加入过量BaCl2溶液产生白色沉淀,加盐酸沉淀不溶解。
①由实验a、b推知B溶液中含有的离子为__________________ ;
②B的化学式为_________________ 。
(1)X元素符号是
(2)Z、W形成的气态氢化物的稳定性
(3)由X、Y、Z、W四种元素中的三种组成的一种强酸,该强酸的稀溶液能与铜反应,离子方程式为
(4)由X、Y、Z、W四种元素组成的一种离子化合物A,已知①1mol A能与足量NaOH浓溶液反应生成标准状况下44.8L气体。②A能与盐酸反应产生气体,该气体能与氯水反应,写出该气体与氯水反应的离子方程式
(5)由X、Y、Z、W和Fe五种元素组成的相对分子质量为392的化合物B,lmolB中含有6mol结晶水。对化合物B进行如下实验:
A.取B的溶液加入过量浓NaOH溶液并加热,产生白色沉淀和无色刺激性气味气体;过一段时间白色沉淀变为灰绿色,最终变为红褐色。
B.另取B的溶液,加入过量BaCl2溶液产生白色沉淀,加盐酸沉淀不溶解。
①由实验a、b推知B溶液中含有的离子为
②B的化学式为
11-12高三上·福建·期中 查看更多[2]
更新时间:2016-12-09 05:57:15
|
相似题推荐
解答题-无机推断题
|
适中
(0.65)
【推荐1】下表为元素周期表的一部分,请参照元素①~⑥在表中的位置,用化学用语 回答下列问题。

(1)元素①的原子结构示意图为_______ 。
(2)元素③和⑥可形成化合物,用电子式表示形成其过程_______ 。
(3)元素②、③形成简单离子的半径(填离子符号)_______ >_______ 。
(4)元素②、⑥形成的气态氢化物稳定性(填化学式,下同)_______ >_______ ;元素③、④形成的最高价氧化物水化物的碱性_______ >_______ 。
(5)元素④的最高价氧化物与元素⑤最高价氧化物的水化物稀溶液反应的离子方程式_______ 。
(6)元素①的最高价氧化物的水化物与元素③最高价氧化物的水化物稀溶液反应的离子方程式_______

(1)元素①的原子结构示意图为
(2)元素③和⑥可形成化合物,用电子式表示形成其过程
(3)元素②、③形成简单离子的半径(填离子符号)
(4)元素②、⑥形成的气态氢化物稳定性(填化学式,下同)
(5)元素④的最高价氧化物与元素⑤最高价氧化物的水化物稀溶液反应的离子方程式
(6)元素①的最高价氧化物的水化物与元素③最高价氧化物的水化物稀溶液反应的离子方程式
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐2】A、B、C、D、E都是短周期元素,原子序数依次增大,B、C同周期,A、D同主族。A、B能形成两种常温下的液态化合物甲和乙,原子个数比分别为2∶1和1∶1。根据以上信息回答下列问题:
(1)甲、乙两分子中含有非极性共价键的物质的电子式是________ ,C元素在周期表中的位置是_____ 。
(2)C和D的离子中,半径较小的是____ (离子符号),以上元素中电负性最大的是____ (元素符号)
(3)常温下将D的单质投入甲中,待D消失后再向上述溶液中加入E的固体单质,此时发生反应的化学方程式是______________ 。
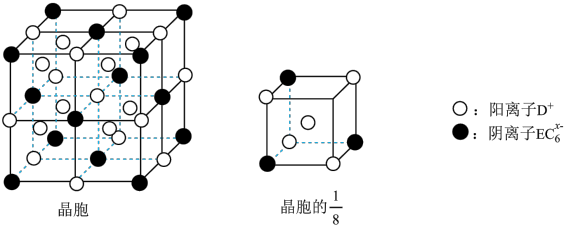
(4)C、D、E可组成离子化合物DxEC6,其晶胞(晶胞是在晶体中具有代表性的最小重复单元)结构如下图所示,阳离子D+(用○表示)位于正方体的棱的中点和正方体内部;阴离子EC6x-(用●表示)位于该正方体的顶点和面心。该化合物的化学式是_________ 。
(1)甲、乙两分子中含有非极性共价键的物质的电子式是
(2)C和D的离子中,半径较小的是
(3)常温下将D的单质投入甲中,待D消失后再向上述溶液中加入E的固体单质,此时发生反应的化学方程式是
(4)C、D、E可组成离子化合物DxEC6,其晶胞(晶胞是在晶体中具有代表性的最小重复单元)结构如下图所示,阳离子D+(用○表示)位于正方体的棱的中点和正方体内部;阴离子EC6x-(用●表示)位于该正方体的顶点和面心。该化合物的化学式是

您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐3】X、Y、Z、W、R 是原子序数依次增大的短周期主族元素 ,元素X 与其它四种元素不在同一周期,但X 与Z 元素在同一主族;W单质常用来制造信号弹和焰火,且W 原子核外电子总数是Y 的2倍,R 元素在同周期中原子半径最小.回答下列问题:
(1)X的元素符号为______ ,Y 元素在周期表中位置是_______ 。
(2)YR4的结构式为__________ 。
(3)R单质与Z的最高价氧化物对应水化物反应的离子方程式为_______ 。
(4)金属性强弱:W_____ Z ( 填“> ”或“< ”), 请设计一个简单的实验方案加以验证:__________ 。
(1)X的元素符号为
(2)YR4的结构式为
(3)R单质与Z的最高价氧化物对应水化物反应的离子方程式为
(4)金属性强弱:W
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐1】现有原子序数之和为51的5种短周期元素A,B,C,D,E。已知A的单质在常温下为无色气体;B原子的最外层电子数比次外层电子数多3个;C和B属于同一主族;D的最高正价与负价的代数和为4,其最高价氧化物对应的水化物的酸性在同主族元素中最强,E元素最外层电子数与其K层电子数相同。
(1)试写出它们的元素符号。__________________________________________ 。
(2)写出B的氢化物的电子式_____________________________ 。
(3)由A、D两种元素形成的化合物是________ 化合物(填“离子”或“共价”),化合物内存在________ 键(填“离子”或“共价”)。
(4)由D、E两种元素形成的化合物的电子式为________ ,它属于________ 化合物,化合物内存在________ 键。
(5)下列关于A,B,C,D,E 5种元素形成的物质的有关叙述正确的是________ (多选)。
a.A,B,C,D都能通过共价键形成单质,其中B形成的单质性质最稳定,是因为其原子半径最小
b.A,B,D 3种元素为非金属元素,它们共同组成的化合物一定是共价化合物
c.B,E形成的化合物E3B2应为离子化合物
d.5种元素两两组合形成的化合物中既有共价化合物,又有离子化合物
e.5种元素形成简单离子的离子半径大小为C>D>B>E>A
(1)试写出它们的元素符号。
(2)写出B的氢化物的电子式
(3)由A、D两种元素形成的化合物是
(4)由D、E两种元素形成的化合物的电子式为
(5)下列关于A,B,C,D,E 5种元素形成的物质的有关叙述正确的是
a.A,B,C,D都能通过共价键形成单质,其中B形成的单质性质最稳定,是因为其原子半径最小
b.A,B,D 3种元素为非金属元素,它们共同组成的化合物一定是共价化合物
c.B,E形成的化合物E3B2应为离子化合物
d.5种元素两两组合形成的化合物中既有共价化合物,又有离子化合物
e.5种元素形成简单离子的离子半径大小为C>D>B>E>A
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
【推荐2】随原子序数递增,八种短周期元素(用字母x等表示)原子半径的相对大小、最高正价或最低负价的变化如下图所示。
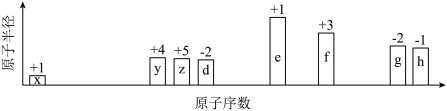
根据判断出的元素回答问题:
(1)写出化合物y2x2的电子式_________ (用相应的元素符号表示,下同)。
(2)写出z的最高价氧化物的水化物与其气态氢化物形成的盐的化学式为______ 。
(3)上述元素可组成盐R: egyz。盐R中z的化合价为_____ 价;写出盐R的名称_______ 。
(4)写出e的单质在足量d2中燃烧后的产物与y的最高价氧化物反应的化学方程式:_____________ 。
(5)写出分别由x、d、e、g四种元素组成的两种物质间发生反应的离子方程式为____________________ 。

根据判断出的元素回答问题:
(1)写出化合物y2x2的电子式
(2)写出z的最高价氧化物的水化物与其气态氢化物形成的盐的化学式为
(3)上述元素可组成盐R: egyz。盐R中z的化合价为
(4)写出e的单质在足量d2中燃烧后的产物与y的最高价氧化物反应的化学方程式:
(5)写出分别由x、d、e、g四种元素组成的两种物质间发生反应的离子方程式为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
【推荐3】A、B、C、D、E为短周期元素,A-E原子序数依次增大,质子数之和为40,B、C同周期,A、D同主族,A、C能形成两种液态化合物A2C和A2C2,E是地壳中含量最多的金属元素。
(1)E元素在周期表中的位置为__________ ;B、C的氢化物稳定性强的是________ (用化学式表示,下同);B、C、D组成的化合物中含有的化学键为_____________
(2)D2C2的电子式是_________ ,将D的单质投入A2C中,反应后得到一种无色溶液,E的单质在该无色溶液中反应的离子方程式为______________ ;
(3)元素D的单质在一定条件下,能与A单质化合生成氢化物DA,熔点为800℃。DA能与水反应放出氢气,化学反应方程式为_____________ 。
(4)废印刷电路版上含有铜,以往的回收方法是将其灼烧使铜转化为氧化铜,再用硫酸溶解。现改用A2C2和稀硫酸浸泡既达到了上述目的,又保护了环境,试写出反应的化学方程式__________________________
(1)E元素在周期表中的位置为
(2)D2C2的电子式是
(3)元素D的单质在一定条件下,能与A单质化合生成氢化物DA,熔点为800℃。DA能与水反应放出氢气,化学反应方程式为
(4)废印刷电路版上含有铜,以往的回收方法是将其灼烧使铜转化为氧化铜,再用硫酸溶解。现改用A2C2和稀硫酸浸泡既达到了上述目的,又保护了环境,试写出反应的化学方程式
您最近一年使用:0次



