现有原子序数之和为51的5种短周期元素A,B,C,D,E。已知A的单质在常温下为无色气体;B原子的最外层电子数比次外层电子数多3个;C和B属于同一主族;D的最高正价与负价的代数和为4,其最高价氧化物对应的水化物的酸性在同主族元素中最强,E元素最外层电子数与其K层电子数相同。
(1)试写出它们的元素符号。__________________________________________ 。
(2)写出B的氢化物的电子式_____________________________ 。
(3)由A、D两种元素形成的化合物是________ 化合物(填“离子”或“共价”),化合物内存在________ 键(填“离子”或“共价”)。
(4)由D、E两种元素形成的化合物的电子式为________ ,它属于________ 化合物,化合物内存在________ 键。
(5)下列关于A,B,C,D,E 5种元素形成的物质的有关叙述正确的是________ (多选)。
a.A,B,C,D都能通过共价键形成单质,其中B形成的单质性质最稳定,是因为其原子半径最小
b.A,B,D 3种元素为非金属元素,它们共同组成的化合物一定是共价化合物
c.B,E形成的化合物E3B2应为离子化合物
d.5种元素两两组合形成的化合物中既有共价化合物,又有离子化合物
e.5种元素形成简单离子的离子半径大小为C>D>B>E>A
(1)试写出它们的元素符号。
(2)写出B的氢化物的电子式
(3)由A、D两种元素形成的化合物是
(4)由D、E两种元素形成的化合物的电子式为
(5)下列关于A,B,C,D,E 5种元素形成的物质的有关叙述正确的是
a.A,B,C,D都能通过共价键形成单质,其中B形成的单质性质最稳定,是因为其原子半径最小
b.A,B,D 3种元素为非金属元素,它们共同组成的化合物一定是共价化合物
c.B,E形成的化合物E3B2应为离子化合物
d.5种元素两两组合形成的化合物中既有共价化合物,又有离子化合物
e.5种元素形成简单离子的离子半径大小为C>D>B>E>A
更新时间:2018-12-22 22:15:25
|
相似题推荐
解答题-无机推断题
|
适中
(0.65)
【推荐1】如表是元素周期表的一部分,①~⑧代表对应的元素。

回答下列问题:
(1)①的一种核素的中子数为2,该核素的符号为_____ 。
(2)③在元素周期表中的位置是_____ ;⑧的原子结构示意图为_____ 。
(3)写出②的最高价氧化物的结构式_____ 。
(4)④和⑦的简单氢化物沸点更高的是_____ (填序号)。
(5)写出⑧的单质与⑤最高价氧化物对应水化物在常温下反应的离子方程式_____ 。
(6)设计实验比较⑤和⑥的金属性强弱______ 。

回答下列问题:
(1)①的一种核素的中子数为2,该核素的符号为
(2)③在元素周期表中的位置是
(3)写出②的最高价氧化物的结构式
(4)④和⑦的简单氢化物沸点更高的是
(5)写出⑧的单质与⑤最高价氧化物对应水化物在常温下反应的离子方程式
(6)设计实验比较⑤和⑥的金属性强弱
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
【推荐2】A、B、W、D、E为短周期元素,且原子序数依次增大,质子数之和为39,B、W同周期,A、D同主族,A、W能形成两种液态化合物A2W和A2W2,E 元素的周期序数与主族序数相等。
(1)E 元素在周期表中的位置___________ 。
(2)写出A2W2的电子式为____________ 。
(3)废印刷电路板上含有铜,以往的回收方法是将其灼烧使铜转化为氧化铜,再用硫酸溶解。现改用A2W2和稀硫酸浸泡废印刷电路板既达到上述目的,又保护了环境,试写出反应的离子方程式________ 。
(4)元素D的单质在一定条件下,能与 A 单质化合生成一种化合物DA,熔点为800℃,DA能与水反应放氢气,若将1molDA和1molE 单质混合加入足量的水,充分反应后成气体的体积是_________ (标准状况下)。
(5)D的某化合物呈淡黄色,可与氯化亚铁溶液反应。若淡黄色固体与氯化亚铁反应的物质的量之比为1:2,且无气体生成,则该反应的离子方程式为_____________ 。
(1)E 元素在周期表中的位置
(2)写出A2W2的电子式为
(3)废印刷电路板上含有铜,以往的回收方法是将其灼烧使铜转化为氧化铜,再用硫酸溶解。现改用A2W2和稀硫酸浸泡废印刷电路板既达到上述目的,又保护了环境,试写出反应的离子方程式
(4)元素D的单质在一定条件下,能与 A 单质化合生成一种化合物DA,熔点为800℃,DA能与水反应放氢气,若将1molDA和1molE 单质混合加入足量的水,充分反应后成气体的体积是
(5)D的某化合物呈淡黄色,可与氯化亚铁溶液反应。若淡黄色固体与氯化亚铁反应的物质的量之比为1:2,且无气体生成,则该反应的离子方程式为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
【推荐3】X、Y、Z、W、Q是原子序数依次增大的短周期主族元素,X、W在周期表中的相对位置如下表;X元素最低负化合价的绝对值与其原子最外层电子数相等;Z是地壳中含量最多的金属元素。
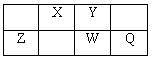
(1)元素Q在周期表中位于第_____ 族,Z的离子结构示意图为_____ 。
(2)Z、W、Q的原子半径由大到小的顺序为___________ 。(用元素符号表示其原子)。
(3)X和氢组成的化合物分子中有6个原子,其结构简式为______ ,写出该物质与水加成的化学方程式________________ 。
(4)Y的最简单气态氢化物甲的水溶液显碱性
①用电离方程式表示氢化物甲的水溶液中的显碱性的原因___________ ,
②在微电子工业中,甲的水溶液可作刻蚀剂H2O2的清除剂,所发生反应的产物不污染环境,其化学方程式为_______________________ 。该反应的氧化剂是____________ 当有1mol甲参加反应时,电子转移_____ mol。
(5)Q和Y形成的一种二元化合物具有色温效应,其相对分子质量在170~190之间,且Q的质量分数约为69.6%,则该化合物的分子式为_______ 。

(1)元素Q在周期表中位于第
(2)Z、W、Q的原子半径由大到小的顺序为
(3)X和氢组成的化合物分子中有6个原子,其结构简式为
(4)Y的最简单气态氢化物甲的水溶液显碱性
①用电离方程式表示氢化物甲的水溶液中的显碱性的原因
②在微电子工业中,甲的水溶液可作刻蚀剂H2O2的清除剂,所发生反应的产物不污染环境,其化学方程式为
(5)Q和Y形成的一种二元化合物具有色温效应,其相对分子质量在170~190之间,且Q的质量分数约为69.6%,则该化合物的分子式为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
【推荐1】A、B、C、D、E五种短周期元素,它们的原子序数依次增大。A是元素周期表中原子半径最小的元素,B元素原子L层上的电子数为K层电子数的2倍;元素D的2价阴离子的核外电子排布与氖原子相同;E与B同主族。请回答:
(1)写出元素的符号:C______________ ;E ______________ 。
(2)化合物CA3的电子式为________________________ 。
(3)B的最高价氧化物的结构式_______________________ 。
(4)写出化合物ED2高温下与B反应的方程式_______________________________________ 。
(1)写出元素的符号:C
(2)化合物CA3的电子式为
(3)B的最高价氧化物的结构式
(4)写出化合物ED2高温下与B反应的方程式
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
【推荐2】A、B、D、E、X是原子序数依次增大的五种短周期元素。A是周期表中相对原子质量最小的元素,A、B能形成两种液态化合物A2B和A2B2。D是短周期中原子半径最大的主族元素,E的周期序数和族序数相等,D、X的原子最外层电子数之和为8。
(1) A2B2的电子式为________________ ; E在周期表中的位置是_____________ 。
(2)如下图所示,将X单质的水溶液分别滴入盛有不同试剂的试管中。


①试管a中发生反应的化学方程式为_______________ 该反应可用于制备漂白液。
②试管b中的实验现象为____________ ,说明X的非金属性强于碘,从原子结构的角度解释其原因是_______ 。
(3)镓(31Ga)与E为同主族元素,氮化镓(GaN)作为第三代半导体材料,具有耐高温、耐高电压等特性,随着5G技术的发展,GaN商用进入快车道。下列相关说法中,正确的是_____ (填字母序号)。
a. Ga位于元素周期表的第四周期
b. GaN中Ga的化合价为+3
c. Ga3+的离子半径小于E3+的离子半径
(4) XB2是一种高效消毒剂,工业上用其处理中性废水中的锰,使Mn2+转化为MnO2沉淀除去,X被还原至最低价,该反应的离子方程式为_________ 。
(1) A2B2的电子式为
(2)如下图所示,将X单质的水溶液分别滴入盛有不同试剂的试管中。


①试管a中发生反应的化学方程式为
②试管b中的实验现象为
(3)镓(31Ga)与E为同主族元素,氮化镓(GaN)作为第三代半导体材料,具有耐高温、耐高电压等特性,随着5G技术的发展,GaN商用进入快车道。下列相关说法中,正确的是
a. Ga位于元素周期表的第四周期
b. GaN中Ga的化合价为+3
c. Ga3+的离子半径小于E3+的离子半径
(4) XB2是一种高效消毒剂,工业上用其处理中性废水中的锰,使Mn2+转化为MnO2沉淀除去,X被还原至最低价,该反应的离子方程式为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐3】X、Y、Z、R、W是原子序数依次增大的短周期主族元素,其中两种为金属元素。X的某同素异形体是天然存在的最硬物质;Y与W同主族,Y的最外层电子数是其周期数的三倍;将Z单质投入水中,浮在水面并剧烈反应;R的简单离子半径在同周期中最小。
(1)W在元素周期表中的位置是___________ ;Z的离子结构示意图为___________ 。
(2)H2Y2的电子式为___________ ;将W的氢化物通入H2Y2溶液中,溶液变浑浊,发生反应的化学方程式为___________ 。
(3)某盐组成为NH4R(WY4)2,向10mL1mol·L-1该盐溶液中滴加1mol·L-1NaOH溶液,沉淀的物质的量随加入NaOH溶液体积的变化如图所示。
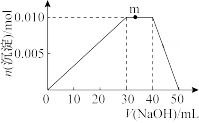
①写出m点发生反应的离子方程式___________ 。
②若在该盐溶液中改加20mL1.2mol·L-1Ba(OH)2溶液,充分反应后,溶液中产生沉淀的物质的量为___________ mol。
(1)W在元素周期表中的位置是
(2)H2Y2的电子式为
(3)某盐组成为NH4R(WY4)2,向10mL1mol·L-1该盐溶液中滴加1mol·L-1NaOH溶液,沉淀的物质的量随加入NaOH溶液体积的变化如图所示。

①写出m点发生反应的离子方程式
②若在该盐溶液中改加20mL1.2mol·L-1Ba(OH)2溶液,充分反应后,溶液中产生沉淀的物质的量为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
【推荐1】如表为元素周期表中的一部分,列出10种元素在周期表中的位置.用化学符号回答下列各题
(1)10种元素中,化学性质最不活泼的是_______ .(符号)
(2)②③④三种元素形成的离子中,离子半径由大到小的顺序是_______ .(离子符号)
(3)①③⑤三种元素最高价氧化物对应的水化物中,碱性最强的是_______ 。
(4)元素⑦的氢化物的化学式为_______ ;该氢化物常温下和②单质反应的化学方程式是_______ ;若该氢化物和元素⑧的单质反应,则化学方程式为_______ 。
(5)⑨的最高价氧化物对应水化物的化学式为_______ ;①和⑨两元素形成化合物为_______ ;该化合物灼烧时火焰颜色为_______ 。
(6)①和⑤元素最高价氧化物对应水化物相互反应的离子方程式为_______ 。
| 族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0族 |
| 2 | ⑥ | ⑦ | ||||||
| 3 | ① | ③ | ⑤ | ⑧ | ⑩ | |||
| 4 | ② | ④ | ⑨ |
(2)②③④三种元素形成的离子中,离子半径由大到小的顺序是
(3)①③⑤三种元素最高价氧化物对应的水化物中,碱性最强的是
(4)元素⑦的氢化物的化学式为
(5)⑨的最高价氧化物对应水化物的化学式为
(6)①和⑤元素最高价氧化物对应水化物相互反应的离子方程式为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
【推荐2】有A、B、D、E、X、Y、Z七种短周期元素。X与Y处于同一周期,Y的最高价氧化物对应的水化物与强酸、强碱均能反应。Z的单质常温下为气态,其相对分子质量是氢气的35.5倍。其余元素的信息如图所示:
(1)E在周期表中的位置是___________ 。
(2)A、B、D三种元素所形成的化合物ABD的电子式为___________ 。
(3)A、D、Z三种元素所形成的化合物DA4Z中的化学键类型是___________ 。
(4)X的最高价氧化物对应水化物与Y的最高价氧化物对应水化物反应的离子方程式为___________ 。
(5)下列可以判断X和Y元素原子失电子能力强弱的是___________ (填字母序号)。
a.单质的熔点X比Y低 b.单质与水反应X比Y剧烈
c.单质与酸反应时,失电子数X比Y少 d.最高价氧化物的水化物的碱性X比Y强
(6)E和Z的最高价氧化物对应水化物的酸性:___________ >___________ (填化学式)。

(1)E在周期表中的位置是
(2)A、B、D三种元素所形成的化合物ABD的电子式为
(3)A、D、Z三种元素所形成的化合物DA4Z中的化学键类型是
(4)X的最高价氧化物对应水化物与Y的最高价氧化物对应水化物反应的离子方程式为
(5)下列可以判断X和Y元素原子失电子能力强弱的是
a.单质的熔点X比Y低 b.单质与水反应X比Y剧烈
c.单质与酸反应时,失电子数X比Y少 d.最高价氧化物的水化物的碱性X比Y强
(6)E和Z的最高价氧化物对应水化物的酸性:
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐3】随着原子序数递增,八种短周期元素原子半径的相对大小、最高正价或最低负价的变化如下图所示。根据判断出的元素回答问题:

(1)f在周期表中的位置是______________ 。
(2)比较d、e常见离子的半径大小(用化学式表示,下同)___ >_____ ;比较g、h的最高价氧化物对应水化物的酸性强弱____ >______ 。
(3)任选上述元素组成一种四原子共价化合物,用电子式表示该化合物的形成过程______ 。
(4)任选上述元素组成一种最强碱,写出该碱的电子式___________ 。
(5)已知1 mol e的单质在足量d2中燃烧,恢复至室温,放出255.5 kJ热量,写出该反应的热化学方程式______________ 。

(1)f在周期表中的位置是
(2)比较d、e常见离子的半径大小(用化学式表示,下同)
(3)任选上述元素组成一种四原子共价化合物,用电子式表示该化合物的形成过程
(4)任选上述元素组成一种最强碱,写出该碱的电子式
(5)已知1 mol e的单质在足量d2中燃烧,恢复至室温,放出255.5 kJ热量,写出该反应的热化学方程式
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐1】元素的电负性用来描述不同元素的原子对键合电子吸引力的大小。电负性应用:
判断元素的金属性和非金属性的强弱。下表列出了同周期的几种短周期元素的部分性质
请回答下列问题:
(l)写出D元素的离子结构示意图_______________ 。
(2)X的值应为____ (填字母)。
A.3.6 B.3.1 C.1.4 D.2.1
(3)分析表中数据,简述同周期元素(除惰性气体)电负性大小与原子半径的关系:________________________________ 。
(4)A、B、C三种元素形成的氢化物中,其稳定性由强到弱的顺序是:__________________ (用化学式表示)。
(5)A、D最高价氧化物对应水化物相互反应的化学方程式:____ 。
判断元素的金属性和非金属性的强弱。下表列出了同周期的几种短周期元素的部分性质
请回答下列问题:
| 元素符号 | A | B | C | D | E |
| 电负性 | 3.0 | 2.5 | X | 1.5 | 0.9 |
| 原子半径(单位nm) | 0.099 | 0.102 | 0.110 | 0.143 | 0.186 |
| 主要化合价 | -1,+7 | -2,+6 | -3,+5 | +3 | +1 |
(2)X的值应为
A.3.6 B.3.1 C.1.4 D.2.1
(3)分析表中数据,简述同周期元素(除惰性气体)电负性大小与原子半径的关系:
(4)A、B、C三种元素形成的氢化物中,其稳定性由强到弱的顺序是:
(5)A、D最高价氧化物对应水化物相互反应的化学方程式:
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐2】已知A、B、C、D、E为中学常见的五种物质,均含元素Y,有的还可能含有元素X、Z,元素X、Y、Z的原子序数依次递增。
①元素Y在A、B、C、D、E中所呈化合价依次递增,其中只有B为单质。
②常温下将气体D通入水中发生反应,生成C和E。
③工业上以A、空气和水为原料,通过催化氧化法制成E。
请回答以下问题:
(1)A分子的空间构型是__________ ;从轨道重叠的方式看,B分子中的共价键类型有__________ 。
(2)写出②中反应的化学方程式:___________________________________________ 。
(3)工业上,若输送Cl2的管道漏气,用A进行检验时可观察到大量白烟,同时有B生成,写出有关反应的化学方程式:_________________________________________________ 。
①元素Y在A、B、C、D、E中所呈化合价依次递增,其中只有B为单质。
②常温下将气体D通入水中发生反应,生成C和E。
③工业上以A、空气和水为原料,通过催化氧化法制成E。
请回答以下问题:
(1)A分子的空间构型是
(2)写出②中反应的化学方程式:
(3)工业上,若输送Cl2的管道漏气,用A进行检验时可观察到大量白烟,同时有B生成,写出有关反应的化学方程式:
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐3】短周期五种元素A、B、C、D、E的原子序数依次增大。A、B、C的单质在常温下都呈气态,C原子最外层电子数是电子层数的3倍,C和E位于同主族。1molDAx与足量的A2C反应生成44.8L(标准状况)G气体。A、B的单质依次为G、T,在密闭容器中充入一定量的G、T,一定条件下发生反应G+T W(未配平),测得各物质的浓度如表所示。
W(未配平),测得各物质的浓度如表所示。
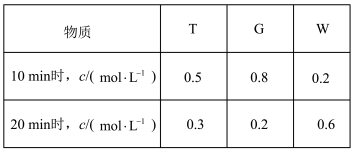
回答下列问题:
(1)A、B、C能组成既含离子键又含共价键的化合物,则该化合物的化学式为___ 。
(2)B、C、D、E的简单离子中,离子半径大小排序为___ 。(用具体的离子表示)
(3)J、L是由A、B、C、E四种元素组成的两种化合物,J、L溶液混合可产生有刺激性气味的气体,写出这两种溶液发生反应的离子方程式:___ ;J、L中能使酸性高锰酸钾溶液褪色的是___ (填化学式)。
(4)B2A4—C2碱性燃料电池放电效率高。该电池放电时,负极反应式为___ ;正极附近溶液的pH___ (填“增大”“减小”或“不变”)。
(5)由上述五种元素中的四种组成的单质、化合物在一定条件下的转化关系(部分条件和产物已省略)如图所示:

①Y是___ (填化学式);W的电子式为___ 。
②B的最高价氧化物对应的水化物为Q,X与足量的Q溶液反应的化学方程式为___ 。
③1molW与足量乙完全反应生成K和甲,转移的电子数约为___ 。
 W(未配平),测得各物质的浓度如表所示。
W(未配平),测得各物质的浓度如表所示。
回答下列问题:
(1)A、B、C能组成既含离子键又含共价键的化合物,则该化合物的化学式为
(2)B、C、D、E的简单离子中,离子半径大小排序为
(3)J、L是由A、B、C、E四种元素组成的两种化合物,J、L溶液混合可产生有刺激性气味的气体,写出这两种溶液发生反应的离子方程式:
(4)B2A4—C2碱性燃料电池放电效率高。该电池放电时,负极反应式为
(5)由上述五种元素中的四种组成的单质、化合物在一定条件下的转化关系(部分条件和产物已省略)如图所示:

①Y是
②B的最高价氧化物对应的水化物为Q,X与足量的Q溶液反应的化学方程式为
③1molW与足量乙完全反应生成K和甲,转移的电子数约为
您最近一年使用:0次



