元素的电负性用来描述不同元素的原子对键合电子吸引力的大小。电负性应用:
判断元素的金属性和非金属性的强弱。下表列出了同周期的几种短周期元素的部分性质
请回答下列问题:
(l)写出D元素的离子结构示意图_______________ 。
(2)X的值应为____ (填字母)。
A.3.6 B.3.1 C.1.4 D.2.1
(3)分析表中数据,简述同周期元素(除惰性气体)电负性大小与原子半径的关系:________________________________ 。
(4)A、B、C三种元素形成的氢化物中,其稳定性由强到弱的顺序是:__________________ (用化学式表示)。
(5)A、D最高价氧化物对应水化物相互反应的化学方程式:____ 。
判断元素的金属性和非金属性的强弱。下表列出了同周期的几种短周期元素的部分性质
请回答下列问题:
| 元素符号 | A | B | C | D | E |
| 电负性 | 3.0 | 2.5 | X | 1.5 | 0.9 |
| 原子半径(单位nm) | 0.099 | 0.102 | 0.110 | 0.143 | 0.186 |
| 主要化合价 | -1,+7 | -2,+6 | -3,+5 | +3 | +1 |
(2)X的值应为
A.3.6 B.3.1 C.1.4 D.2.1
(3)分析表中数据,简述同周期元素(除惰性气体)电负性大小与原子半径的关系:
(4)A、B、C三种元素形成的氢化物中,其稳定性由强到弱的顺序是:
(5)A、D最高价氧化物对应水化物相互反应的化学方程式:
更新时间:2017-04-23 19:29:03
|
相似题推荐
解答题-无机推断题
|
适中
(0.65)
名校
【推荐1】联合国大会将2019年定为“化学元素周期表国际年”,高度体现了元素周期表的重要性,图中表示了元素周期表短周期的一部分,A~G代表7种短周期元素。
(1)写出七种元素中化学性质最不活泼的元素形成的单质的化学式_______ 。
(2)元素B的最低价阴离子的离子结构示意图是_______ 。化合物AB2的电子式为_______
(3)B、E两种元素的最简单氢化物中稳定性较强的是_______ (填化学式)。
(4)E、F两种元素的最高价氧化物对应的水化物中,酸性较弱的是_______ (填化学式)。
(5)元素C最高价氧化物对应水化物与元素F的单质反应的离子方程式为:_______ 。
| A | B | ||||||
| C | D | E | F | G |
(2)元素B的最低价阴离子的离子结构示意图是
(3)B、E两种元素的最简单氢化物中稳定性较强的是
(4)E、F两种元素的最高价氧化物对应的水化物中,酸性较弱的是
(5)元素C最高价氧化物对应水化物与元素F的单质反应的离子方程式为:
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
【推荐2】有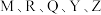 五种短周期主族元素,其中
五种短周期主族元素,其中 为短周期主族元素中原子半径最大的,
为短周期主族元素中原子半径最大的, 的最高正价与最低负价的代数和为
的最高正价与最低负价的代数和为 四种元素在元素周期表中的相对位置如图。回答下列问题:
四种元素在元素周期表中的相对位置如图。回答下列问题:
(1)R在元素周期表中的位置是_________ 。
(2)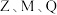 的简单离子的半径由大到小的顺序为
的简单离子的半径由大到小的顺序为_________ (用离子符号表示)。
(3)写出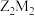 的电子式:
的电子式:_________ 。其所含的化学键类型为_________ 。
(4)下列事实能作为比较元素 与
与 的非金属性相对强弱依据的是_________(填标号)。
的非金属性相对强弱依据的是_________(填标号)。
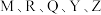 五种短周期主族元素,其中
五种短周期主族元素,其中 为短周期主族元素中原子半径最大的,
为短周期主族元素中原子半径最大的, 的最高正价与最低负价的代数和为
的最高正价与最低负价的代数和为 四种元素在元素周期表中的相对位置如图。回答下列问题:
四种元素在元素周期表中的相对位置如图。回答下列问题: | |||
 |  |  |
(2)
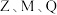 的简单离子的半径由大到小的顺序为
的简单离子的半径由大到小的顺序为(3)写出
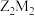 的电子式:
的电子式:(4)下列事实能作为比较元素
 与
与 的非金属性相对强弱依据的是_________(填标号)。
的非金属性相对强弱依据的是_________(填标号)。A.常温下 的单质呈固态, 的单质呈固态, 的单质呈气态 的单质呈气态 | B.最简单氢化物的稳定性: |
C. 与 与 形成的化合物中 形成的化合物中 呈正价 呈正价 | D.酸性: |
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
【推荐3】元素周期表与元素周期律在学习、研究中有很重要的作用。下表所示为某5种元素的相关信息,已知W、X都位于第三周期。
回答下列问题:
(1)W在元素周期表中的位置为___________ ,X的最高价氧化物对应的水化物的化学式为___________ 。
(2)Y的单质与水反应的离子方程式是___________ 。
(3)用电子式表示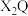 的形成过程:
的形成过程:___________ 。
(4)金属性:Y___________ (填“>”或“<”)X,用原子结构解释原因:___________ 。
(5)下列对于Z及其化合物的推断中正确的是___________ (填标号)。
A.Z的化合价中有-1和+7
B.Z的最高价氧化物对应水化物的酸性弱于W的最高价氧化物对应水化物的酸性
C.Z元素单质的氧化性强于W元素单质的氧化性
(6)将X元素的单质在Q元素的单质中点燃生成M,预测将M投入硫酸亚铁溶液中,主要的反应现象是___________ 。
| 元素 | 信息 |
| Q | 地壳中含量最高的元素 |
| W | 最高化合价为+7 |
| X | 最高价氧化物对应的水化物在本周期中碱性最强 |
| Y | 焰色试验(透过蓝色钴玻璃)的火焰呈紫色 |
| Z | 原子结构示意图为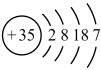 |
(1)W在元素周期表中的位置为
(2)Y的单质与水反应的离子方程式是
(3)用电子式表示
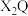 的形成过程:
的形成过程:(4)金属性:Y
(5)下列对于Z及其化合物的推断中正确的是
A.Z的化合价中有-1和+7
B.Z的最高价氧化物对应水化物的酸性弱于W的最高价氧化物对应水化物的酸性
C.Z元素单质的氧化性强于W元素单质的氧化性
(6)将X元素的单质在Q元素的单质中点燃生成M,预测将M投入硫酸亚铁溶液中,主要的反应现象是
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐1】有关元素X、Y、Z、W的信息如下:
请回答下列问题:
(1) Y的单质在空气中充分燃烧所得氧化物的电子式________________ ;
(2) X、Y、W的简单离子的半径由大到小的是_______________ (写离子符号);
(3) 向淀粉碘化钾溶液中滴加几滴ZX3的浓溶液,现象为_____________ ,Z3+基态离子的电子排布式为_________________ ;
(4) 以WX3溶液为原料制取无水WX3,主要操作包括加热浓缩、冷却结晶、过滤,先制得WX3·6H2O晶体,然后在条件下加热WX3·6H2O晶体,____________________ ,能进一步制取无水WX3,其原因是(结合离子方程式简要说明) _____________________________________ 。
元素 | 信息 |
X | 位于第三周期,其最高价氧化物水化物的酸性最强 |
Y | 在第三周期元素中,其第一电离能最小 |
Z | 单质是生活中常见金属,其制品用量最大,在潮湿空气中最易被腐蚀 |
W | 其基态原子外围电子排布为3s2p1 |
请回答下列问题:
(1) Y的单质在空气中充分燃烧所得氧化物的电子式
(2) X、Y、W的简单离子的半径由大到小的是
(3) 向淀粉碘化钾溶液中滴加几滴ZX3的浓溶液,现象为
(4) 以WX3溶液为原料制取无水WX3,主要操作包括加热浓缩、冷却结晶、过滤,先制得WX3·6H2O晶体,然后在条件下加热WX3·6H2O晶体,
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
【推荐2】A、B、C、D、E、F是高中阶段学习的常见单质或化合物,单质A在单质B中燃烧产生苍白色的火焰,产物溶于水得到常见的强酸。化合物C可由B与水反应得到,且C具有强氧化性。化合物D是淡黄色物质,可用于呼吸面具,可由一种活泼金属E在氧气中燃烧得到。D在一定条件下可转化为F,F在工业上可以制肥皂,制玻璃等。根据以上描述,请回答下列问题:
(1)物质F的俗称_______ ,C的化学式为_______ 。
(2)铁钉在B中被锈蚀为棕黄色物质,写出该反应的化学方程式,并用单线桥标出电子转移的方向和数目_______ 。
(3)写出单质E与水反应的离子方程式为_______ 。
(4)200℃时,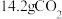 和
和 的混合物气体与足量的D反应,反应后固体增加了6.2g,则原混合物的平均相对分子质量为
的混合物气体与足量的D反应,反应后固体增加了6.2g,则原混合物的平均相对分子质量为_______ , 和
和 的物质的量之比为
的物质的量之比为_______ 。
(1)物质F的俗称
(2)铁钉在B中被锈蚀为棕黄色物质,写出该反应的化学方程式,并用单线桥标出电子转移的方向和数目
(3)写出单质E与水反应的离子方程式为
(4)200℃时,
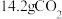 和
和 的混合物气体与足量的D反应,反应后固体增加了6.2g,则原混合物的平均相对分子质量为
的混合物气体与足量的D反应,反应后固体增加了6.2g,则原混合物的平均相对分子质量为 和
和 的物质的量之比为
的物质的量之比为
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐3】现有A、B、C、D、E五种元素,它们的核电荷数依次增多。
①A的核电荷数大于2,可形成氢化物 ,该氢化物在常温下是液体;
,该氢化物在常温下是液体;
②A和B两元素可形成化合物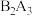 ,该化合物既能溶于强酸溶液,又能溶于强碱溶液;
,该化合物既能溶于强酸溶液,又能溶于强碱溶液;
③ 比
比 多8个电子;
多8个电子;
④C与D元素可以形成化合物CD;
⑤CD的溶液中通入氯气后加淀粉溶液显蓝色;
⑥在周期表中E处于C的下两个周期,E单质可与冷水反应生成氢气,反应时E的单质与生成的氢气的物质的量之比为 。
。
试回答下列问题:
(1)A是_____ (写元素符号,下同), 分子的空间结构为
分子的空间结构为_____________ 。
(2)B的离子结构示意图为_______ ,C元素最高价氧化物对应的水化物的电子式为_________ ,D的原子的电子排布式为___________ 。
(3)用电子式表示 的形成过程:
的形成过程:______________ 。
(4)写出CD的溶液中通入氯气的离子方程式:_____________ 。
(5)比较B、C、E三种元素形成的简单离子半径由小到大的顺序(B、C、E离子用实际离子符号表示):_____________ 。
①A的核电荷数大于2,可形成氢化物
 ,该氢化物在常温下是液体;
,该氢化物在常温下是液体;②A和B两元素可形成化合物
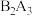 ,该化合物既能溶于强酸溶液,又能溶于强碱溶液;
,该化合物既能溶于强酸溶液,又能溶于强碱溶液;③
 比
比 多8个电子;
多8个电子;④C与D元素可以形成化合物CD;
⑤CD的溶液中通入氯气后加淀粉溶液显蓝色;
⑥在周期表中E处于C的下两个周期,E单质可与冷水反应生成氢气,反应时E的单质与生成的氢气的物质的量之比为
 。
。试回答下列问题:
(1)A是
 分子的空间结构为
分子的空间结构为(2)B的离子结构示意图为
(3)用电子式表示
 的形成过程:
的形成过程:(4)写出CD的溶液中通入氯气的离子方程式:
(5)比较B、C、E三种元素形成的简单离子半径由小到大的顺序(B、C、E离子用实际离子符号表示):
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐1】某元素的核素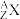 ,其氯化物XCl2 111mg溶于水后,加入0.1mol/L的硝酸银溶液20mL,恰好将其中的Cl-完全沉淀。已知该核素中的质子数和中子数相等。试回答下列问题:
,其氯化物XCl2 111mg溶于水后,加入0.1mol/L的硝酸银溶液20mL,恰好将其中的Cl-完全沉淀。已知该核素中的质子数和中子数相等。试回答下列问题:
(1)X元素的原子序数为__________ ,原子结构示意图为_____________ ;
(2)用电子式表示出XCl2的形成过程______________________________ ;
(3)写出元素X的氢化物的电子式________________________________ ;将其氢化物放入水中,立刻剧烈反应,向反应后的水溶液中滴加酚酞试剂,溶液变红色,写出该反应的化学方程式________________________________ 。
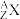 ,其氯化物XCl2 111mg溶于水后,加入0.1mol/L的硝酸银溶液20mL,恰好将其中的Cl-完全沉淀。已知该核素中的质子数和中子数相等。试回答下列问题:
,其氯化物XCl2 111mg溶于水后,加入0.1mol/L的硝酸银溶液20mL,恰好将其中的Cl-完全沉淀。已知该核素中的质子数和中子数相等。试回答下列问题:(1)X元素的原子序数为
(2)用电子式表示出XCl2的形成过程
(3)写出元素X的氢化物的电子式
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
【推荐2】有A、B、C、D四种短周期元素,它们的原子序数由A到D依次增大,已知A和B原子有相同的电子层数,且A的L层电子数是K层电子数的两倍,C在空气中燃烧呈黄色火焰,C的单质在高温下与B的单质充分反应,可以得到与D单质颜色相同的淡黄色固态化合物,试根据以上叙述回答:
(1)画出B分子的结构式_______ ,写出具有17个中子的D原子符号_______ 。
(2)D元素位于元素周期表的________ 周期________ 族。
(3)写出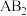 的电子式
的电子式______ ,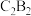 的电子式
的电子式_________ 。
(4)用电子式表示化合物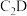 的形成过程
的形成过程________________________ 。
(5)写出A单质与D的最高价氧化物的水化物的反应的方程式_________________________ 。
(1)画出B分子的结构式
(2)D元素位于元素周期表的
(3)写出
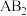 的电子式
的电子式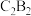 的电子式
的电子式(4)用电子式表示化合物
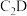 的形成过程
的形成过程(5)写出A单质与D的最高价氧化物的水化物的反应的方程式
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
【推荐3】下表是元素周期表中短周期元素的一部分,表中所列字母分别代表一种元素。
回答下列问题:
(1)上述元素中②元素的名称_______ ;⑤元素在周期表中的位置是________ 。
(2)在③、⑦、⑧的气态氢化物中最稳定的是_____ (用化学式表示);⑦的最高价氧化物对应水化物的化学式是________ 。
(3)写出⑥的单质和④的最高价氧化物对应水化物的化学方程式是________ 。
(4)④、⑤是两种活泼性不同的金属,用事实来说明④比⑤活泼性更强________ 。
(5)由①和⑧组成的化合物极易溶于水,请设计简单的实验加以说明。写出简要的实验操作、现象和结论。__________________________ 。
族 周期 | I A | Ⅱ A | Ⅲ A | Ⅳ A | V A | Ⅵ A | Ⅶ A | 0 |
| 一 | ① | |||||||
| 二 | ② | ③ | ||||||
| 三 | ④ | ⑤ | ⑥ | ⑦ | ⑧ |
(1)上述元素中②元素的名称
(2)在③、⑦、⑧的气态氢化物中最稳定的是
(3)写出⑥的单质和④的最高价氧化物对应水化物的化学方程式是
(4)④、⑤是两种活泼性不同的金属,用事实来说明④比⑤活泼性更强
(5)由①和⑧组成的化合物极易溶于水,请设计简单的实验加以说明。写出简要的实验操作、现象和结论。
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐1】科学家预测21世纪中叶将进入“氢能经济”时代,下列物质都是具有广阔应用前景的储氢材料。回答下列问题:
(1)Zr(锆)在元素周期表中位于第五周期,与钛同族,基态Zr的价层电子排布式为_______ 。
(2)亚氨基锂(Li2NH) 所含元素第一电离能最小的是____ ,电负性最大的是_____ (填元素符号)。
(3)咔唑( )的沸点比芴(
)的沸点比芴( )高的主要原因是
)高的主要原因是________ 。
(4)①NH3BH3 (氨硼烷,熔点104℃)与乙烷互为等电子体。NH3BH3的晶体类型为____ 。其中B的杂化类型为____ ,可通过_________ 测定该分子的立体构型。
②NH3BH3可通过环硼氨烷、CH4与H2O进行合成,键角: CH4______ H2O (填“> "或“<"),原因是________ 。
(5)MgH2晶体属四方品系,结构如图,晶胞参数a =b= 450pm, c= 30lpm,原子坐标为A(0,0,0)、B(0.305,0.305,0)、C(1,1,1)、D(0.195,0.805,0.5)。

①Mg2+的半径为72pm,则H+的半径为______ pm (列出计算表达式)
②用NA表示阿伏加 德罗常数,MgH2晶体中氢的密度是标准状况下氢气密度的_____ 倍(列出计算表达式,氢气密度为0.089g·L-1)。
(1)Zr(锆)在元素周期表中位于第五周期,与钛同族,基态Zr的价层电子排布式为
(2)亚氨基锂(Li2NH) 所含元素第一电离能最小的是
(3)咔唑(
 )的沸点比芴(
)的沸点比芴( )高的主要原因是
)高的主要原因是(4)①NH3BH3 (氨硼烷,熔点104℃)与乙烷互为等电子体。NH3BH3的晶体类型为
②NH3BH3可通过环硼氨烷、CH4与H2O进行合成,键角: CH4
(5)MgH2晶体属四方品系,结构如图,晶胞参数a =b= 450pm, c= 30lpm,原子坐标为A(0,0,0)、B(0.305,0.305,0)、C(1,1,1)、D(0.195,0.805,0.5)。

①Mg2+的半径为72pm,则H+的半径为
②用NA表示阿伏加 德罗常数,MgH2晶体中氢的密度是标准状况下氢气密度的
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
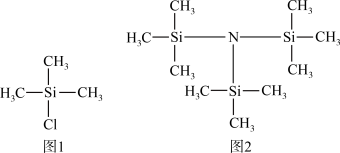
【推荐2】科学家最近开发了催化剂Mo3S4Fe捕获N2、Na和三甲基硅酰氯[Cl-Si(CH3)3] (用M代表,结构简式如图1)合成[(CH3)3Si]3N (用G代表,结构简式如图2)。
回答下列问题:
(1)基态Mo原子的价层电子排布式为4d55s1,其位于元素周期表_______ 区,最高化合价为_______ 。
(2)1 mol G中采用sp3杂化的原子有_______ mol。已知SiH4中Si—H键的电子云偏向H,G中元素电负性由小到大的顺序为_______ (填元素符号)。在G中Si、N原子构成的立体结构为_______ 。
(3)我国科学家成功研制出超灵敏传感器(MoS2/In2O3)检测气体—NO2。 晶体层状结构如图3所示。
晶体层状结构如图3所示。
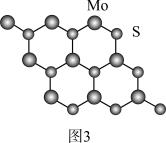
在该结构中Mo原子数、共价键数之比为_______ 。
(4)铵铁蓝广泛用于生产生活中。制备原理如下:
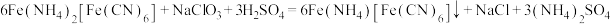
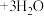
①Fe(NH4)2[Fe(CN)6]中外界的Fe2+比内界的易被氧化,其原因是_______ 。
②1 mol [Fe(CN)6]4-含_______ mol σ键。
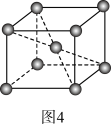
(5)钼晶胞如图4所示。已知两个钼原子最近距离为a cm,设NA为阿伏加德罗常数的值,钼晶体密度为ρ g/cm3。则钼的摩尔质量为_______ g/mol。

回答下列问题:
(1)基态Mo原子的价层电子排布式为4d55s1,其位于元素周期表
(2)1 mol G中采用sp3杂化的原子有
(3)我国科学家成功研制出超灵敏传感器(MoS2/In2O3)检测气体—NO2。
 晶体层状结构如图3所示。
晶体层状结构如图3所示。
在该结构中Mo原子数、共价键数之比为
(4)铵铁蓝广泛用于生产生活中。制备原理如下:
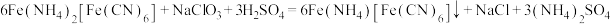
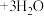
①Fe(NH4)2[Fe(CN)6]中外界的Fe2+比内界的易被氧化,其原因是
②1 mol [Fe(CN)6]4-含
(5)钼晶胞如图4所示。已知两个钼原子最近距离为a cm,设NA为阿伏加德罗常数的值,钼晶体密度为ρ g/cm3。则钼的摩尔质量为

您最近一年使用:0次
【推荐3】氧族元素及其化合物在生产、生活中发挥着重要的作用。回答如下问题:
(1)氧元素在元素周期表中的位置__________ 。基态氧原子的价层电子轨道表示式为__________ ,电子占据最高能级的电子云轮廓图为__________ 形。
(2)硫为__________ 区元素,P、S、Cl的电负性由大到小的顺序为__________ 。
(3) 、
、 、
、 沸点由大到小的顺序为
沸点由大到小的顺序为__________ 。
(4)硫酸的结构式如图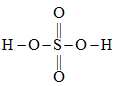 ,比较酸性:
,比较酸性: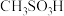
__________ 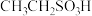 (填“大于”“小于”或“等于”),并说明原因:
(填“大于”“小于”或“等于”),并说明原因:__________ 。
(1)氧元素在元素周期表中的位置
(2)硫为
(3)
 、
、 、
、 沸点由大到小的顺序为
沸点由大到小的顺序为(4)硫酸的结构式如图
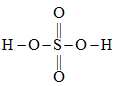 ,比较酸性:
,比较酸性: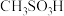
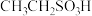 (填“大于”“小于”或“等于”),并说明原因:
(填“大于”“小于”或“等于”),并说明原因:
您最近一年使用:0次



