有A、B、C、D四种短周期元素,它们的原子序数由A到D依次增大,已知A和B原子有相同的电子层数,且A的L层电子数是K层电子数的两倍,C在空气中燃烧呈黄色火焰,C的单质在高温下与B的单质充分反应,可以得到与D单质颜色相同的淡黄色固态化合物,试根据以上叙述回答:
(1)画出B分子的结构式_______ ,写出具有17个中子的D原子符号_______ 。
(2)D元素位于元素周期表的________ 周期________ 族。
(3)写出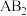 的电子式
的电子式______ ,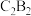 的电子式
的电子式_________ 。
(4)用电子式表示化合物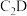 的形成过程
的形成过程________________________ 。
(5)写出A单质与D的最高价氧化物的水化物的反应的方程式_________________________ 。
(1)画出B分子的结构式
(2)D元素位于元素周期表的
(3)写出
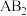 的电子式
的电子式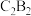 的电子式
的电子式(4)用电子式表示化合物
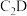 的形成过程
的形成过程(5)写出A单质与D的最高价氧化物的水化物的反应的方程式
18-19高一下·江西·周测 查看更多[1]
(已下线)【南昌新东方】2019-2020 雷氏中学 高一下 周练
更新时间:2020-06-16 10:49:43
|
相似题推荐
解答题-无机推断题
|
适中
(0.65)
【推荐1】1869年,门捷列夫制出了第一张元素周期表,成为化学史上重要的里程碑之一,元素周期表体现了元素位-构-性的关系。结合元素周期表和下表回答问题:

(1)在图中用实线补全现行长式元素周期表的边界_____________ 。
(2)上表元素①~⑨中属于短周期但不属于主族元素的是_____________ (填元素符号);元素⑨在元素周期表的位置是第_____________ 周期第_____________ 族。
(3)元素②形成单质的电子式为_____________ ;下列各组元素中,单质都具有良好导电性的是_____________ (填字母序号)。
a.①③⑥ b.②⑥⑨ c.④⑤⑧ d.⑤⑥⑨
(4)元素⑦与元素⑧相比,非金属性较强的是_____________ (填元素符号);下列可作为判断元素非金属性强弱依据的是_____________ (填字母序号)。
a.常温下单质的状态 b.简单气态氢化物的稳定性
c.单质与氢气反应的难易程度 d.氧化物对应水化物的酸性强弱
(5)元素⑧的单质与元素③的简单氢化物反应的离子方程式为_____________ 。

(1)在图中用实线补全现行长式元素周期表的边界
(2)上表元素①~⑨中属于短周期但不属于主族元素的是
(3)元素②形成单质的电子式为
a.①③⑥ b.②⑥⑨ c.④⑤⑧ d.⑤⑥⑨
(4)元素⑦与元素⑧相比,非金属性较强的是
a.常温下单质的状态 b.简单气态氢化物的稳定性
c.单质与氢气反应的难易程度 d.氧化物对应水化物的酸性强弱
(5)元素⑧的单质与元素③的简单氢化物反应的离子方程式为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
【推荐2】I.按要求回答下列问题:
(1)某粒子有1个原子核,核中有17个质子、20个中子,核外有18个电子,该粒子的化学符号是___________ 。
(2)写出下列物质的电子式:Mg(OH)2___________ ,NH3___________ ,Na2O2___________ 。
(3)用电子式表示下列化合物的形成过程:Na2S___________ ;CO2___________ 。
Ⅱ.如图为元素周期表的一部分,列出了10种元素在元素周期表中的位置,试回答下列问题:
(1)②③④三种元素最高价氧化物对应水化物的碱性由强到弱的顺序是___________ (填化学式)。
(2)10种元素中,简单离子半径最大的是___________ 填离子符号)。
(3)元素⑦的简单氢化物与过量的元素⑧的单质反应的化学方程式为___________ 。
(4)元素⑩的原子序数为___________ ,其单质与水在高温下反应的化学方程式为___________ 。
(5)元素①⑦⑧形成的常见化合物的化学式___________ ,含有化学键类型___________ 、___________ 。
(1)某粒子有1个原子核,核中有17个质子、20个中子,核外有18个电子,该粒子的化学符号是
(2)写出下列物质的电子式:Mg(OH)2
(3)用电子式表示下列化合物的形成过程:Na2S
Ⅱ.如图为元素周期表的一部分,列出了10种元素在元素周期表中的位置,试回答下列问题:
| ① | |||||||||||||||||
| ⑥ | ⑦ | ||||||||||||||||
| ② | ④ | ⑤ | ⑧ | ||||||||||||||
| ③ | ⑩ | ||||||||||||||||
| ⑨ |
(2)10种元素中,简单离子半径最大的是
(3)元素⑦的简单氢化物与过量的元素⑧的单质反应的化学方程式为
(4)元素⑩的原子序数为
(5)元素①⑦⑧形成的常见化合物的化学式
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐3】为了庆祝元素周期表诞生150周年,联合国将2019年定为“国际化学元素周期表年”,元素周期表反映了元素之间的内在联系,是学习、研究和应用化学的一种重要工具。下表是元素周期表的一部分,数字①~⑦代表前四周期七种主族元素,请按题目要求回答下列问题:
(1)①~⑦对应元素中,非金属性最强的元素名称是___________ ;⑤在周期表中的位置为___________ 。
(2)②与③形成化合物的电子式为___________ ;①的最高价氧化物的结构式为___________ 。
(3)③、④、⑥三种元素最高价氧化物对应的水化物的碱性由强到弱的顺序是___________ (用化学式来回答)。写出③、④两种元素最高价氧化物对应水化物反应的离子方程式___________ 。
(4)①~⑦对应元素中,位于金属与非金属的分界线附近的是___________ (填对应的序号)。
| ① | ② | |||||||
| ③ | ④ | ⑤ | ||||||
| ⑥ | …… | ⑦ | ||||||
(2)②与③形成化合物的电子式为
(3)③、④、⑥三种元素最高价氧化物对应的水化物的碱性由强到弱的顺序是
(4)①~⑦对应元素中,位于金属与非金属的分界线附近的是
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐1】已知a、b、c、d、e、f是中学化学中常见的七种元素,其结构或者性质信息如下表所示:
(1)写出元素 d基态原子的电子排布式为______ 。
(2)元素a的原子核外共有______ 种不同运动状态的电子,有______ 种不同能级的电子。
(3)c、f 的气态氢化物的稳定性顺序为______ (填化学式),请比较 a、b、c的电负性大小顺序为______ (填元素符号)。
(4)df2与过量的b的最高价氧化物对应水化物的稀溶液反应,其中生成物有 HfO3和一种遇空气显红棕色的气体,试写出反应的化学方程式:______ ,该反应时若有1 mol df2参加反应,则转移的电子数为______ 。
| 元素 | 结构或者性质信息 |
| a | 原子的L 层上s能级电子数等于p能级电子数 |
| b | 非金属元素,其单质为气态,有多种氧化物且都是大气污染物 |
| c | 原子的最外层电子数是内层电子数的 3 倍 |
| d | 元素的正三价离子的 3d 能级为半充满 |
| e | 元素基态原子的 M层全充满,N层没有成对电子,只有一个未成对电子 |
| f | 单质常温、常压下是易挥发的液体,基态原子的N层上有1个未成对的p电子 |
(2)元素a的原子核外共有
(3)c、f 的气态氢化物的稳定性顺序为
(4)df2与过量的b的最高价氧化物对应水化物的稀溶液反应,其中生成物有 HfO3和一种遇空气显红棕色的气体,试写出反应的化学方程式:
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
【推荐2】A、B、C、D是四种短周期主族元素, E位于第四周期。 A的最外层电子数是次外层电子数的2倍, C+与A4-具有相同的电子层结构, D的氧化物为光导纤维的主要成分。 B的简单氢化物的水溶液呈碱性, E与 B同主族。
请完成下列问题:
(1)D元素在周期表中的位置:__________________ 。
(2)B的最简单氢化物化学式为_______ ;D的氢化物稳定性比B的_____ (填“强”或“弱”)。
(3)A与D之间形成的化学键属于___________ (填“离子键”、“极性共价键” 或 “非极性共价键”);C最高价氧化物对应的水化物溶液呈_______ (填“酸性” 、“碱性”或“两性”)。
(4)B、C、D三种元素的原子半径由大到小顺序为_______________ (用元素符号表示)。
(5) E 与锗、硒的第一电离能由小到大的顺序为_____________ (用元素符号表示) 。与A的氧化物(AO)互为等电子体的有______ (写一种即可)。
(6)C的最高价氧化物的水化物与D的氧化物反应的离子方程式:________________ 。
请完成下列问题:
(1)D元素在周期表中的位置:
(2)B的最简单氢化物化学式为
(3)A与D之间形成的化学键属于
(4)B、C、D三种元素的原子半径由大到小顺序为
(5) E 与锗、硒的第一电离能由小到大的顺序为
(6)C的最高价氧化物的水化物与D的氧化物反应的离子方程式:
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐3】铍由于重量轻、弹性模数高和热稳定性好,已成为引人注目的飞机和导弹结构材料。铍与相邻主族的铝元素性质相似。
(1)Be原子的最外层电子的轨道表示式_______ 。
(2)下列有关铍和铝的叙述正确的是_______。
(3)写出氧化铍和NaOH溶液反应的离子方程式:_______ 。
(4)铍的熔点是1287℃,釱的熔点为650℃,原因是_______ 。
(5)氯化铍在气态时存在 分子(a)和二聚分子
分子(a)和二聚分子 ,固态时则具有如下图所示的链状结构(c)。
,固态时则具有如下图所示的链状结构(c)。

a为直线型分子,a是含有_______ (填“极性”或“非极性”)共价键的_______ (填“极性”或“非极性”)分子。二聚分子 中Be原子的成键方式相同,且所有原子都在同一平面上,b的结构式为
中Be原子的成键方式相同,且所有原子都在同一平面上,b的结构式为_______ 。
(1)Be原子的最外层电子的轨道表示式
(2)下列有关铍和铝的叙述正确的是_______。
| A.都属于轻金属 | B.失电子的能力都比镁弱 |
| C.原子核外电子云形状都是2种 | D.氯化物的水溶液PH均小于7 |
(4)铍的熔点是1287℃,釱的熔点为650℃,原因是
(5)氯化铍在气态时存在
 分子(a)和二聚分子
分子(a)和二聚分子 ,固态时则具有如下图所示的链状结构(c)。
,固态时则具有如下图所示的链状结构(c)。
a为直线型分子,a是含有
 中Be原子的成键方式相同,且所有原子都在同一平面上,b的结构式为
中Be原子的成键方式相同,且所有原子都在同一平面上,b的结构式为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐1】短周期主族元素A,B,C,D,E,F的原子序数依次增大,它们的原子核外电子层数之和为13。B的化合物种类繁多,数目庞大;C,D是空气中含量最多的两种元素,D,E两种元素的单质反应可以生成两种不同的离子化合物;F为同周期半径最小的元素。试回答以下问题:
(1)D、E两种元素的单质反应生成的两种离子化合物分别是________ 、___________ 。
(2)化学组成为BDF2的电子式为:_______ ,A、C、F三种元素形成的化合物CA4F为_________ 化合物(填 “离子”或“共价”)。
(3)化合物甲、乙由A,B,D,E中的三种或四种组成,且甲、乙的水溶液均呈碱性。则甲、乙反应的离子方程式为:_______________________________ 。
(4)由C,D,E,F形成的简单离子的离子半径由大到小的顺序是_________________ (用元素离子符号表示)。
(5)元素B和F的非金属性强弱,B的非金属性_________ 于F(填“强”或“弱”),并用化学方程式证明上述结论_______________________________ 。
(1)D、E两种元素的单质反应生成的两种离子化合物分别是
(2)化学组成为BDF2的电子式为:
(3)化合物甲、乙由A,B,D,E中的三种或四种组成,且甲、乙的水溶液均呈碱性。则甲、乙反应的离子方程式为:
(4)由C,D,E,F形成的简单离子的离子半径由大到小的顺序是
(5)元素B和F的非金属性强弱,B的非金属性
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
【推荐2】A、B、C、D、E、F六种物质的相互转化关系如下图所示(反应条件未标出),其中反应①是置换反应,B、C、F都是气态单质,且B为黄绿色;反应③中有水生成,反应②需要放电才能发生,A和D相遇有白烟生成。
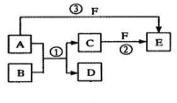
(1)反应③的化学方程式为:_________________ ;
(2)反应①中每生成1 molC,转移的电子数为______________ ;
(3)A与D的水溶液恰好完全反应时,其生成物的水溶液呈_____ 性(填“酸”“碱”或“中”),该水溶液中存在着如下关系,用粒子浓度符号填写。
①c(H+)+____ = c(OH-)+ c(Cl-);
②c(H+)= c(OH-)+____ ;
(4)元素X与组成B的元素同周期,X的单质既可与酸反应也可与碱反应且都生成H2,则
①X的单质与碱反应的离子方程式_____________________________ ;
②X、空气、海水可以组成新型海水标志灯的电池。该电池以海水为电解质溶液,靠氧气使X不断氧化而源源不断产生电流,只要把灯放入海水中,数分钟后就会发出耀眼的闪光,其能量比干电池高20~50倍。则该新型电池的正极的电极反应式为________________ ;原电池的总反应方程式为________________________ 。

(1)反应③的化学方程式为:
(2)反应①中每生成1 molC,转移的电子数为
(3)A与D的水溶液恰好完全反应时,其生成物的水溶液呈
①c(H+)+
②c(H+)= c(OH-)+
(4)元素X与组成B的元素同周期,X的单质既可与酸反应也可与碱反应且都生成H2,则
①X的单质与碱反应的离子方程式
②X、空气、海水可以组成新型海水标志灯的电池。该电池以海水为电解质溶液,靠氧气使X不断氧化而源源不断产生电流,只要把灯放入海水中,数分钟后就会发出耀眼的闪光,其能量比干电池高20~50倍。则该新型电池的正极的电极反应式为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐3】元素及其化合物知识在工农业生产、生活中被广泛使用,造福人类。
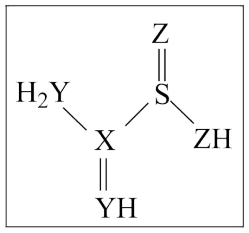
I.元素X、Y、Z和H、S元素组成的某种化合物(结构如图)常用作丝绸漂白剂,图中所有元素仅X、Y、Z同周期且原子序数依次增大。回答下列问题:
(1)Y元素的原子结构示意图为___________ ,该漂白剂所含元素非金属性最强的元素是在元素周期表中的位置为___________ 。
(2)下列说法错误的是___________(选填序号)。
Ⅱ.该漂白剂中有两种元素的氢化物均可发生如下转化:

(3)若该氢化物的水溶液呈碱性,写出该氢化物的电子式为___________ 。图中该氢化物转化为甲的化学方程式___________ 。化合物丁中Y元素的质量分数为___________ %。
(4)若该化合物的水溶液呈酸性,图中甲转化为乙的化学方程式为___________ 。该氢化物与丙的浓溶液反应,出现淡黄色浑浊且有刺激性气体放出。每生成1摩尔沉淀时,转移的电子数目为___________ 。

I.元素X、Y、Z和H、S元素组成的某种化合物(结构如图)常用作丝绸漂白剂,图中所有元素仅X、Y、Z同周期且原子序数依次增大。回答下列问题:
(1)Y元素的原子结构示意图为
(2)下列说法错误的是___________(选填序号)。
| A.原子半径:X>Y>Z | B.简单气态氢化物稳定性:Y<Z |
| C.沸点:H2Z<H2S | D.该化合物中所有原子均为8电子稳定结构 |
Ⅱ.该漂白剂中有两种元素的氢化物均可发生如下转化:

(3)若该氢化物的水溶液呈碱性,写出该氢化物的电子式为
(4)若该化合物的水溶液呈酸性,图中甲转化为乙的化学方程式为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
【推荐1】A、B、C、D、E、F为原子序数依次增大第三周期元素。已知A、C、F三原子的最外层共有11个电子,且这种三元素的最高价氧化物的水化物之间两两皆能反应,均能生成盐和水,D元素原子的最外层电子数比次外层电子数少4个,E元素氢化物中有2个氢原子,试回答:
(1)写出B原子结构示意图___
(2)元素最高价氧化物对应水化物中碱性最强的是___ ,写出一种含有F元素的具有漂白性的物质___ (用化学式表示)。
(3)用电子式表示A、F原子形成化合物的过程___ 。
(4)C、F两种元素最高价氧化物的水化物之间反应的离子方程式___ 。
(5)设计实验证明E、F两种元素非金属性的强弱___ (化学方程式加必要文字说明)。
(1)写出B原子结构示意图
(2)元素最高价氧化物对应水化物中碱性最强的是
(3)用电子式表示A、F原子形成化合物的过程
(4)C、F两种元素最高价氧化物的水化物之间反应的离子方程式
(5)设计实验证明E、F两种元素非金属性的强弱
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐2】现有A、B、C、D、E、F、G七种短周期主族元素,其原子序数依次增大。已如A、D位于同一主族,D是短周期中原子半径最大的。B、E最外层电子数是最内层电子数的2倍。C、F的最外层电子数相等,且C、F的原子序数之和为A、D原子序数之和的两倍。
(1)A、C、D、F形成的简单离子半径由大到小的顺序是____________ (用元素符号填写)。
(2)B、E、F、G最高价氧化物对应的水化物酸性最强的是___________ (用化学式填写)。
(3)由C、D两元素能形成一种原子个数比为1:1的化合物,该化合物所含的化学键类型有____________ 。
(4)下列事实能说明G元素的非金属性比F元素的非金属性强的是______________ 。
a. G单质与Na2S溶液反应溶液变浑浊
b. F氢化物的酸性比G的氢化物酸性弱
c. G和F两元素的简单氢化物受热分解,前者的分解温度高
(5)A、C、D、F四种元素形成的化合物M和N在溶液中相互反应的离子方程式是________________ 。
(1)A、C、D、F形成的简单离子半径由大到小的顺序是
(2)B、E、F、G最高价氧化物对应的水化物酸性最强的是
(3)由C、D两元素能形成一种原子个数比为1:1的化合物,该化合物所含的化学键类型有
(4)下列事实能说明G元素的非金属性比F元素的非金属性强的是
a. G单质与Na2S溶液反应溶液变浑浊
b. F氢化物的酸性比G的氢化物酸性弱
c. G和F两元素的简单氢化物受热分解,前者的分解温度高
(5)A、C、D、F四种元素形成的化合物M和N在溶液中相互反应的离子方程式是
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐3】元素的电负性用来描述不同元素的原子对键合电子吸引力的大小。电负性应用:
判断元素的金属性和非金属性的强弱。下表列出了同周期的几种短周期元素的部分性质
请回答下列问题:
(l)写出D元素的离子结构示意图_______________ 。
(2)X的值应为____ (填字母)。
A.3.6 B.3.1 C.1.4 D.2.1
(3)分析表中数据,简述同周期元素(除惰性气体)电负性大小与原子半径的关系:________________________________ 。
(4)A、B、C三种元素形成的氢化物中,其稳定性由强到弱的顺序是:__________________ (用化学式表示)。
(5)A、D最高价氧化物对应水化物相互反应的化学方程式:____ 。
判断元素的金属性和非金属性的强弱。下表列出了同周期的几种短周期元素的部分性质
请回答下列问题:
| 元素符号 | A | B | C | D | E |
| 电负性 | 3.0 | 2.5 | X | 1.5 | 0.9 |
| 原子半径(单位nm) | 0.099 | 0.102 | 0.110 | 0.143 | 0.186 |
| 主要化合价 | -1,+7 | -2,+6 | -3,+5 | +3 | +1 |
(2)X的值应为
A.3.6 B.3.1 C.1.4 D.2.1
(3)分析表中数据,简述同周期元素(除惰性气体)电负性大小与原子半径的关系:
(4)A、B、C三种元素形成的氢化物中,其稳定性由强到弱的顺序是:
(5)A、D最高价氧化物对应水化物相互反应的化学方程式:
您最近一年使用:0次



