通常人们把拆开1mol某化学键所消耗的能量看作是该化学键的键能。键能的大小可衡量化学键的强弱,也可以估算化学反应的反应热。下表为某些化学键的键能
已知火箭燃料肼( )有关化学反应的能量变化如图所示,则下列说法正确的是
)有关化学反应的能量变化如图所示,则下列说法正确的是
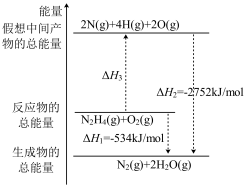
| 化学键 | N-N | O=O | N≡N | N-H |
| 键能(kJ/mol) | 154 | 500 | 942 | a |
 )有关化学反应的能量变化如图所示,则下列说法正确的是
)有关化学反应的能量变化如图所示,则下列说法正确的是
A.相同条件下 比 比 稳定 稳定 |
B.  |
| C.表中的a=391 |
D.图中的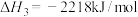 |
更新时间:2023-11-30 15:52:20
|
相似题推荐
单选题
|
适中
(0.65)
名校
【推荐1】CH4与CO2重整制氢的主要反应的热化学方程式为
反应Ⅰ:
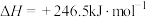
反应Ⅱ:
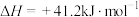
反应Ⅲ: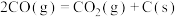
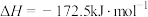
 下,将
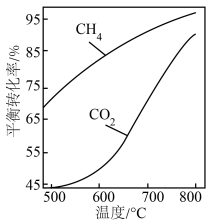
下,将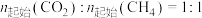 的混合气体置于密闭容器中,不同温度下重整体系中CH4和CO2的平衡转化率如图所示。下列说法正确的是
的混合气体置于密闭容器中,不同温度下重整体系中CH4和CO2的平衡转化率如图所示。下列说法正确的是
反应Ⅰ:

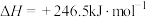
反应Ⅱ:

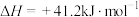
反应Ⅲ:
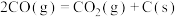
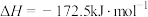
 下,将
下,将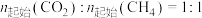 的混合气体置于密闭容器中,不同温度下重整体系中CH4和CO2的平衡转化率如图所示。下列说法正确的是
的混合气体置于密闭容器中,不同温度下重整体系中CH4和CO2的平衡转化率如图所示。下列说法正确的是
| A.反应Ⅰ的ΔS>0,反应Ⅱ的ΔS<0 |
B.反应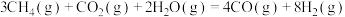  |
| C.500℃~800℃,反应Ⅲ进行的程度始终比反应Ⅱ的大 |
| D.向重整体系中加入选择性更高的催化剂有助于提高H2的平衡产率 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】已知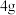 氢气完全燃烧生成水蒸气时放出能量
氢气完全燃烧生成水蒸气时放出能量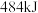 ,水蒸气中
,水蒸气中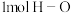 键形成时放出能量
键形成时放出能量 ,
, 键断裂时吸收的能量为
键断裂时吸收的能量为 ,断开
,断开 氧气中的化学键需要吸收的能量是
氧气中的化学键需要吸收的能量是
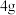 氢气完全燃烧生成水蒸气时放出能量
氢气完全燃烧生成水蒸气时放出能量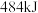 ,水蒸气中
,水蒸气中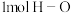 键形成时放出能量
键形成时放出能量 ,
, 键断裂时吸收的能量为
键断裂时吸收的能量为 ,断开
,断开 氧气中的化学键需要吸收的能量是
氧气中的化学键需要吸收的能量是A.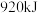 | B.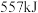 | C.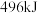 | D.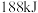 |
您最近一年使用:0次
单选题
|
适中
(0.64)
【推荐3】下列各组热化学方程式中ΔH1小于ΔH2的是
(1)S(s)+O2(g)===SO2(g),ΔH1
S(g)+O2(g)===SO2(g),ΔH2
(2)CH4(g)+2O2(g)===CO2(g)+2H2O(l),ΔH1
CH4(g)+1.5O2(g)===CO(g)+2H2O(g),ΔH2
(3)4Al(s)+3O2(g)===2Al2O3(s),ΔH1
4Fe(s)+3O2(g)===2Fe2O3(s),ΔH2
(4)放热反应CO(g)+2H2(g) CH3OH(g)ΔH1
CH3OH(g)ΔH1
CO(g)+2H2(g) CH3OH(l)ΔH2
CH3OH(l)ΔH2
(1)S(s)+O2(g)===SO2(g),ΔH1
S(g)+O2(g)===SO2(g),ΔH2
(2)CH4(g)+2O2(g)===CO2(g)+2H2O(l),ΔH1
CH4(g)+1.5O2(g)===CO(g)+2H2O(g),ΔH2
(3)4Al(s)+3O2(g)===2Al2O3(s),ΔH1
4Fe(s)+3O2(g)===2Fe2O3(s),ΔH2
(4)放热反应CO(g)+2H2(g)
 CH3OH(g)ΔH1
CH3OH(g)ΔH1CO(g)+2H2(g)
 CH3OH(l)ΔH2
CH3OH(l)ΔH2| A.只有(2) | B.只有(2 ) (4) |
| C.只有(1) (2 ) (4) | D.只有(2 ) (3) |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】甲醇羰基化制乙酸的催化剂为可溶性铱配合物(主催化剂)和碘化物(助催化剂),利用铱配合物[Ir(CO2)I2]-催化甲醇羰基化的反应历程如图所示(其中Me-CH3,Ac-COCH3)。下列说法不正确的是


| A.该催化循环中Ir的成键数目发生变化 |
| B.HI是反应过程中的助催化剂 |
| C.CO分压增大对反应速率没有影响 |
| D.反应历程中存在反应[Ir(CO)2I3(CH3)]-+CO=Ir(CO)3I2(CH3)+I- |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】已知A转化为C和D分步进行:①A(g)⇌B(g)+2D(g);②B(g)⇌C(g)+D(g),其反应过程能量如图所示,下列说法正确的是
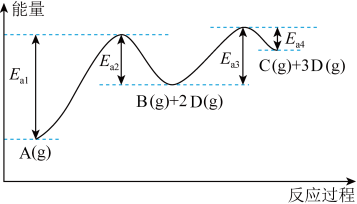

| A.1molA(g)的能量低于1molB(g)的能量 |
| B.B(g)⇌C(g)+D(g) ΔH=(Ea4-Ea3)kJ/mol |
| C.断裂1molA(g)化学键吸收的热量小于形成1molC(g)和3molD(g)化学键所放出的热量 |
| D.反应过程中,由于Ea3<Ea1,反应②速率大于反应①,气体B很难大量积累 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】根据如图所得判断正确的是
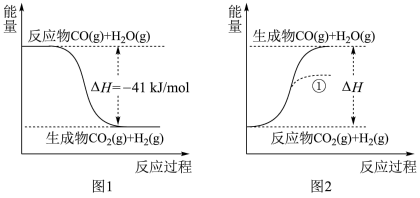
已知H2O(g)=H2O(l) △H=-44kJ/mol

已知H2O(g)=H2O(l) △H=-44kJ/mol
| A.图1反应为吸热反应 |
| B.图1反应使用催化剂时,会改变其△H |
| C.图2中若H2O的状态为液态,则能量变化曲线可能为① |
| D.图2中反应为CO2(g)+H2(g)=CO(g)+H2O(l) △H=+41kJ/mol |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】下列热化学方程式书写正确 的是
| A.2H2O (g) =2H2(g)+O2(g) |
| B.2H2(g)+O2(g) = 2H2O(l) △H=-571.6 kJ/mol |
| C.2SO2 + O2 = 2SO3 △H=-196.6 kJ/mol |
| D.C(s) + O2(g) = CO2(g) △H= +393.5 kJ/mol |
您最近一年使用:0次




