钠、氯及其化合物有如图转化关系,淡黄色物质M可在潜水艇中作为氧气的来源,常被用作供氧剂,N常被用来杀菌消毒。请按要求填空:

(1)实验室中金属钠通常保存在___________ 中,金属钠在空气中燃烧火焰呈___________ 色。
(2)写出M与水反应的离子方程式为___________ ,当生成标准状况下的氧气 时,转移电子数目为
时,转移电子数目为___________ (用 表示阿伏加德罗常数的值)。
表示阿伏加德罗常数的值)。
(3)新制的氯水呈___________ 色,放置一段时间后,溶液的 会
会___________ (填“增大”或“减小”)。
(4) 在空气中
在空气中 的作用下,产生有漂白、杀菌作用的次氯酸,该反应的化学方程式为
的作用下,产生有漂白、杀菌作用的次氯酸,该反应的化学方程式为___________ 。
(5)特殊条件下的离子反应方程式的书写:
①在碱性条件下,氯气可将废水中的 氧化为无毒无害的
氧化为无毒无害的 和
和 ,该反应的离子方程式为
,该反应的离子方程式为___________ 。
②在酸性条件下,向铬废水中加入绿矾 ,可将
,可将 还原为
还原为 ,该反应的离子方程式为
,该反应的离子方程式为___________ 。

(1)实验室中金属钠通常保存在
(2)写出M与水反应的离子方程式为
 时,转移电子数目为
时,转移电子数目为 表示阿伏加德罗常数的值)。
表示阿伏加德罗常数的值)。(3)新制的氯水呈
 会
会(4)
 在空气中
在空气中 的作用下,产生有漂白、杀菌作用的次氯酸,该反应的化学方程式为
的作用下,产生有漂白、杀菌作用的次氯酸,该反应的化学方程式为(5)特殊条件下的离子反应方程式的书写:
①在碱性条件下,氯气可将废水中的
 氧化为无毒无害的
氧化为无毒无害的 和
和 ,该反应的离子方程式为
,该反应的离子方程式为②在酸性条件下,向铬废水中加入绿矾
 ,可将
,可将 还原为
还原为 ,该反应的离子方程式为
,该反应的离子方程式为
更新时间:2023-12-15 10:59:51
|
相似题推荐
解答题-工业流程题
|
适中
(0.65)
名校
【推荐1】钯(Pd)见一种银白色过渡金属,质软、有良好的延展性和可塑性,可锻造、压延和拉丝。块状金属钯能吸收大量氢气,使体积显著胀大、变脆乃至破裂成碎片。一种从废钯催化剂(杂质主要含有机物、活性炭及少量Fe、Cu、Al等元素)中回收钯和催化剂FeOCl的工艺流程如图所示:
②离子交换树脂的基本工作原理分别为 (
(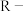 表示树脂的有机成分);
表示树脂的有机成分);
③常温下,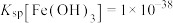 ,
,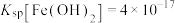 ,
,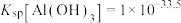 ;当溶液中某离子浓度小于等于
;当溶液中某离子浓度小于等于 时,可认为该离子沉淀完全;
时,可认为该离子沉淀完全;
④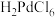 是一种二元强酸,
是一种二元强酸,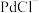 在溶液中存在配位平衡:
在溶液中存在配位平衡: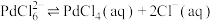
 ;
;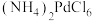 在水中溶解度小。
在水中溶解度小。
回答下列问题:
(1)废钯催化剂“焙烧”时,先通入空气进行逆流式焙烧的目的是___________ ,再通入甲酸继续焙烧的目的是___________ 。
(2)“酸浸”过程需要升高温度至70℃左右,则主要反应的离子方程式为___________ 。
(3)“洗脱”时,加入最佳“试剂Y”的名称是___________ ,“洗脱液”中要加入过量 的目的是
的目的是___________ 。
(4)“还原”过程中,不生成污染环境的气体,则被氧化的元素与被还原的元素物质的量之比为___________ 。“调pH”步骤中,若铁元素和铝元素浓度均为 ,则调pH的范围为
,则调pH的范围为___________  。
。

②离子交换树脂的基本工作原理分别为
 (
(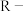 表示树脂的有机成分);
表示树脂的有机成分);③常温下,
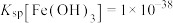 ,
,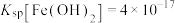 ,
,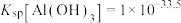 ;当溶液中某离子浓度小于等于
;当溶液中某离子浓度小于等于 时,可认为该离子沉淀完全;
时,可认为该离子沉淀完全;④
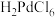 是一种二元强酸,
是一种二元强酸,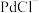 在溶液中存在配位平衡:
在溶液中存在配位平衡: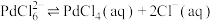
 ;
;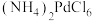 在水中溶解度小。
在水中溶解度小。回答下列问题:
(1)废钯催化剂“焙烧”时,先通入空气进行逆流式焙烧的目的是
(2)“酸浸”过程需要升高温度至70℃左右,则主要反应的离子方程式为
(3)“洗脱”时,加入最佳“试剂Y”的名称是
 的目的是
的目的是(4)“还原”过程中,不生成污染环境的气体,则被氧化的元素与被还原的元素物质的量之比为
 ,则调pH的范围为
,则调pH的范围为 。
。
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐2】有一瓶澄清的溶液,其中可能含有 、
、 、
、 、
、 、
、 、
、 、
、 、
、 、
、 、
、 等离子。取该溶液进行以下实验:
等离子。取该溶液进行以下实验:
①用pH试纸检验,溶液呈强酸性;
②取溶液适量,加入少量 和数滴新制氯水,振荡,
和数滴新制氯水,振荡, 层呈紫红色;
层呈紫红色;
③另取溶液适量,逐滴加入NaOH溶液;
a.溶液从酸性变为中性;
b.溶液逐渐产生沉淀;
c.沉淀完全溶解;
④取适量③得到的碱性溶液,加入 溶液,有白色沉淀生成。
溶液,有白色沉淀生成。
根据上述实验现象,回答下列问题。
(1)由①可以排除_______ 的存在。
(2)由②可以证明_______ 的存在;同时排除_______ 的存在。
(3)由③可以证明_______ 的存在;写出c所涉及的离子反应方程式:_______ 。
(4)由④可以排除_______ 的存在,同时证明_______ 的存在。
 、
、 、
、 、
、 、
、 、
、 、
、 、
、 、
、 、
、 等离子。取该溶液进行以下实验:
等离子。取该溶液进行以下实验:①用pH试纸检验,溶液呈强酸性;
②取溶液适量,加入少量
 和数滴新制氯水,振荡,
和数滴新制氯水,振荡, 层呈紫红色;
层呈紫红色;③另取溶液适量,逐滴加入NaOH溶液;
a.溶液从酸性变为中性;
b.溶液逐渐产生沉淀;
c.沉淀完全溶解;
④取适量③得到的碱性溶液,加入
 溶液,有白色沉淀生成。
溶液,有白色沉淀生成。根据上述实验现象,回答下列问题。
(1)由①可以排除
(2)由②可以证明
(3)由③可以证明
(4)由④可以排除
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
解题方法
【推荐3】已知: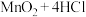 (浓)
(浓)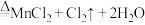 。实验室用足量NaOH溶液吸收从浓盐酸和
。实验室用足量NaOH溶液吸收从浓盐酸和 反应体系中导出的气体。当吸收温度不同时,生成的产物可能是NaClO、
反应体系中导出的气体。当吸收温度不同时,生成的产物可能是NaClO、 、NaCl中的两种或三种。
、NaCl中的两种或三种。
(1)若产物为NaClO、NaCl,请写出NaOH与 反应的
反应的离子方程式 :_______ 。吸收后溶液中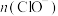
_______  (请填写“<”、“=”或“>”)
(请填写“<”、“=”或“>”)
(2)若产物为 、NaCl,则参加反应的氧化剂和还原剂的物质的量之比为:
、NaCl,则参加反应的氧化剂和还原剂的物质的量之比为:_______ 。
(3)若产物为NaClO、 、NaCl,则NaOH与
、NaCl,则NaOH与 相互反应的物质的量之比为:
相互反应的物质的量之比为:____ 。
(4)实验室制备氯气时高锰酸钾也是常用的强氧化剂,在酸性条件下, 离子被还原成
离子被还原成 。写出高锰酸钾与浓盐酸在室温下制氯气的
。写出高锰酸钾与浓盐酸在室温下制氯气的离子方程式 _______ 。
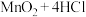 (浓)
(浓)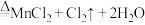 。实验室用足量NaOH溶液吸收从浓盐酸和
。实验室用足量NaOH溶液吸收从浓盐酸和 反应体系中导出的气体。当吸收温度不同时,生成的产物可能是NaClO、
反应体系中导出的气体。当吸收温度不同时,生成的产物可能是NaClO、 、NaCl中的两种或三种。
、NaCl中的两种或三种。(1)若产物为NaClO、NaCl,请写出NaOH与
 反应的
反应的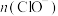
 (请填写“<”、“=”或“>”)
(请填写“<”、“=”或“>”)(2)若产物为
 、NaCl,则参加反应的氧化剂和还原剂的物质的量之比为:
、NaCl,则参加反应的氧化剂和还原剂的物质的量之比为:(3)若产物为NaClO、
 、NaCl,则NaOH与
、NaCl,则NaOH与 相互反应的物质的量之比为:
相互反应的物质的量之比为:(4)实验室制备氯气时高锰酸钾也是常用的强氧化剂,在酸性条件下,
 离子被还原成
离子被还原成 。写出高锰酸钾与浓盐酸在室温下制氯气的
。写出高锰酸钾与浓盐酸在室温下制氯气的
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
【推荐1】固体盐X由四种常见元素组成,其中仅含一种金属元素,有如图转化关系:

已知:H中溶质仅为一种常见正盐。黄绿色气体C密度为相同条件下H2的33.75倍。
请回答:
(1)X的组成元素为____ ,固体F成分为____ 。
(2)固体X在水中也可反应生成气体B,同时生成一种的相对较稳定的白色沉淀,请写出该反应化学方程式____ 。
(3)向血红色溶液Ⅰ中加入足量的KI溶液,发生氧化还原反应,产物中含有与血红色物质组成元素相同的微粒,请写出该反应可能的离子方程式____ 。
(4)气体C的化学式为____ 。将气体C通入KOH溶液,微热,恰好完全反应,生成两种物质的量之比1∶5的盐,写出这两种盐的化学式____ ,设计定量实验方案 验证上述比例关系____ 。

已知:H中溶质仅为一种常见正盐。黄绿色气体C密度为相同条件下H2的33.75倍。
请回答:
(1)X的组成元素为
(2)固体X在水中也可反应生成气体B,同时生成一种的相对较稳定的白色沉淀,请写出该反应化学方程式
(3)向血红色溶液Ⅰ中加入足量的KI溶液,发生氧化还原反应,产物中含有与血红色物质组成元素相同的微粒,请写出该反应可能的离子方程式
(4)气体C的化学式为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
【推荐2】X、Y、Z四种主族元素的单质在常温下都是气体,X、Y、Z对应的单质可以两两反应生成相应的A、B、C三个分子,其中B、C都是10电子且含有相同的元素X。A是一种难溶于水的有毒气体。他们之间还存在下列关系:
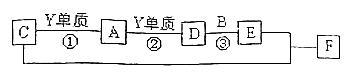
请回答下列问题:
(1)Z的原子结构示意图________ ,C的电子式为________ 。
(2)反应②的现象为______ ;写出反应③的化学方程式_________________________
(3)化合物F中含有的化合键为___________ 。

请回答下列问题:
(1)Z的原子结构示意图
(2)反应②的现象为
(3)化合物F中含有的化合键为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐3】A、B两种固体,都由甲、乙两种元素组成。在A、B中,甲(金属元素)、乙(非金属元素)两种元素的原子个数比分别为1:1和1:2。高温煅烧A、B时,产物都是C(固体)和D(气体)。由D可制得E(酸),E和另一种酸组成的混合酸跟甲苯反应可生成三硝基甲苯。C与E的稀溶液反应得到溶液F,往F溶液中加入NaOH溶液,有红褐色沉淀生成,该沉淀经灼烧后转变成C。往F溶液中加入甲元素的单质得到溶液G。试根据以上信息填写下列空白:
(1)A的化学式是
(2)B煅烧生成C和D的化学方程式是
(3)甲元素的单质与F溶液反应的离子方程式是
(4)往G溶液中加入NaOH溶液发生的现象是 ,
写出该反应的化学方程式 、 。
(5)工业上用D制E时,在原料气相同的情况下,测得压强对D平衡转化率的影响见下表:根据表中数据,考虑综合经济效益,你认为该反应应在下列哪中压强下进行最为有利: 。
(1)A的化学式是
(2)B煅烧生成C和D的化学方程式是
(3)甲元素的单质与F溶液反应的离子方程式是
(4)往G溶液中加入NaOH溶液发生的现象是 ,
写出该反应的化学方程式 、 。
(5)工业上用D制E时,在原料气相同的情况下,测得压强对D平衡转化率的影响见下表:根据表中数据,考虑综合经济效益,你认为该反应应在下列哪中压强下进行最为有利: 。
| 0.1MPa | 0.5MPa[ | 1 MPa | 10 MPa | |
| 400℃ | 99.2% | 99.6%[ | 99.7% | 99.9%[来 |
| 500℃ | 93.5% | 96.9% | 97.8% | 99.3% |
| 600℃ | 73.7% | 85.8% | 89.5% | 96.4% |
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐1】常温下,A是可用来对自来水进行消毒的黄绿色单质气体,A、B、C、D、E 都含X元素,其转化关系如下图所示。
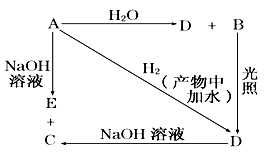
(1)请分别写出A、B、C、D、E的化学式(如为溶液请填溶质的化学式):
A_____ ,B _____ ,C ______ ,D_____ ,E___________ 。
(2)写出下列反应的化学方程式:
A+H2O:______________ ;
A+NaOH:______________________ 。

(1)请分别写出A、B、C、D、E的化学式(如为溶液请填溶质的化学式):
A
(2)写出下列反应的化学方程式:
A+H2O:
A+NaOH:
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐2】用Cl2和Ca(OH)2制备少量漂粉精(一种含氯消毒剂)的装置如图。
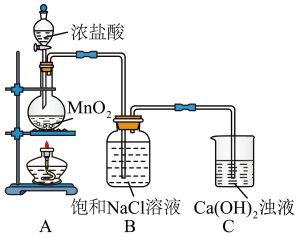
(1)C中制漂粉精时Cl2中不能有HCl,HCl可能对制备漂粉精造成影响是____ 。
(2)用Cl2和Ca(OH)2制备的漂粉精,其有效成分是____ 。
(3)漂粉精常用于游泳池的消毒,起消毒作用的是HClO。漂粉精在水中释放HClO的途径如下:
途径一:Ca(ClO)2+2H2O Ca(OH)2+2HClO
Ca(OH)2+2HClO
途径二:Ca(ClO)2+H2O+CO2=______+______(把反应补充完整)____
(4)池水的酸碱性对漂粉精的消毒效果影响明显。
①池水碱性过强,杀毒作用会_____ (填“增强”或“减弱”)。
②池水酸性过强,会刺激眼睛和皮肤。通常加入Na2CO3、NaHCO3以降低酸性,起到降低酸性作用的离子分别是_____ (填离子符号)。
(5)某届奥运会期间,发生了室外游泳池水变绿的事件,成为当时的一大新闻。有关负责人说,池水变绿是藻类生长造成的。该游泳池每隔一段时间就要投放含氯消毒剂,当再次投放时,误投了过氧化氢(H2O2)消毒剂。消毒剂为什么不起作用了?_____ 。

(1)C中制漂粉精时Cl2中不能有HCl,HCl可能对制备漂粉精造成影响是
(2)用Cl2和Ca(OH)2制备的漂粉精,其有效成分是
(3)漂粉精常用于游泳池的消毒,起消毒作用的是HClO。漂粉精在水中释放HClO的途径如下:
途径一:Ca(ClO)2+2H2O
 Ca(OH)2+2HClO
Ca(OH)2+2HClO途径二:Ca(ClO)2+H2O+CO2=______+______(把反应补充完整)
(4)池水的酸碱性对漂粉精的消毒效果影响明显。
①池水碱性过强,杀毒作用会
②池水酸性过强,会刺激眼睛和皮肤。通常加入Na2CO3、NaHCO3以降低酸性,起到降低酸性作用的离子分别是
(5)某届奥运会期间,发生了室外游泳池水变绿的事件,成为当时的一大新闻。有关负责人说,池水变绿是藻类生长造成的。该游泳池每隔一段时间就要投放含氯消毒剂,当再次投放时,误投了过氧化氢(H2O2)消毒剂。消毒剂为什么不起作用了?
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐3】化学小组同学为探究氯水的成分及性质进行了如下实验:
(试管中溶液均为1mL,均滴入氯水5滴)
(1)实验②中反应方程式为___________ ,由此推断氧化性
___________  (填“>”或“<”)
(填“>”或“<”)
(2)实验③中溶液变红是由于溶液中含有___________ (填微粒符号,下同);使溶液褪色的微粒是___________ 。
(3)同学们发现久置的氯水会失去漂白性,溶液由黄绿色变为无色。为探究氯水失效的原因,进行实验用强光照射盛有氯水的密闭广口瓶,并用传感器测定广口瓶中数据,
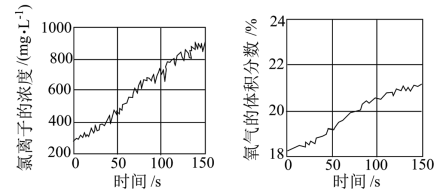
得到如下曲线。
解释上两图中曲线变化的原因___________ 。若在上述整个实验过程中测定溶液的氢离子浓度,氢离子浓度的变化是___________ 。(填“增大”、“减小”或“不变”)
(4)同学们根据“ 在催化剂作用下可发生分解”的性质,认为实验⑤中现象不一定说明氧化性
在催化剂作用下可发生分解”的性质,认为实验⑤中现象不一定说明氧化性 。为证实
。为证实 将
将 氧化,可继续补充实验:
氧化,可继续补充实验:___________ (填操作、现象)。
| 实验① | 实验② | 实验③ | 实验④ | 实验⑤ | |
| 实验操作(氯水均为新制) |  |  | 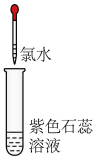 |  |  |
| 实验现象 | 蒸馏水由无色逐渐变为浅黄绿色 | 溶液变蓝 | 石蕊溶液先变红,后褪色 | 产生白色沉淀 | 产生大量无色气泡 |
(1)实验②中反应方程式为

 (填“>”或“<”)
(填“>”或“<”)(2)实验③中溶液变红是由于溶液中含有
(3)同学们发现久置的氯水会失去漂白性,溶液由黄绿色变为无色。为探究氯水失效的原因,进行实验用强光照射盛有氯水的密闭广口瓶,并用传感器测定广口瓶中数据,

得到如下曲线。
解释上两图中曲线变化的原因
(4)同学们根据“
 在催化剂作用下可发生分解”的性质,认为实验⑤中现象不一定说明氧化性
在催化剂作用下可发生分解”的性质,认为实验⑤中现象不一定说明氧化性 。为证实
。为证实 将
将 氧化,可继续补充实验:
氧化,可继续补充实验:
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐1】图中,A为一种中学化学中常见的单质,B、C、D、E是含有A元素的常见化合物。它们的焰色实验均为黄色。
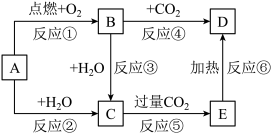
(1)写出下列物质的化学式:B___ 。
(2)以上6个反应中属于氧化还原反应的有___ (填写编号)。
(3)写出A →C反应的离子方程式___ 。
(4)写出B→C反应的离子方程式:___ ;E→D的化学方程式:___ 。
(5)加热5.00gD和E的固体混合物,使E完全分解,固体混合物的质量减少了0.31g,则原混合物中D的质量分数为___ 。

(1)写出下列物质的化学式:B
(2)以上6个反应中属于氧化还原反应的有
(3)写出A →C反应的离子方程式
(4)写出B→C反应的离子方程式:
(5)加热5.00gD和E的固体混合物,使E完全分解,固体混合物的质量减少了0.31g,则原混合物中D的质量分数为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐2】下列图示中,A为一种常见的单质,B、C、D、E是含A元素的常见化合物,B为淡黄色粉末。请填写下列空白:
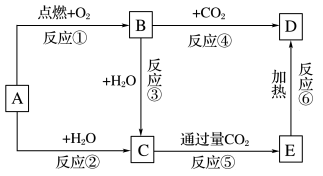
(1)写出下列物质的化学式:A_______ ,B_______ ,C_______ ,D_______ 。
(2)写出下列反应的离子方程式、化学方程式: 离子方程式:
离子方程式:_______ , 化学方程式:
化学方程式:_______ 。
(3)写出B的一种用途:_______ 。

(1)写出下列物质的化学式:A
(2)写出下列反应的离子方程式、化学方程式:
 离子方程式:
离子方程式: 化学方程式:
化学方程式:(3)写出B的一种用途:
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐3】甲、乙两位同学分别设计实验,测定某试样(成分为 及少量不溶性杂质)中
及少量不溶性杂质)中 的质量分数。
的质量分数。
(1)甲同学设计的实验流程如下:

①试样溶解过程中发生反应的化学方程式为___________ 。
②实验中用 盐酸配制
盐酸配制 盐酸,配制时应选用
盐酸,配制时应选用___________ mL量筒;用量筒量取盐酸时仰视读数,会使所配溶液浓度___________ (选填“偏高”“偏低”或“不变”)。
③称取5.12 g试样,得0.10 g滤渣,冷却后称量得固体为5.85 g,则试样中 的质量分数为
的质量分数为___________ 。
(2)乙同学利用如下图所示的装置进行实验。

①实验中应选取的试剂是___________ (填字母)。
a.稀盐酸 b.二氧化锰 c.蒸馏水 d.碳酸钙
②装置的连接顺序应是___________ (填各接口的字母)。
 及少量不溶性杂质)中
及少量不溶性杂质)中 的质量分数。
的质量分数。(1)甲同学设计的实验流程如下:

①试样溶解过程中发生反应的化学方程式为
②实验中用
 盐酸配制
盐酸配制 盐酸,配制时应选用
盐酸,配制时应选用③称取5.12 g试样,得0.10 g滤渣,冷却后称量得固体为5.85 g,则试样中
 的质量分数为
的质量分数为(2)乙同学利用如下图所示的装置进行实验。

①实验中应选取的试剂是
a.稀盐酸 b.二氧化锰 c.蒸馏水 d.碳酸钙
②装置的连接顺序应是
您最近一年使用:0次



