化学反应伴随能量变化,获取反应能量变化有多条途径。
(1)下列反应中,属于吸热反应的是_____(填字母)。
(2)获取能量变化的途径
①通过化学键的键能计算。
已知:
计算可得: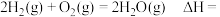
_____ 
若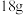 水蒸气转化为液态水放出
水蒸气转化为液态水放出 的热量,则反应
的热量,则反应 的反应热为
的反应热为_____ , 的燃烧热为
的燃烧热为_____
已知
②根据上述数据, 和
和 本身具有的能量最低的是
本身具有的能量最低的是_____
③ 的液态乙醇在氧气中完全燃烧,生成液态水和二氧化碳气体,放出
的液态乙醇在氧气中完全燃烧,生成液态水和二氧化碳气体,放出 的热量,写出该反应的热化学方程式
的热量,写出该反应的热化学方程式_____
(1)下列反应中,属于吸热反应的是_____(填字母)。
A. 与水反应 与水反应 | B.甲烷的燃烧反应 |
C. 与盐酸反应 与盐酸反应 | D.锌与盐酸反应 |
①通过化学键的键能计算。
已知:
| 化学键种类 |  |  |  |  |  |
键能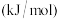 | 436 | 498 | 463.4 | 432 | 366 |
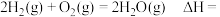

若
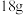 水蒸气转化为液态水放出
水蒸气转化为液态水放出 的热量,则反应
的热量,则反应 的反应热为
的反应热为 的燃烧热为
的燃烧热为已知
②根据上述数据,
 和
和 本身具有的能量最低的是
本身具有的能量最低的是③
 的液态乙醇在氧气中完全燃烧,生成液态水和二氧化碳气体,放出
的液态乙醇在氧气中完全燃烧,生成液态水和二氧化碳气体,放出 的热量,写出该反应的热化学方程式
的热量,写出该反应的热化学方程式
更新时间:2023-10-31 07:00:04
|
相似题推荐
填空题
|
适中
(0.65)
名校
【推荐1】根据下述数据回答:
下表的数据是破坏1mol物质化学键所消耗的能量(kJ)

(1)表氢化物中本身具有的能量最高的是________ ,最稳定的是_______ 。
(2)X2+H2=2HX(X代表Cl、Br、I)的反应是吸热反应还是放热反应?_______
(3)相同条件下,X2(X代表Cl、Br、I)分别与等物质的量氢气反应时放出或吸收能量最多的是_____________ 。
下表的数据是破坏1mol物质化学键所消耗的能量(kJ)

(1)表氢化物中本身具有的能量最高的是
(2)X2+H2=2HX(X代表Cl、Br、I)的反应是吸热反应还是放热反应?
(3)相同条件下,X2(X代表Cl、Br、I)分别与等物质的量氢气反应时放出或吸收能量最多的是
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】 、
、 、C都是优质的能源物质,它们燃烧的热化学方程式分别为
、C都是优质的能源物质,它们燃烧的热化学方程式分别为
①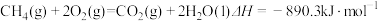
②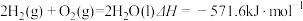
③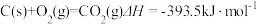
(1)在深海中存在一种甲烷细菌,它们依靠酶使甲烷气体与 作用产生的能量存活,甲烷细菌使
作用产生的能量存活,甲烷细菌使 甲烷气体与
甲烷气体与 反应生成
反应生成 气体与液态水,放出的能量
气体与液态水,放出的能量_____ (填“>”“<”或“=”)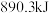 。
。
(2)甲烷气体与 可用于合成水煤气(主要成分是一氧化碳和氢气):
可用于合成水煤气(主要成分是一氧化碳和氢气):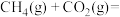
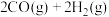 ,
, 完全反应可释放
完全反应可释放 热量,则能表示该反应过程中能量变化的是
热量,则能表示该反应过程中能量变化的是_____ (填标号)。
A.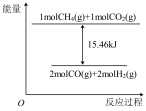 B.
B.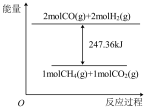 C.
C.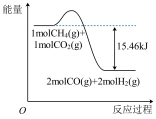 D.
D.
(3)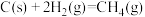 的反应热无法直接测量,但通过上述反应可求出
的反应热无法直接测量,但通过上述反应可求出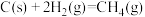 的反应热
的反应热
______ 。
(4)目前对于上述物质的研究是燃料研究的重点,下列关于上述物质的研究方向中可行的是_____ (填标号)。
A. 寻找优质催化剂,使 与
与 反应生成
反应生成 与
与 ,并放出热量
,并放出热量
B. 寻找优质催化剂,在常温常压下使 分解生成
分解生成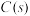 与
与
C. 寻找优质催化剂,利用太阳能使大气中的 与海底开采的
与海底开采的 合成水煤气
合成水煤气
D. 将固态碳合成为 ,以
,以 作为燃料
作为燃料
 、
、 、C都是优质的能源物质,它们燃烧的热化学方程式分别为
、C都是优质的能源物质,它们燃烧的热化学方程式分别为①
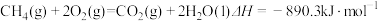
②
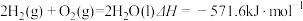
③
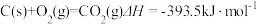
(1)在深海中存在一种甲烷细菌,它们依靠酶使甲烷气体与
 作用产生的能量存活,甲烷细菌使
作用产生的能量存活,甲烷细菌使 甲烷气体与
甲烷气体与 反应生成
反应生成 气体与液态水,放出的能量
气体与液态水,放出的能量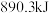 。
。(2)甲烷气体与
 可用于合成水煤气(主要成分是一氧化碳和氢气):
可用于合成水煤气(主要成分是一氧化碳和氢气):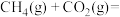
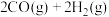 ,
, 完全反应可释放
完全反应可释放 热量,则能表示该反应过程中能量变化的是
热量,则能表示该反应过程中能量变化的是A.
 B.
B. C.
C.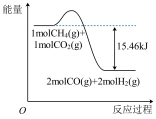 D.
D.
(3)
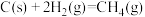 的反应热无法直接测量,但通过上述反应可求出
的反应热无法直接测量,但通过上述反应可求出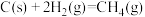 的反应热
的反应热
(4)目前对于上述物质的研究是燃料研究的重点,下列关于上述物质的研究方向中可行的是
A. 寻找优质催化剂,使
 与
与 反应生成
反应生成 与
与 ,并放出热量
,并放出热量B. 寻找优质催化剂,在常温常压下使
 分解生成
分解生成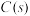 与
与
C. 寻找优质催化剂,利用太阳能使大气中的
 与海底开采的
与海底开采的 合成水煤气
合成水煤气D. 将固态碳合成为
 ,以
,以 作为燃料
作为燃料
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】红磷P(s)和Cl2(g)发生反应生成PCl3(g)和PCl5(g)。反应过程和能量关系如图所示(图中的△H表示生成1mol产物的数据)。

根据上图回答下列问题:
(1)P和Cl2反应生成PCl3的热化学方程式___ 。
(2)PCl5分解成PCl3和Cl2的热化学方程式___ 。
(3)P和Cl2分两步反应生成1molPCl5的△H3=__ ,P和Cl2一步反应生成1molPCl5的△H4___ △H3 (填“大于”、“小于”或“等于”)。
(4)PCl5与足量水充分反应,最终生成两种酸,已知反应前后各元素化合价不变,其化学方程式是__ 。

根据上图回答下列问题:
(1)P和Cl2反应生成PCl3的热化学方程式
(2)PCl5分解成PCl3和Cl2的热化学方程式
(3)P和Cl2分两步反应生成1molPCl5的△H3=
(4)PCl5与足量水充分反应,最终生成两种酸,已知反应前后各元素化合价不变,其化学方程式是
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】1909年,化学家哈伯用N2和H2在高温高压条件下首次合成了氨气,反应原理为N2(g)+3H2(g) 2NH3(g),该反应的能量变化如图所示(a、b均大于零),回答下列问题:
2NH3(g),该反应的能量变化如图所示(a、b均大于零),回答下列问题:

(1)根据图示写出生成2molNH3时的热化学方程式:___ 。
(2)在500℃、30MPa下,断裂11molH—H键、1molN—H键、1molN≡N键需要吸收的能量分别为436kJ、391kJ、946.5kJ。
①每消耗0.6molN2该反应放出的热量为___ 。
②向某一密闭容器中充入1.5molH2(g)和0.5molN2(g),在催化剂条件下进行上述反应,此时断裂的H—H键吸收的热量___ (填“>”、“<”“=”)654 ,原因是
,原因是___ 。
 2NH3(g),该反应的能量变化如图所示(a、b均大于零),回答下列问题:
2NH3(g),该反应的能量变化如图所示(a、b均大于零),回答下列问题:
(1)根据图示写出生成2molNH3时的热化学方程式:
(2)在500℃、30MPa下,断裂11molH—H键、1molN—H键、1molN≡N键需要吸收的能量分别为436kJ、391kJ、946.5kJ。
①每消耗0.6molN2该反应放出的热量为
②向某一密闭容器中充入1.5molH2(g)和0.5molN2(g),在催化剂条件下进行上述反应,此时断裂的H—H键吸收的热量
 ,原因是
,原因是
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】按要求填空:
(1)已知下列反应的反应热为:①CH3COOH(l)+2O2(g)= 2CO2(g)+2H2O(l) △H1= - 870.3 kJ• mol-1
②C(s)+O2(g) = CO2(g) △H= -393.5 kJ• mol-1
③H2(g)+ O2(g) = H2O(l) △H= - 285.8 kJ• mol-1
O2(g) = H2O(l) △H= - 285.8 kJ• mol-1
试计算下列反应的反应热:2C(s)+2H2(g)+O2(g) =CH3COOH(l) △H=_____________ 。
(2) 已知:2Al (s)+ O2(g)= Al2O3(s) △H= -1644.3 kJ• mol-1
O2(g)= Al2O3(s) △H= -1644.3 kJ• mol-1
2Fe (s) + O2(g)= Fe2O3(s) △H= -815.88 kJ• mol-1
O2(g)= Fe2O3(s) △H= -815.88 kJ• mol-1
试写出铝粉与氧化铁粉末发生铝热反应的热化学方程式___________________________ 。
(3)大气中的部分碘源于O3对海水中Ⅰ-的氧化。将O3持续通入NaI溶液中进行模拟研究 O3将I — 氧化成I2 的过程由3步反应组成: ① I —(aq)+ O3(g)= ⅠO—(aq)+O2(g) △H1
②ⅠO—(aq)+ H+(aq) HOI (aq) △H2
HOI (aq) △H2
③ HIO(aq) + I—(aq) + H+(aq) I2(aq) + H2O(l) △H3
I2(aq) + H2O(l) △H3
总反应的离子方程式为_______________________________ ,反应热为 _______________ (用含△H1、△H2、△H3 的式子表示)。
(1)已知下列反应的反应热为:①CH3COOH(l)+2O2(g)= 2CO2(g)+2H2O(l) △H1= - 870.3 kJ• mol-1
②C(s)+O2(g) = CO2(g) △H= -393.5 kJ• mol-1
③H2(g)+
 O2(g) = H2O(l) △H= - 285.8 kJ• mol-1
O2(g) = H2O(l) △H= - 285.8 kJ• mol-1 试计算下列反应的反应热:2C(s)+2H2(g)+O2(g) =CH3COOH(l) △H=
(2) 已知:2Al (s)+
 O2(g)= Al2O3(s) △H= -1644.3 kJ• mol-1
O2(g)= Al2O3(s) △H= -1644.3 kJ• mol-12Fe (s) +
 O2(g)= Fe2O3(s) △H= -815.88 kJ• mol-1
O2(g)= Fe2O3(s) △H= -815.88 kJ• mol-1试写出铝粉与氧化铁粉末发生铝热反应的热化学方程式
(3)大气中的部分碘源于O3对海水中Ⅰ-的氧化。将O3持续通入NaI溶液中进行模拟研究 O3将I — 氧化成I2 的过程由3步反应组成: ① I —(aq)+ O3(g)= ⅠO—(aq)+O2(g) △H1
②ⅠO—(aq)+ H+(aq)
 HOI (aq) △H2
HOI (aq) △H2 ③ HIO(aq) + I—(aq) + H+(aq)
 I2(aq) + H2O(l) △H3
I2(aq) + H2O(l) △H3总反应的离子方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】盖斯定律的应用
利用已知反应焓变求未知反应焓变。
一个反应的化学方程式可由另外几个化学方程式相加减得到,则该化学反应的焓变也可以由几个化学反应焓变的_____ 而得到。
恒压条件下,化学反应的反应热仅与反应的_____ 和_____ 有关,而与反应的_____ 无关。如图所示:
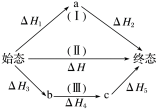
ΔH=_____ =_____
利用已知反应焓变求未知反应焓变。
一个反应的化学方程式可由另外几个化学方程式相加减得到,则该化学反应的焓变也可以由几个化学反应焓变的
恒压条件下,化学反应的反应热仅与反应的

ΔH=
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】次氯酸钠氧化法可以制备Na2FeO4。
已知:2H2(g)+O2(g)=2H2O(l) ΔH=akJ·mol-1
NaCl(aq)+H2O(l)=NaClO(aq)+H2(g) ΔH=bkJ·mol-1
4Na2FeO4(aq)+10H2O(l)=4Fe(OH)3(s)+3O2(g)+8NaOH(aq) ΔH=ckJ·mol-1
反应2Fe(OH)3(s)+3NaClO(aq)+4NaOH(aq)=2Na2FeO4(aq)+3NaCl(aq)+5H2O(l)的ΔH=_____ kJ·mol-1.
已知:2H2(g)+O2(g)=2H2O(l) ΔH=akJ·mol-1
NaCl(aq)+H2O(l)=NaClO(aq)+H2(g) ΔH=bkJ·mol-1
4Na2FeO4(aq)+10H2O(l)=4Fe(OH)3(s)+3O2(g)+8NaOH(aq) ΔH=ckJ·mol-1
反应2Fe(OH)3(s)+3NaClO(aq)+4NaOH(aq)=2Na2FeO4(aq)+3NaCl(aq)+5H2O(l)的ΔH=
您最近一年使用:0次

 CO(g)+3H2(g) △H=+206.2kJ•mol-1
CO(g)+3H2(g) △H=+206.2kJ•mol-1

