如图所示的无机物的转化关系中,部分生成物和反应条件已略去。其中A与F是两种酸式盐;常温下B、C、Y、Z是气体,且B能使Z的水溶液褪色;E是一种常见的化肥;X中含有20个电子。
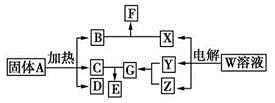
(1)写出X的电子式:________________ ;E中含有的化学键类型是________________ 。
(2)Z与C以物质的量之比31反应也能生成G,同时生成另一种二元化合物H,已知该反应 中只有一种元素的化合价发生改变,则H的化学式为________________ 。H大量用于面粉的漂白和消毒,它与水反应的化学方程式为________________ 。
(3)将体积均为560 mL(标准状况)的B和Z同时缓缓通入水中,得到1.0 L溶液,则溶液中c(H + )=________ mol/L。
(4)A~G七种物质中,属于电解质的有________ 种。

(1)写出X的电子式:
(2)Z与C以物质的量之比31反应也能生成G,同时生成另一种二元化合物H,已知该反应 中只有一种元素的化合价发生改变,则H的化学式为
(3)将体积均为560 mL(标准状况)的B和Z同时缓缓通入水中,得到1.0 L溶液,则溶液中c(H + )=
(4)A~G七种物质中,属于电解质的有
2014高三·全国·专题练习 查看更多[2]
更新时间:2016-12-09 05:59:45
|
相似题推荐
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐1】化合物X是日常生活中的一种常用调味品。已知物质A、B、C、D、E、F有如图所示的转化关系:
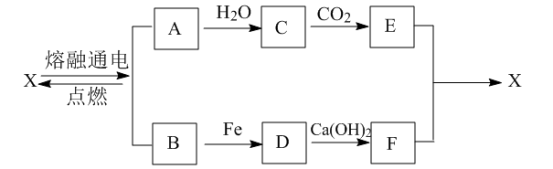
(1)A、B、C、D、E、F中不属于电解质的是__ (填化学式,下同),属于电解质且水溶液显碱性的是__ 。
(2)A→C反应的化学方程式为__ 。
(3)B→D反应的化学方程式为__ ,反应现象为___ 。
(4)写出B与石灰乳[Ca(OH)2]反应的化学方程式:__ ,产物中__ (填化学式)为漂白粉的有效成分。

(1)A、B、C、D、E、F中不属于电解质的是
(2)A→C反应的化学方程式为
(3)B→D反应的化学方程式为
(4)写出B与石灰乳[Ca(OH)2]反应的化学方程式:
您最近一年使用:0次
【推荐2】实验兴趣小组为探究电解质的导电性做了如下实验。根据所学知识回答下列问题:
(1)实验一:灯泡________ ;(填“发光”或“不发光”,下同);实验二:灯泡________ 。
(2)干燥的KNO3固体、NaCl固体、蒸馏水都___________ ;(填“导电”或“不导电”)但是KNO3溶液、NaCl溶液却能够 ___________ 。(填“导电”或“不导电”)
| 实验操作 | 实验一:向三个烧杯中分别加入硝KNO3固体、NaCl固体和蒸馏水。按照右图所示连接装置,将石墨电极伸入到烧杯中,观察并记录现象 实验二:将少量KNO3固体和NaCl固体加入盛有水的烧杯中,搅拌使其完全溶解转化为相应的溶液,重复上述的实验,观察并记录现象 |
|
| 实验现象 | 实验一:灯泡___________;(填“发光”或“不发光”) 实验二:灯泡___________。(填“发光”或“不发光”) | |
| 实验结论 | 干燥的KNO3固体、NaCl固体、蒸馏水都___________;(填“导电”或“不导电”)但是KNO3溶液、NaCl溶液却能够 ___________ 。(填“导电”或“不导电”) | |
(1)实验一:灯泡
(2)干燥的KNO3固体、NaCl固体、蒸馏水都
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐1】某化学小组欲测定 溶液与
溶液与 溶液反应的化学反应速率,所用试剂为10 mL 0.1 mol⋅L-1
溶液反应的化学反应速率,所用试剂为10 mL 0.1 mol⋅L-1 溶液和10 mL 0.3 mol⋅L-1
溶液和10 mL 0.3 mol⋅L-1 溶液,所得溶液中
溶液,所得溶液中 随时间变化的曲线如图1所示,用
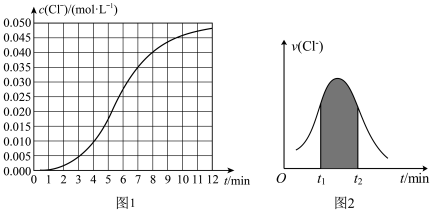
随时间变化的曲线如图1所示,用 表示的反应速率随时间的变化情况如图2所示。
表示的反应速率随时间的变化情况如图2所示。
(1)配平该反应的化学方程式:_________ 。
_______ ______
______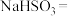 _____
_____ ______
______ _______。
_______。
(2)根据实验数据可知,该反应在0∼7 min内的平均反应速率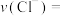
_______ mol⋅L-1∙min-1 。
(3)图2中阴影部分面积表示的是_______ 。
(4)分析图2发现,在反应过程中,该反应的反应速率先增大后减小。对于反应速率先增大的原因该小组进行如下探究实验。已知 对该反应的反应速率无影响。
对该反应的反应速率无影响。
实验1:向2个烧杯中分别加入10 mL 0.1 mol⋅L-1 溶液和10 mL 0.3 mol⋅L-1
溶液和10 mL 0.3 mol⋅L-1 溶液,将其中一个烧杯在50℃下进行反应。
溶液,将其中一个烧杯在50℃下进行反应。
实验2:分别向2个烧杯中加入10 mL 0.1 mol⋅L-1 溶液;向烧杯ⅰ中加入1 mL蒸馏水,向烧杯ⅱ中加入1 mL 0.1 mol⋅L-1
溶液;向烧杯ⅰ中加入1 mL蒸馏水,向烧杯ⅱ中加入1 mL 0.1 mol⋅L-1 溶液;再分别向2个烧杯中加入10 mL 0.3 mol⋅L-1
溶液;再分别向2个烧杯中加入10 mL 0.3 mol⋅L-1 溶液。
溶液。
实验3:取10 mL 0.1 mol⋅L-1 溶液于烧杯中,先加入少量NaCl固体,再加入10 mL 0.3 mol⋅L-1
溶液于烧杯中,先加入少量NaCl固体,再加入10 mL 0.3 mol⋅L-1 溶液。
溶液。
①实验1探究的是_______ ,可以用_______ 的方法控制温度为50℃。
②实验2中,向烧杯ⅰ中加入1 mL蒸馏水的作用是_______ 。
③实验3探究的可能是_______ 。
 溶液与
溶液与 溶液反应的化学反应速率,所用试剂为10 mL 0.1 mol⋅L-1
溶液反应的化学反应速率,所用试剂为10 mL 0.1 mol⋅L-1 溶液和10 mL 0.3 mol⋅L-1
溶液和10 mL 0.3 mol⋅L-1 溶液,所得溶液中
溶液,所得溶液中 随时间变化的曲线如图1所示,用
随时间变化的曲线如图1所示,用 表示的反应速率随时间的变化情况如图2所示。
表示的反应速率随时间的变化情况如图2所示。
(1)配平该反应的化学方程式:
_______
 ______
______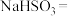 _____
_____ ______
______ _______。
_______。(2)根据实验数据可知,该反应在0∼7 min内的平均反应速率
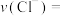
(3)图2中阴影部分面积表示的是
(4)分析图2发现,在反应过程中,该反应的反应速率先增大后减小。对于反应速率先增大的原因该小组进行如下探究实验。已知
 对该反应的反应速率无影响。
对该反应的反应速率无影响。实验1:向2个烧杯中分别加入10 mL 0.1 mol⋅L-1
 溶液和10 mL 0.3 mol⋅L-1
溶液和10 mL 0.3 mol⋅L-1 溶液,将其中一个烧杯在50℃下进行反应。
溶液,将其中一个烧杯在50℃下进行反应。实验2:分别向2个烧杯中加入10 mL 0.1 mol⋅L-1
 溶液;向烧杯ⅰ中加入1 mL蒸馏水,向烧杯ⅱ中加入1 mL 0.1 mol⋅L-1
溶液;向烧杯ⅰ中加入1 mL蒸馏水,向烧杯ⅱ中加入1 mL 0.1 mol⋅L-1 溶液;再分别向2个烧杯中加入10 mL 0.3 mol⋅L-1
溶液;再分别向2个烧杯中加入10 mL 0.3 mol⋅L-1 溶液。
溶液。实验3:取10 mL 0.1 mol⋅L-1
 溶液于烧杯中,先加入少量NaCl固体,再加入10 mL 0.3 mol⋅L-1
溶液于烧杯中,先加入少量NaCl固体,再加入10 mL 0.3 mol⋅L-1 溶液。
溶液。①实验1探究的是
②实验2中,向烧杯ⅰ中加入1 mL蒸馏水的作用是
③实验3探究的可能是
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐2】三氧化二砷(As2O3)是重要的化工原料,某以含砷废水制备三氧化二砷的流程如下。

资料:
ⅰ.含砷废水的主要成分: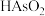 (亚砷酸)、
(亚砷酸)、 、
、 、
、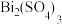 (硫酸铋)。
(硫酸铋)。
ⅱ.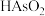 是可溶的弱酸,
是可溶的弱酸, 、
、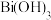 均为难溶沉淀。
均为难溶沉淀。
(1)纯化
充分反应后,分离出精制含砷废水的方法是_____ 。
(2)沉砷
①沉砷过程中由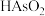 生成
生成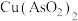 的离子方程式为
的离子方程式为_____ 。
②沉砷过程中按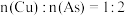 加入
加入 [
[ 与
与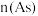 分别表示Cu元素与As元素的物质的量],同时需小心调控溶液的pH,pH过高会导致砷的沉淀率降低,其原因可能是
分别表示Cu元素与As元素的物质的量],同时需小心调控溶液的pH,pH过高会导致砷的沉淀率降低,其原因可能是_____ 。
(3)还原浸出
①补全还原浸出过程发生主要反应的化学方程式:_____ 。
 _____
_____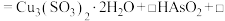 _____
_____
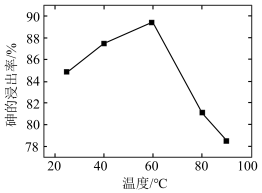
②其他条件相同时,还原浸出 ,不同温度下砷的浸出率如下图。随着温度升高,砷的漫出率先增大后减小的原因是
,不同温度下砷的浸出率如下图。随着温度升高,砷的漫出率先增大后减小的原因是_____ 。
(4)还原渣经过充分氧化处理,可返回_____ (填字母)工序,循环利用。
a.纯化 b.沉砷 c.还原浸出

资料:
ⅰ.含砷废水的主要成分:
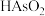 (亚砷酸)、
(亚砷酸)、 、
、 、
、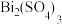 (硫酸铋)。
(硫酸铋)。ⅱ.
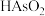 是可溶的弱酸,
是可溶的弱酸, 、
、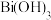 均为难溶沉淀。
均为难溶沉淀。(1)纯化
充分反应后,分离出精制含砷废水的方法是
(2)沉砷
①沉砷过程中由
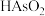 生成
生成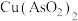 的离子方程式为
的离子方程式为②沉砷过程中按
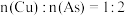 加入
加入 [
[ 与
与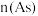 分别表示Cu元素与As元素的物质的量],同时需小心调控溶液的pH,pH过高会导致砷的沉淀率降低,其原因可能是
分别表示Cu元素与As元素的物质的量],同时需小心调控溶液的pH,pH过高会导致砷的沉淀率降低,其原因可能是(3)还原浸出
①补全还原浸出过程发生主要反应的化学方程式:
 _____
_____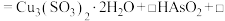 _____
_____②其他条件相同时,还原浸出
 ,不同温度下砷的浸出率如下图。随着温度升高,砷的漫出率先增大后减小的原因是
,不同温度下砷的浸出率如下图。随着温度升高,砷的漫出率先增大后减小的原因是
(4)还原渣经过充分氧化处理,可返回
a.纯化 b.沉砷 c.还原浸出
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐3】Ⅰ.配470 mL 0.10 mol/L  溶液,请回答下列问题:
溶液,请回答下列问题:
(1)计算需要 的质量为
的质量为___________ g。
(2)配制溶液时,现有天平、药匙、烧杯、量筒、玻璃棒,还需要的玻璃仪器有___________ 和___________ (填名称)。
(3)在此配制过程中,下列情况会使所得溶液的浓度偏高的是___________ (填序号)。
A.转移溶液时未洗涤烧杯和玻璃棒
B.定容时俯视刻度线观察液面
C.容量瓶用蒸馏水洗净后未干燥
D.称量固体时,砝码上沾有杂质
E.摇匀后静置,发现液面低于刻度线,再补加蒸馏水至刻度线
Ⅱ. 、
、 、
、 、
、 、
、 、
、 组成的一个氧化还原反应体系中,发生
组成的一个氧化还原反应体系中,发生 的反应过程。
的反应过程。
(4)①将以上物质分别填入下面对应的横线上,并配平化学方程式:________
___________+___________+___________=___________+___________+___________
②氧化剂是___________ 氧化产物是___________
③反应中若产生0.2 mol的还原产物,则有___________ mol电子转移。
 溶液,请回答下列问题:
溶液,请回答下列问题:(1)计算需要
 的质量为
的质量为(2)配制溶液时,现有天平、药匙、烧杯、量筒、玻璃棒,还需要的玻璃仪器有
(3)在此配制过程中,下列情况会使所得溶液的浓度偏高的是
A.转移溶液时未洗涤烧杯和玻璃棒
B.定容时俯视刻度线观察液面
C.容量瓶用蒸馏水洗净后未干燥
D.称量固体时,砝码上沾有杂质
E.摇匀后静置,发现液面低于刻度线,再补加蒸馏水至刻度线
Ⅱ.
 、
、 、
、 、
、 、
、 、
、 组成的一个氧化还原反应体系中,发生
组成的一个氧化还原反应体系中,发生 的反应过程。
的反应过程。(4)①将以上物质分别填入下面对应的横线上,并配平化学方程式:
___________+___________+___________=___________+___________+___________
②氧化剂是
③反应中若产生0.2 mol的还原产物,则有
您最近一年使用:0次
【推荐1】某溶液X中只可能含有 、Fe2+、Al3+、
、Fe2+、Al3+、 、
、 、Cl-、
、Cl-、 中的若干种。某研究性小组为探究该溶液的组成,进行了如下实验:
中的若干种。某研究性小组为探究该溶液的组成,进行了如下实验:
实验Ⅰ.取2000mL溶液X,加入足量的浓NaOH溶液并加热,共收集到5.6L(已换算成标准状况)气体A,反应结束后无沉淀产生;往反应后的溶液中通入足量CO2,充分反应后生成19.5g沉淀B。
实验Ⅱ.另取200mL溶液X,加入足量2mol·L-1BaCl2溶液,充分反应后生成58.25g白色沉淀C;将沉淀C加入盐酸中,无明显现象。
实验Ⅲ.另取200mL溶液X,加入盐酸酸化的FeCl2溶液,无明显现象。
请回答下列问题:
(1)实验过程中需要用BaCl2固体配制250mL2mol·L-1BaCl2溶液,需要用到的玻璃仪器有烧杯、量筒、玻璃棒、胶头滴管、___________ ,玻璃棒的作用为___________ 。
(2)实验Ⅰ中生成气体A的离子方程式为___________ ;沉淀B为___________ (填化学式);19.5g沉淀B的物质的量为___________ mol。
(3)实验Ⅱ中生成白色沉淀C后进行的操作为___________ 、___________ 、干燥、称量;由实验Ⅱ可知溶液X中含有___________ (填离子符号),溶液X中该离子的物质的量浓度为___________ mol/L。
(4)通过实验Ⅲ可知溶液X中一定不含有 ,理由是
,理由是___________ 。
 、Fe2+、Al3+、
、Fe2+、Al3+、 、
、 、Cl-、
、Cl-、 中的若干种。某研究性小组为探究该溶液的组成,进行了如下实验:
中的若干种。某研究性小组为探究该溶液的组成,进行了如下实验:实验Ⅰ.取2000mL溶液X,加入足量的浓NaOH溶液并加热,共收集到5.6L(已换算成标准状况)气体A,反应结束后无沉淀产生;往反应后的溶液中通入足量CO2,充分反应后生成19.5g沉淀B。
实验Ⅱ.另取200mL溶液X,加入足量2mol·L-1BaCl2溶液,充分反应后生成58.25g白色沉淀C;将沉淀C加入盐酸中,无明显现象。
实验Ⅲ.另取200mL溶液X,加入盐酸酸化的FeCl2溶液,无明显现象。
请回答下列问题:
(1)实验过程中需要用BaCl2固体配制250mL2mol·L-1BaCl2溶液,需要用到的玻璃仪器有烧杯、量筒、玻璃棒、胶头滴管、
(2)实验Ⅰ中生成气体A的离子方程式为
(3)实验Ⅱ中生成白色沉淀C后进行的操作为
(4)通过实验Ⅲ可知溶液X中一定不含有
 ,理由是
,理由是
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
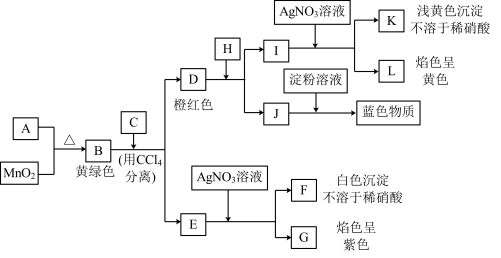
【推荐2】各物质之间的转化关系如下图,部分生成物省略。C、D是由X、Y、Z中两种元素组成的化合物,X、Y、Z的原子序数依次增大,在周期表中X的原子半径最小,Y、Z原子最外层电子数之和为10。D为无色非可燃性气体,G为黄绿色单质气体,J、M为金属,I有漂白作用,反应①常用于制作印刷电路板。
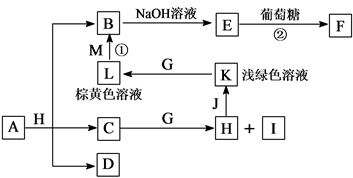
请回答下列问题:
(1)写出A的化学式______________ ,C的电子式______________ 。
(2)比较Y与Z的原子半径大小:_________ >_______ (填写元素符号)。
(3)已知F溶于稀硝酸,溶液变成蓝色,放出无色气体。请写出该反应的化学方程式
_______________________________________________ 。
(4)研究表明:气体D在一定条件下可被还原为晶莹透明的晶体N,其结构中原子的排列为正四面体,请写出N及其2种同素异形体的名称____ 、______ 、_______ 。
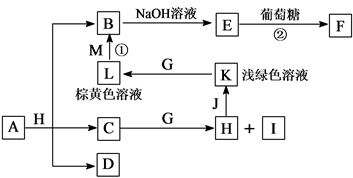
请回答下列问题:
(1)写出A的化学式
(2)比较Y与Z的原子半径大小:
(3)已知F溶于稀硝酸,溶液变成蓝色,放出无色气体。请写出该反应的化学方程式
(4)研究表明:气体D在一定条件下可被还原为晶莹透明的晶体N,其结构中原子的排列为正四面体,请写出N及其2种同素异形体的名称
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐1】(1)普鲁士蓝的化学式是KFe[Fe(CN)6],该物质的化学键有离子键、共价键和_____ 。
(2)KOCN是离子晶体;碳原子采取sp杂化,1mol该物质中含有的π键数目为____ 。
(3)H2O2常温下是液体,沸点较高(150℃),其主要原因是____ 。
(4)非金属元素 的第一电离能大于
的第一电离能大于 的第一电离能,原因是
的第一电离能,原因是______ 。
(5)V2O5溶于NaOH溶液,可得到钒酸钠(Na3VO4),该盐阴离子的立体构型为________ 。
(6)已知食盐的密度为ρ g·cm-3,其摩尔质量为M g·mol-1,阿伏加 德罗常数为NA,则在食盐晶体晶胞参数是_______ cm。
(7)1 mol SiO2晶体中含________ mol Si—O键。
(8)1 mol NH4BF4含有________ mol配位键。
(9)冰、金刚石、MgO、CaCl2、干冰5种晶体的熔点由高到低的顺序为:_____________ 。
(10)体心立方结构的金属如:Na、K、Fe的晶胞的空间占有率表达式为________ (含π)。
(2)KOCN是离子晶体;碳原子采取sp杂化,1mol该物质中含有的π键数目为
(3)H2O2常温下是液体,沸点较高(150℃),其主要原因是
(4)非金属元素
 的第一电离能大于
的第一电离能大于 的第一电离能,原因是
的第一电离能,原因是(5)V2O5溶于NaOH溶液,可得到钒酸钠(Na3VO4),该盐阴离子的立体构型为
(6)已知食盐的密度为ρ g·cm-3,其摩尔质量为M g·mol-1,阿伏加 德罗常数为NA,则在食盐晶体晶胞参数是
(7)1 mol SiO2晶体中含
(8)1 mol NH4BF4含有
(9)冰、金刚石、MgO、CaCl2、干冰5种晶体的熔点由高到低的顺序为:
(10)体心立方结构的金属如:Na、K、Fe的晶胞的空间占有率表达式为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
【推荐2】A、B、C、D、E、F 六种短周期主族元素,它们的原子序数依次增大。A 与 E 同主族,D 与 F 同主族,且 A 与 D 能形成两种液态化合物;B 的某种单质是自然界中硬度最大的物质,C 与D 形成的化合物是大气常见污染物之一。请回答下列问题:
(1)F 在元素周期表中的位置是_____ ,D、E、F 三种元素简单离子半径由大到小的顺序是________ (用离子符号表示)。
(2)元素 E、F 可形成多原子化合物E2Fx(x ≥ 2)。该化合物中所含的化学键类型是_____ 。
(3)实验室可利用_____ (填试剂名称)清洗附着于试管内壁的 F 单质。
(4)处理含 BC−废水的方法之一是在微生物的作用下,BC−被 D 的单质氧化成 ABD−,同时生成C 的简单氢化物,该反应的离子方程式为_____ 。
(1)F 在元素周期表中的位置是
(2)元素 E、F 可形成多原子化合物E2Fx(x ≥ 2)。该化合物中所含的化学键类型是
(3)实验室可利用
(4)处理含 BC−废水的方法之一是在微生物的作用下,BC−被 D 的单质氧化成 ABD−,同时生成C 的简单氢化物,该反应的离子方程式为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
【推荐3】短周期主族元素A、B、C、D、E在元素周期表中的位置如图所示,A的简单离子半径是同周期元素简单离子中半径最小的。请回答下列问题:

(1)描述D在元素周期表中的位置:_____________________________ 。
(2)在A、B、C、E四种元素最高价氧化物对应的水化物中酸性最强的是__________ (写化学式,下同),非金属最简单气态氢化物最不稳定的是_____________________ 。
(3)写出满足下列条件分子的结构式_________________________
①所有原子最外层是8个电子; ②C和E组成的化合物

(1)描述D在元素周期表中的位置:
(2)在A、B、C、E四种元素最高价氧化物对应的水化物中酸性最强的是
(3)写出满足下列条件分子的结构式
①所有原子最外层是8个电子; ②C和E组成的化合物
您最近一年使用:0次