下列说法正确的是
| A.增大压强,活化分子百分数增多,化学反应速率一定增大 |
| B.C(石墨,s)=C(金刚石,s) ∆H=+1.9 kJ/mol,则金刚石比石墨稳定 |
| C.CaCO3(s)=CaO(s)+CO2(g) ∆H>0,∆S>0,则不论在何种条件下都不可能自发进行 |
| D.用CH3COOH溶液和NaOH溶液反应测定中和热:CH3COOH(aq)+NaOH(aq)=CH3COONa(aq)+H2O(aq) ∆H>-57.3 kJ/mol |
更新时间:2023-11-21 10:33:46
|
相似题推荐
单选题
|
较易
(0.85)
名校
解题方法
【推荐1】下列说法或表示方法正确的是
| A.若将等量的硫蒸气和硫固体分别完全燃烧,后者放出热量多 |
B.由“C(石墨)=C(金刚石)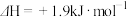 ”可知,金刚石比石墨稳定 ”可知,金刚石比石墨稳定 |
| C.1mol白磷和3mol白磷的燃烧热相等 |
D.在稀溶液中: 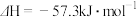 ,若将含1mol ,若将含1mol  与含1mol NaOH的溶液混合,放出的热量等于57.3kJ 与含1mol NaOH的溶液混合,放出的热量等于57.3kJ |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
解题方法
【推荐2】如图是CH4与Zr形成过渡金属化合物的过程。下列说法不正确的是
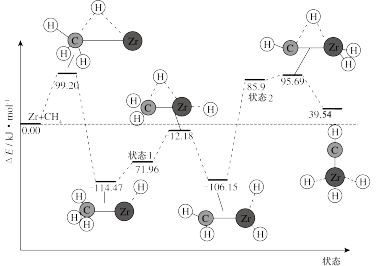

| A.整个反应快慢,由CH2-Zr…H2→状态2反应决定 |
| B.Zr+CH4→CH3-Zr…H活化能为213.6kJ·mol-1 |
| C.在中间产物中CH3-Zr…H状态最稳定 |
| D.Zr+CH4→CH-Zr…H3 ∆H=+39.54 kJ·mol-1 |
您最近一年使用:0次
【推荐3】下列说法或表示法正确的是
| A.H2(g)+Cl2(g)=2HCl(g)要在光照和点燃条件下才反应,所以△H>0,△S<0。 |
| B.由C(s,石墨)=C(s,金刚石);△H=+1.19kJ·mol-1可知,金刚石比石墨稳定 |
| C.在稀溶液中:H+(aq)+OH-(aq)=H2O(1);△H=-57.3kJ·mol-1,若将0.5mol/L的H2SO4溶液1mol/L的NaOH溶液等体积混合,放出的热量等于57.3kJ |
| D.乙醇的燃烧热△H=-1366.8kJ·mol-1,在25℃、101kPa时,92g乙醇充分燃烧后放出2733.6kJ热量 |
您最近一年使用:0次
单选题
|
较易
(0.85)
【推荐1】某实验小组学生按照课本实验要求,用50 mL 0.5 mol/L盐酸与50 mL 0.55 mol/L NaOH溶液在如图所示的装置中进行中和反应,通过测定反应过程中放出的热量计算中和热。下列说法正确的是
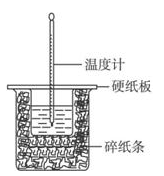

| A.实验过程中没有热量损失 |
| B.图中实验装置缺少环形玻璃搅拌棒 |
| C.烧杯内填满碎纸条的作用是固定小烧杯 |
| D.酸或碱的物质的量越大,所测中和热的数值越大 |
您最近一年使用:0次
单选题
|
较易
(0.85)
解题方法
【推荐2】下列有关热化学反应的描述,正确的是
A.甲醇的燃烧热为△H=-725.76kJ•mol-1,其燃烧热化学方程式为:CH3OH(l)+ O2(g)=CO2(g)+2H2O(g) △H=-725.76kJ•mol-1 O2(g)=CO2(g)+2H2O(g) △H=-725.76kJ•mol-1 |
B.已知2Li2O(s)=4Li(s)+O2(g) △H=+1196kJ•mol-1,则有:2Li(s)+ O2(g)=Li2O(s) △H=-598kJ•mol-1 O2(g)=Li2O(s) △H=-598kJ•mol-1 |
| C.稀盐酸和稀NaOH溶液的反应热△H=-57.3kJ•mol-1,则稀硝酸溶解Cu(OH)2在相同条件下的热化学方程式为:2H+(aq)+Cu(OH)2(s)=Cu2+(aq)+2H2O(l) △H=-114.6kJ•mol-1 |
| D.已知CH3CH2CH2CH3(g)转化为CH3CH(CH3)2(g)的热化学方程式为:CH3CH2CH2CH3(g)=CH3CH(CH3)2(g) △H=-8kJ•mol-1,则稳定性关系为:CH3CH2CH2CH3(g)>CH3CH(CH3)2(g) |
您最近一年使用:0次
单选题
|
较易
(0.85)
解题方法
【推荐3】下列有关热化学方程式及其叙述正确的是
| A.氢气的燃烧热为-285.5kJ/mol,则电解水的热化学方程式为:2H2O(1)=2H2(g)+O2(g)△H=+285.5kJ/mol |
| B.1mol甲烷完全燃烧生成CO2和H2O(l)时放出890kJ热量,则它的热化学方程式为:CH4(g)+2O2(g)=CO2(g)+2H2O(1)△H=-890kJ/mol |
| C.已知:2C(s)+O2(g)=2CO(g)△H=-221kJ•mol-1,则C的燃烧热为-110.5kJ/mol |
| D.HF与NaOH溶液反应:H+(aq)+OH-(aq)=H2O(1)△H=-57.3kJ/mol |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
【推荐1】近日,大连理工大学在《ACS Catal》发文称:合成了一种B/N共掺杂多孔碳纳米管负载的Mo单原子位点(Mo/BCN),该材料在室温下能将 高效电还原为
高效电还原为 。相关机理如图2所示(图1为碳纳米管):
。相关机理如图2所示(图1为碳纳米管):
下列叙述正确的是
 高效电还原为
高效电还原为 。相关机理如图2所示(图1为碳纳米管):
。相关机理如图2所示(图1为碳纳米管):
下列叙述正确的是
| A.碳纳米管是一种新型非金属化合物材料 |
| B.碳纳米管掺杂B、N的过程属于物理变化 |
C.该材料能降低 成为活化分子所需要的能量 成为活化分子所需要的能量 |
| D.该过程属于氮的固定中的自然固氮 |
您最近一年使用:0次
单选题
|
较易
(0.85)
【推荐2】下列说法不正确 的是
| A.发生有效碰撞的分子必须是活化分子 |
| B.采用合适的催化剂可以使一些不自发的化学反应得以实现 |
| C.可以利用物质的颜色变化与浓度变化间的比例关系来测量反应速率 |
| D.反应物和生成物所具有的总能量的相对大小决定了反应是放热还是吸热 |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
【推荐1】下列说法中,正确的是
| A.冰在室温下自动熔化成水,这是熵增的过程 | B.能够自发进行的反应一定是放热反应 |
| C.ΔH > 0的反应均不能自发进行 | D.能够自发进行的反应一定是熵增的过程 |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
解题方法
【推荐2】下列说法正确的是
A.反应N2(g)+3H2(g) 2NH3(g)的△H<0,△S>0 2NH3(g)的△H<0,△S>0 |
| B.反应2CO+2NO=N2+2CO2在常温下能自发进行,则反应的△H>0,△S<0 |
| C.反应4Fe(s)+3O2(g)=2Fe2O3(s)常温下可自发进行,该反应为吸热反应 |
| D.反应TiO2(s)+2Cl2(g)=TiCl4(g)+O2(g) △H>0能自发进行,其原因是△S>0 |
您最近一年使用:0次

 在室温水汽条件下实现高效
在室温水汽条件下实现高效 催化氧化
催化氧化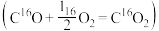 ,其反应历程中相对能量的变化如图所示(
,其反应历程中相对能量的变化如图所示( 分别代表过渡态1、过渡态2、过渡态3),下列说法正确的是
分别代表过渡态1、过渡态2、过渡态3),下列说法正确的是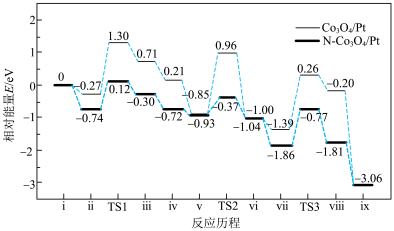
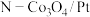 ,故使用催化剂
,故使用催化剂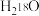 进行同位素标记实验,检测到以上反应中有
进行同位素标记实验,检测到以上反应中有 和
和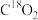 生成,说明反应过程中有
生成,说明反应过程中有 键的断裂
键的断裂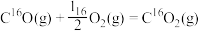 的
的 ,该反应在低温时不能自发进行
,该反应在低温时不能自发进行 被吸附在催化剂表面,则
被吸附在催化剂表面,则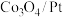 更容易吸附
更容易吸附

