实验室使用标准 溶液测定补铁剂硫酸亚铁片中
溶液测定补铁剂硫酸亚铁片中 的含量,发生反应为
的含量,发生反应为 。加入无色、被氧化后变为紫红色的二苯胺磺酸钠做指示剂。下列说法错误的是
。加入无色、被氧化后变为紫红色的二苯胺磺酸钠做指示剂。下列说法错误的是
 溶液测定补铁剂硫酸亚铁片中
溶液测定补铁剂硫酸亚铁片中 的含量,发生反应为
的含量,发生反应为 。加入无色、被氧化后变为紫红色的二苯胺磺酸钠做指示剂。下列说法错误的是
。加入无色、被氧化后变为紫红色的二苯胺磺酸钠做指示剂。下列说法错误的是| A.将硫酸亚铁片研碎,置于稀硫酸中溶解后过滤 |
| B.标准重铬酸钾液应用酸式滴定管取用 |
C.由实验可知酸性溶液中还原性: 二苯胺磺酸钠 二苯胺磺酸钠 |
D.酸性 溶液与乙醇生成乙酸的离子方程式为: 溶液与乙醇生成乙酸的离子方程式为: |
更新时间:2023-12-12 09:27:26
|
相似题推荐
单选题
|
较易
(0.85)
【推荐1】下列离子方程式正确的是
A.碳酸钙与稀盐酸反应: CO +2H+ = CO2↑+H2O +2H+ = CO2↑+H2O |
| B.AgNO3溶液与KCl溶液混合: Ag+ +Cl- = AgCl↓ |
| C.氢氧化钡与硫酸反应: H++ OH- = H2O |
| D.Fe 与FeCl3溶液反应: Fe + Fe3+= 2Fe2+ |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
解题方法
【推荐2】下列各组的两种物质在溶液中的反应,可用同一离子方程式表示的是
| A.氢氧化钠与盐酸;氢氧化钠与碳酸 |
| B.BaCl2溶液与Na2SO4溶液;Ba(OH)2溶液与NaHSO4溶液 |
| C.Na2CO3溶液与硝酸溶液;CaCO3与硝酸溶液 |
| D.石灰石与硝酸;石灰石与盐酸 |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
【推荐3】下列离子方程式的书写及评价,均合理的是( )
| 选项 | 离子方程式 | 评价 |
| A | 将2 molCl2通入含1 molFeI2的溶液中:2Fe2++2I-+2Cl2===2Fe3++4Cl-+I2 | 正确;Cl2过量,可将Fe2+、I-均氧化 |
| B | Ba(HCO3)2溶液与足量的NaOH溶液反应:Ba2++HCO3-+OH-===BaCO3↓+H2O | 正确;酸式盐与碱反应生成正盐和水 |
| C | 过量SO2通入NaClO溶液中:SO2+H2O+ClO-===HClO+HSO3- | 正确;说明酸性:H2SO3强于HClO |
| D | 将等体积的3.5mol/L的HCl溶液,逐滴加入到1 mol/L的NaAlO2溶液中:6AlO2-+21H+==5Al3++Al(OH)3↓+9H2O | 正确;第一步反应和第二步反应消耗的H+的物质的量之比为2∶5 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
较易
(0.85)
解题方法
【推荐1】绿矾在高温下易分解,用如图所示装置检验绿矾的分解产物(加热装置已略去)。绿矾分解反应的化学方程式为2FeSO4·7H2O Fe2O3+SO2↑+SO3↑+14H2O。已知二氧化硫的沸点为-10℃,三氧化硫的沸点为44.8℃,b为干燥的试管。下列有关说法不正确的是
Fe2O3+SO2↑+SO3↑+14H2O。已知二氧化硫的沸点为-10℃,三氧化硫的沸点为44.8℃,b为干燥的试管。下列有关说法不正确的是

 Fe2O3+SO2↑+SO3↑+14H2O。已知二氧化硫的沸点为-10℃,三氧化硫的沸点为44.8℃,b为干燥的试管。下列有关说法不正确的是
Fe2O3+SO2↑+SO3↑+14H2O。已知二氧化硫的沸点为-10℃,三氧化硫的沸点为44.8℃,b为干燥的试管。下列有关说法不正确的是
| A.SO2是还原产物,Fe2O3是氧化产物 |
| B.b中所得到的溶液中硫酸的质量分数理论上为29.5% |
| C.将反应后的气体通入氯化钡溶液中,产生的沉淀为BaSO3、BaSO4 |
| D.将反应后的气体通入足量硝酸钡溶液中,产生的沉淀只有BaSO4 |
您最近一年使用:0次
单选题
|
较易
(0.85)
解题方法
【推荐2】根据实验目的,下列实验操作及现象、实验结论都正确的是
| 选项 | 实验目的 | 实验操作及现象 | 实验结论 |
| A | 检验久置的 是否变质 是否变质 | 取久置的 粉末,向其中滴加过量盐酸,产生无色气体 粉末,向其中滴加过量盐酸,产生无色气体 |  未完全变质 未完全变质 |
| B | 证明 是弱电解质 是弱电解质 | 用pH计分别测量氨水和氢氧化钠溶液的pH,氨水的pH小 | 是弱电解质 |
| C | 探究淀粉的水解程度 | 将淀粉水解液分成两份。向第一份中先加入NaOH溶液调节溶液至碱性,再加入银氨溶液并水浴加热,出现银镜;向第二份中滴加少量碘水,溶液变蓝色 | 淀粉部分水解 |
| D | 探究卤素单质 、 、 和 和 的氧化性强弱 的氧化性强弱 | 向NaBr溶液中通入过量氯气,溶液变橙色,再滴加淀粉KI溶液,溶液变蓝色 | 氧化性: |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
较易
(0.85)
解题方法
【推荐1】下列实验操作正确且能达到实验目的的是
| A.配制一定物质的量浓度的H2SO4溶液 | B.用酸性KMnO4溶液滴定Na2SO3溶液 | C.除去氯气中的少量氯化氢 | D.制备氨气 |
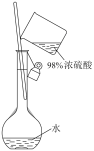 | 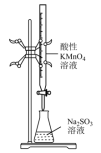 | 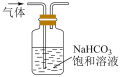 | 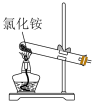 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
较易
(0.85)
【推荐2】利用下列装置和试剂进行实验,能达到实验目的的是
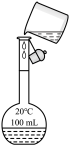 | 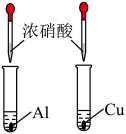 | 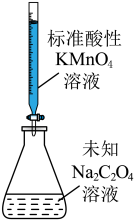 | 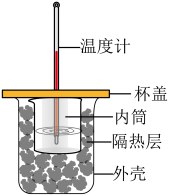 |
| A.向容量瓶中转移溶液 | B.比较Al和Cu的金属活动性 | C.测定未知Na2C2O4溶液的浓度 | D.中和反应反应热的测定 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次

 ,若有
,若有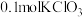 参加反应,下列说法正确的是
参加反应,下列说法正确的是 为
为
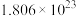 个
个

 溶液(脱碳液)脱除
溶液(脱碳液)脱除 ,脱碳液中含有的
,脱碳液中含有的 能减少溶液对管道的腐蚀。可使用“碘量法”测定脱碳液中
能减少溶液对管道的腐蚀。可使用“碘量法”测定脱碳液中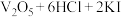
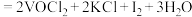 ;
;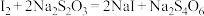 。
。 时,反应转移1mol电子
时,反应转移1mol电子

