高铁电池作为新型可充电电池,具有放电曲线平坦,高能高容量,原料丰富,绿色无污染等优点。如图为简易的高铁电池的工作装置。已知:放电后,两极都产生红褐色悬浮物。
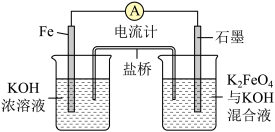
请回答下列问题:
(1)该电池放电时的总反应为___________ 。
(2)该电池充电时阳极反应的电极反应方程式为___________ 。
(3)放电时,此盐桥中阴离子的运动方向是___________ (填“从左向右”或“从右向左”)。

请回答下列问题:
(1)该电池放电时的总反应为
(2)该电池充电时阳极反应的电极反应方程式为
(3)放电时,此盐桥中阴离子的运动方向是
2023高三·全国·专题练习 查看更多[1]
(已下线)电解池 金属的腐蚀与防护
更新时间:2024-01-10 11:16:09
|
相似题推荐
填空题
|
较易
(0.85)
名校
【推荐1】I.应用电化学原理,回答下列问题。
(1)下图中电流计指针偏移时,盐桥(装含琼脂的饱和 溶液)中离子移动的方向:
溶液)中离子移动的方向:___________ 离子移向硫酸锌溶液。
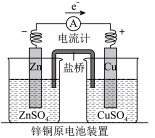
(2)下图中正极反应式为___________ ;若将 换成
换成 ,则负极反应式为
,则负极反应式为___________ 。
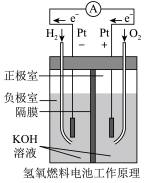
(3)下图中铅蓄电池放电时负极的质量___________ (填“增大”或“减小”),正极反应式为___________
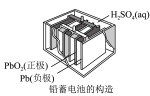
Ⅱ.现有如图所示装置,所有电极均为Pt,请按要求回答下列问题:
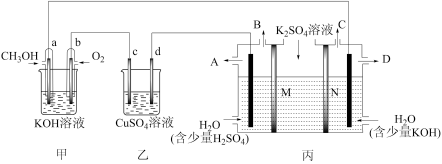
(4)甲装置是___________ (填“原电池”或“电解池”),乙池中c极的电极反应___________
(5)当b极消耗标准状况下的 112mL时,若乙中硫酸铜溶液的体积是200mL,假若电解前后溶液体积保持不变,此时乙池中的pH=
112mL时,若乙中硫酸铜溶液的体积是200mL,假若电解前后溶液体积保持不变,此时乙池中的pH=___________ 。若 (aq)足够,电解一段时间后,要恢复到原来的状态,则可加入
(aq)足够,电解一段时间后,要恢复到原来的状态,则可加入___________ 。
(6)现用丙装置电解硫酸钾溶液制取氢气、氧气、硫酸和氢氧化钾,其中M、N为离子交换膜,只允许某些离子通过,则A出口导出的溶液溶质为___________ (写化学式),N为___________ 离子交换膜(填“阴”或“阳”)。
(1)下图中电流计指针偏移时,盐桥(装含琼脂的饱和
 溶液)中离子移动的方向:
溶液)中离子移动的方向:
(2)下图中正极反应式为
 换成
换成 ,则负极反应式为
,则负极反应式为
(3)下图中铅蓄电池放电时负极的质量

Ⅱ.现有如图所示装置,所有电极均为Pt,请按要求回答下列问题:

(4)甲装置是
(5)当b极消耗标准状况下的
 112mL时,若乙中硫酸铜溶液的体积是200mL,假若电解前后溶液体积保持不变,此时乙池中的pH=
112mL时,若乙中硫酸铜溶液的体积是200mL,假若电解前后溶液体积保持不变,此时乙池中的pH= (aq)足够,电解一段时间后,要恢复到原来的状态,则可加入
(aq)足够,电解一段时间后,要恢复到原来的状态,则可加入(6)现用丙装置电解硫酸钾溶液制取氢气、氧气、硫酸和氢氧化钾,其中M、N为离子交换膜,只允许某些离子通过,则A出口导出的溶液溶质为
您最近半年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐2】如图所示,组成一个原电池。
(1)当电解质溶液为稀硫酸时:
①Fe电极是__ (填“正”或“负”)极,其电极反应为___ 。
②Cu电极是__ 极,其电极反应为___ 。
(2)由铜、锌和稀硫酸组成的原电池中,铜是__ 极,电极反应式是__ ;锌是__ 极,电极反应式是___ 。

(1)当电解质溶液为稀硫酸时:
①Fe电极是
②Cu电极是
(2)由铜、锌和稀硫酸组成的原电池中,铜是
您最近半年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐3】如图为原电池装置示意图:
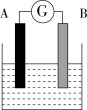
(1)若A为Zn,B为石墨棒,电解质溶液为稀硫酸,则A为________ 极(填正或负),写出电极反应式:正极_______________________ ,负极________________________ .总反应为:____________________ 。
(2)若A为铜片,B为铁片,电解质为FeCl3溶液,则A为________ 极(填正或负),写出电极反应式:正极_____________________________ ,负极________________________ .总反应为:_______________________________ 。
(3)若A、B均为铂片,电解质为KOH溶液,分别从A、B两极通入H2和O2,该电池即为燃料电池,通入氧气的一极为该电池的________ 极(填正或负),该电池的总反应为:____________________

(1)若A为Zn,B为石墨棒,电解质溶液为稀硫酸,则A为
(2)若A为铜片,B为铁片,电解质为FeCl3溶液,则A为
(3)若A、B均为铂片,电解质为KOH溶液,分别从A、B两极通入H2和O2,该电池即为燃料电池,通入氧气的一极为该电池的
您最近半年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐1】铜锌原电池的电极反应式
(1)锌片为_______ 极,发生___________ 反应,电极反应式为________________ ;
(2)铜片为_______ 极,发生__________ 反应,电极反应式为__________________ 。
(3)该反应的总化学方程式为___________________ 。
(1)锌片为
(2)铜片为
(3)该反应的总化学方程式为
您最近半年使用:0次
填空题
|
较易
(0.85)
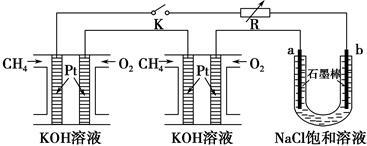
【推荐2】新型高效的甲烷燃料电池采用铂为电极材料,两电极上分别通入CH4和O2,电解质为KOH溶液。某研究小组将两个甲烷燃料电池串联后作为电源,进行饱和氯化钠溶液(滴有几滴酚酞)电解实验,如图所示。
回答下列问题:
(1)甲烷燃料电池正极、负极的电极反应分别为________________________ 、________________________ 。
(2)闭合K开关后,a、b电极上均有气体产生,其中a电极上得到的是________ ;电解过程中________ 极(填“a”或“b”)附近会出现红色。电解氯化钠溶液的总化学方程式为________________________ 。将a、b两极的产物相互反应可得到“84”消毒液的有效成分NaClO,特殊情况下可用“84”消毒液吸收SO2,反应的离子方程式为________________________ 。
(3)若每个电池甲烷通入量为1 L(标准状况),且反应完全,则理论上最多能产生的氯气体积为________ L(标准状况)。

回答下列问题:
(1)甲烷燃料电池正极、负极的电极反应分别为
(2)闭合K开关后,a、b电极上均有气体产生,其中a电极上得到的是
(3)若每个电池甲烷通入量为1 L(标准状况),且反应完全,则理论上最多能产生的氯气体积为
您最近半年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐3】根据所学的知识回答下列问题
(1)将反应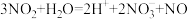 拆写为两个“半反应式”:氧化反应式:
拆写为两个“半反应式”:氧化反应式:_______ ;还原反应式:_______ 。
(2)某化学反应的反应物和产物如下: 。
。
①该反应的氧化剂是_______ 。
②该反应的氧化产物是_______ 。
③配平该反应的化学方程式_______ 。
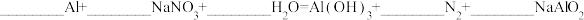 ④反应过程中转移300个e,生成
④反应过程中转移300个e,生成_______ 个 。
。
(3)某化学兴趣小组的同学设计了如图所示的装置,完成下列问题:

①反应过程中,_______ 棒质量减少。
②正极的电极反应为_______ 。
③盐桥的作用是向甲、乙两烧杯中提供 和
和 ,使两烧杯溶液中保持电中性。反应过程中
,使两烧杯溶液中保持电中性。反应过程中 将进入
将进入_______ (填“甲”或“乙”)烧杯。
(1)将反应
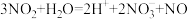 拆写为两个“半反应式”:氧化反应式:
拆写为两个“半反应式”:氧化反应式:(2)某化学反应的反应物和产物如下:
 。
。①该反应的氧化剂是
②该反应的氧化产物是
③配平该反应的化学方程式
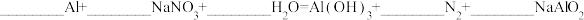 ④反应过程中转移300个e,生成
④反应过程中转移300个e,生成 。
。(3)某化学兴趣小组的同学设计了如图所示的装置,完成下列问题:

①反应过程中,
②正极的电极反应为
③盐桥的作用是向甲、乙两烧杯中提供
 和
和 ,使两烧杯溶液中保持电中性。反应过程中
,使两烧杯溶液中保持电中性。反应过程中 将进入
将进入
您最近半年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐1】为了探究原电池和电解池的工作原理,某研究性学习小组分别用如图所示的装置进行实验,回答下列问题。
Ⅰ.用甲装置进行第一组实验:
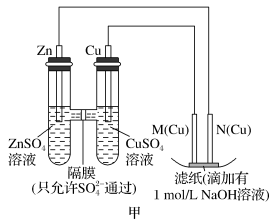
(1)甲装置中电解池在 (左侧或右侧),在保证电极反应不变的情况下,下列材料不能代替左侧Cu电极的是_______(填序号)。
(2)实验过程中,SO
_____ (填“从左向右”“从右向左”或“不”)移动;滤纸上能观察到的现象有_______ 。
Ⅱ.该小组同学用乙装置进行第二组实验时发现,两极均有气体产生,Y极溶液逐渐变成紫红色,停止实验后观察到铁电极明显变细,电解液仍澄清。查阅资料知,高铁酸根离子( )在溶液中呈紫红色。请根据实验现象及所查信息,填写下列空白:
)在溶液中呈紫红色。请根据实验现象及所查信息,填写下列空白:
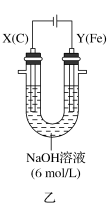
(3)电解过程中,X极溶液的pH_______ (填“增大”“减小”或“不变”)。
(4)电解过程中,Y极发生的电极反应为______ 和_______ 。
(5)已知K2FeO4和Zn可以构成碱性电池,其中K2FeO4在电池中作正极材料,电池总反应为2K2FeO4+3Zn=Fe2O3+ZnO+2K2ZnO2,则该电池正极发生的电极反应为:_______ 。
Ⅰ.用甲装置进行第一组实验:

(1)甲装置中电解池在 (左侧或右侧),在保证电极反应不变的情况下,下列材料不能代替左侧Cu电极的是_______(填序号)。
| A.石墨 | B.镁 | C.银 | D.铂 |

Ⅱ.该小组同学用乙装置进行第二组实验时发现,两极均有气体产生,Y极溶液逐渐变成紫红色,停止实验后观察到铁电极明显变细,电解液仍澄清。查阅资料知,高铁酸根离子(
 )在溶液中呈紫红色。请根据实验现象及所查信息,填写下列空白:
)在溶液中呈紫红色。请根据实验现象及所查信息,填写下列空白:
(3)电解过程中,X极溶液的pH
(4)电解过程中,Y极发生的电极反应为
(5)已知K2FeO4和Zn可以构成碱性电池,其中K2FeO4在电池中作正极材料,电池总反应为2K2FeO4+3Zn=Fe2O3+ZnO+2K2ZnO2,则该电池正极发生的电极反应为:
您最近半年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐2】某同学用下图所示装置研究有关电化学的问题(甲、乙、丙三池中溶质足量),当闭合该装置的电键K时,观察到电流计的指针发生了偏转。

请回答下列问题:
(1)甲池为_________ (填“原电池”、“电解池”或“电镀池”),A电极为_________ (填“正极”、“负极”、“阴极”或“阳极”),其电极反应式为__________ 。
(2)乙池中C极为_________ (填“正极”、“负极”、“阴极”或“阳极”),其电极反应式为__________ 。当池中D极质量增重21.6g时,甲池中B电极理论上消耗O2的体积为_________ L(标准状况)。
(3)丙池中F电极为_______ (填“正极”“负极”、“阴极”或“阳极”),该池的总反应的化学方程式为__________ 。
(4)已知丙池中的溶液为400 mL,合上开关K,一段时间后,丙池中,F极增重1.28 g,若不考虑溶液体积变化,则此时溶液的pH为_______ 。

请回答下列问题:
(1)甲池为
(2)乙池中C极为
(3)丙池中F电极为
(4)已知丙池中的溶液为400 mL,合上开关K,一段时间后,丙池中,F极增重1.28 g,若不考虑溶液体积变化,则此时溶液的pH为
您最近半年使用:0次
填空题
|
较易
(0.85)
解题方法
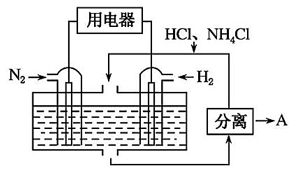
【推荐1】(1)如图表示使用新型电极材料,以N2、H2为电极反应物,以HCl-NH4Cl为电解质溶液制造出既能提供能量,同时又能实现氮固定的新型燃料电池。请写出该电池的正极反应式:___________ 。生产中可分离出的物质A的化学式为:___________ 。
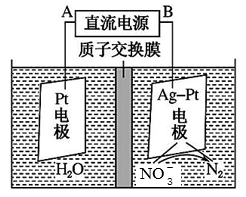
(2)电化学降解治理水中硝酸盐污染。在酸性条件下,电化学降解 的原理如图所示,阴极反应式为
的原理如图所示,阴极反应式为___________ 。假设降解前两极溶液质量相等,当电路中有2mol电子通过时,此时两极溶液质量的差值为___________ g。
(3)科学家制造出一种使用固体电解质的燃料电池,其效率更高,可用于航空航天。如图1所示装置中,以稀土金属材料作惰性电极,在两极上分别通入CH4和空气,其中固体电解质是掺杂了Y2O3的ZrO2固体,它在高温下能传导正极生成的O2−离子。
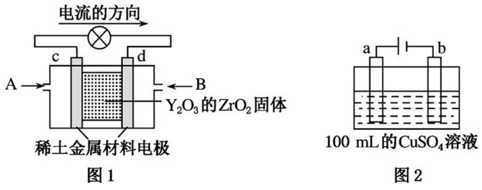
①d电极的名称为___________ ,该电极的电极方程式为:___________ 。
②如图2所示为用惰性电极电解100mL0.5mol·L−1CuSO4溶液,a电极上的电极反应式为___________

(2)电化学降解治理水中硝酸盐污染。在酸性条件下,电化学降解
 的原理如图所示,阴极反应式为
的原理如图所示,阴极反应式为
(3)科学家制造出一种使用固体电解质的燃料电池,其效率更高,可用于航空航天。如图1所示装置中,以稀土金属材料作惰性电极,在两极上分别通入CH4和空气,其中固体电解质是掺杂了Y2O3的ZrO2固体,它在高温下能传导正极生成的O2−离子。

①d电极的名称为
②如图2所示为用惰性电极电解100mL0.5mol·L−1CuSO4溶液,a电极上的电极反应式为
您最近半年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐2】多晶硅是制作光伏电池的关键材料。以下是由粗硅制备多晶硅的简易过程(略)。氢化过程中所需的高纯度H2可用惰性电极电解KOH溶液制备,写出产生H2的电极名称______ (填“阳极”或“阴极”),该电极反应方程式为________________________ 。
您最近半年使用:0次
填空题
|
较易
(0.85)
【推荐3】下图A为直流电源,B为渗透饱和氯化钠溶液和酚酞试液的滤纸,C为电镀槽,接通电路后,发现B 上的 C 点显红色,请填空:
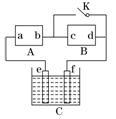
(1)电源A的a为____________ 极。
(2)滤纸B上发生的总反应方程式为:
____________________________________________ 。
(3)欲在电镀槽中实现铁上镀铜,接通K点,使c、d两点短路,则电极e的电极材料为______ ,f极上发生的反应为:___________________________________________ 。

(1)电源A的a为
(2)滤纸B上发生的总反应方程式为:
(3)欲在电镀槽中实现铁上镀铜,接通K点,使c、d两点短路,则电极e的电极材料为
您最近半年使用:0次

 或
或 ,可交替得到
,可交替得到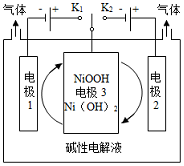
 填“1”或“2”
填“1”或“2” 产生,该电极的反应式为
产生,该电极的反应式为 、101kPa时,
、101kPa时, 完全燃烧生成液态水放出
完全燃烧生成液态水放出 的热量,则
的热量,则 。
。


