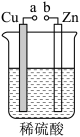
根据所学的知识回答下列问题
(1)将反应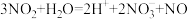 拆写为两个“半反应式”:氧化反应式:
拆写为两个“半反应式”:氧化反应式:_______ ;还原反应式:_______ 。
(2)某化学反应的反应物和产物如下: 。
。
①该反应的氧化剂是_______ 。
②该反应的氧化产物是_______ 。
③配平该反应的化学方程式_______ 。
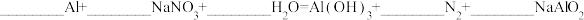 ④反应过程中转移300个e,生成
④反应过程中转移300个e,生成_______ 个 。
。
(3)某化学兴趣小组的同学设计了如图所示的装置,完成下列问题:

①反应过程中,_______ 棒质量减少。
②正极的电极反应为_______ 。
③盐桥的作用是向甲、乙两烧杯中提供 和
和 ,使两烧杯溶液中保持电中性。反应过程中
,使两烧杯溶液中保持电中性。反应过程中 将进入
将进入_______ (填“甲”或“乙”)烧杯。
(1)将反应
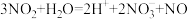 拆写为两个“半反应式”:氧化反应式:
拆写为两个“半反应式”:氧化反应式:(2)某化学反应的反应物和产物如下:
 。
。①该反应的氧化剂是
②该反应的氧化产物是
③配平该反应的化学方程式
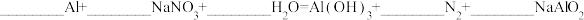 ④反应过程中转移300个e,生成
④反应过程中转移300个e,生成 。
。(3)某化学兴趣小组的同学设计了如图所示的装置,完成下列问题:

①反应过程中,
②正极的电极反应为
③盐桥的作用是向甲、乙两烧杯中提供
 和
和 ,使两烧杯溶液中保持电中性。反应过程中
,使两烧杯溶液中保持电中性。反应过程中 将进入
将进入
更新时间:2023-04-22 21:47:41
|
相似题推荐
填空题
|
较易
(0.85)
解题方法
【推荐1】氧化还原反应的应用比较广泛。阅读下面的材料,结合相关化学知识回答下列问题。
(1)黑火药主要是硝酸钾、硫磺、木炭三种粉末的混合物,在点燃条件下,其爆炸时发生的化学反应主要为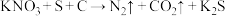 (未配平)。
(未配平)。
①在黑火药爆炸的反应中,氧化剂为_______ ,被氧化的物质为_______ 。
②根据化学方程式分析,一个硫原子参与反应时_______ (填“得到”或“失去”)_______ 个电子。
(2)稀硫酸与铁粉的反应方程式如下,用双线桥法表示该反应中电子转移的方向和数目______ 。
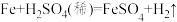
(3)已知存在下列反应:
①
② 。
。
则 、
、 、
、 微粒氧化性由强到弱的顺序是
微粒氧化性由强到弱的顺序是_______ 。
(1)黑火药主要是硝酸钾、硫磺、木炭三种粉末的混合物,在点燃条件下,其爆炸时发生的化学反应主要为
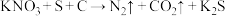 (未配平)。
(未配平)。①在黑火药爆炸的反应中,氧化剂为
②根据化学方程式分析,一个硫原子参与反应时
(2)稀硫酸与铁粉的反应方程式如下,用双线桥法表示该反应中电子转移的方向和数目
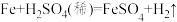
(3)已知存在下列反应:
①

②
 。
。则
 、
、 、
、 微粒氧化性由强到弱的顺序是
微粒氧化性由强到弱的顺序是
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐2】黑火药爆炸反应为:S+2KNO3+3C=K2S+3CO2+N2,在该反应中,被还原的元素为_______ ;还原剂:_______ ;
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐1】现有以下物质:①铜;②氨的水溶液;③硝酸;④  固体;⑤稀硫酸;⑥
固体;⑤稀硫酸;⑥  ;⑦
;⑦  固体;⑧乙醇;⑨
固体;⑧乙醇;⑨  固体;⑩熔融的
固体;⑩熔融的 。
。
(1)能导电的是_____ 。
(2)属于非电解质的是_______ 。
(3)既不属于电解质也不属于非电解质的是______ 。
(4)写出上述物质中②和⑤反应的离子方程式________ 。
(5)请补充完整并配平物质 ①和 ③ 的稀溶液反应的离子方程式:
____ Cu+_____ NO +
+_____ =__ Cu2++ __ NO↑ +____
 固体;⑤稀硫酸;⑥
固体;⑤稀硫酸;⑥  ;⑦
;⑦  固体;⑧乙醇;⑨
固体;⑧乙醇;⑨  固体;⑩熔融的
固体;⑩熔融的 。
。(1)能导电的是
(2)属于非电解质的是
(3)既不属于电解质也不属于非电解质的是
(4)写出上述物质中②和⑤反应的离子方程式
(5)请补充完整并配平物质 ①和 ③ 的稀溶液反应的离子方程式:
 +
+
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐2】(一)某化学兴趣小组为探究元素性质的递变规律,设计了如下系列实验:利用如图装置可以验证元素的非金属性的变化规律。
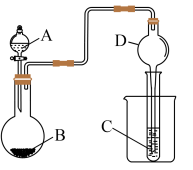
(1)图中:A装置名称是___ ,干燥管D的作用是___ 。
(2)实验室中现有药品Na2S、KMnO4、MnO2、浓盐酸,请从中选择合适药品设计实验验 证氯的非金属性大于硫,烧瓶中发生反应的离子方程式为___ 。
(3)若要用此装置证明酸性:HNO3>H2CO3>H2SiO3,进而证明非金属性:N>C>Si,从以下所给物质中选出甲同学设计的实验所用到物质:
①稀HNO3溶液 ②稀盐酸 ③碳酸钙 ④Na2SiO3溶液 ⑤SiO2
装置A、C中所选试剂分别为__ (填序号);能说明酸性H2CO3>H2SiO3的实验现象是__ 。
(二)四种短周期元素W、X、Y、Z,原子序数依次增大,请回答下列问题。
(1)Z在元素周期表中位于___ 族。
(2)上述元素的最高价氧化物对应的水化物中,有一种物质在一定条件下均能与其他三种物质发生化学反应,该元素是___ (填元素符号)。
(3)①下列可作为比较X和Y金属性强弱的依据是___ (填序号)。
a.自然界中的含量
b.单质与酸反应时失去的电子数
c.单质与水反应的难易程度
d.最高价氧化物对应水化物的碱性
②从原子结构的角度解释X的金属性强于Y的原因:___ 。
(4)W的一种氢化物HW3可用于有机合成,其酸性与醋酸相似。体积和浓度均相等的HW3与X的最高价氧化物对应的水化物混合,反应的化学方程式是__ 。

(1)图中:A装置名称是
(2)实验室中现有药品Na2S、KMnO4、MnO2、浓盐酸,请从中选择合适药品设计实验验 证氯的非金属性大于硫,烧瓶中发生反应的离子方程式为
(3)若要用此装置证明酸性:HNO3>H2CO3>H2SiO3,进而证明非金属性:N>C>Si,从以下所给物质中选出甲同学设计的实验所用到物质:
①稀HNO3溶液 ②稀盐酸 ③碳酸钙 ④Na2SiO3溶液 ⑤SiO2
装置A、C中所选试剂分别为
(二)四种短周期元素W、X、Y、Z,原子序数依次增大,请回答下列问题。
| W | X | Y | Z | |
| 结构或性质 | 最高价氧化物对应的水化物与其气态氢化物反应得到离子化合物 | 焰色反应 呈黄色 | 在同周期主族元素形成的简单离子中,离子半径最小,它的最高价氧化物为两性氧化物 | 最高正价与最低负价之和为零 |
(1)Z在元素周期表中位于
(2)上述元素的最高价氧化物对应的水化物中,有一种物质在一定条件下均能与其他三种物质发生化学反应,该元素是
(3)①下列可作为比较X和Y金属性强弱的依据是
a.自然界中的含量
b.单质与酸反应时失去的电子数
c.单质与水反应的难易程度
d.最高价氧化物对应水化物的碱性
②从原子结构的角度解释X的金属性强于Y的原因:
(4)W的一种氢化物HW3可用于有机合成,其酸性与醋酸相似。体积和浓度均相等的HW3与X的最高价氧化物对应的水化物混合,反应的化学方程式是
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐3】饮用水中的 对人类健康会产生危害,为了降低饮用水中
对人类健康会产生危害,为了降低饮用水中 的浓度,某饮用水研究人员提出:在碱性条件下用铝粉将
的浓度,某饮用水研究人员提出:在碱性条件下用铝粉将 还原为
还原为 :
: 。请回答下列问题:
。请回答下列问题:
(1)请配平其化学方程式并用双线桥表示电子转移的方向和数目:___________ 。
(2)上述反应中,还原剂是___________ ,还原产物是___________ 。
(3)另一种去除污水中 的方法是在酸性污水中加入铁粉,最终生成铵根和FeO(OH),该反应的离子方程式为:
的方法是在酸性污水中加入铁粉,最终生成铵根和FeO(OH),该反应的离子方程式为:___________ 。
 对人类健康会产生危害,为了降低饮用水中
对人类健康会产生危害,为了降低饮用水中 的浓度,某饮用水研究人员提出:在碱性条件下用铝粉将
的浓度,某饮用水研究人员提出:在碱性条件下用铝粉将 还原为
还原为 :
: 。请回答下列问题:
。请回答下列问题:(1)请配平其化学方程式并用双线桥表示电子转移的方向和数目:
(2)上述反应中,还原剂是
(3)另一种去除污水中
 的方法是在酸性污水中加入铁粉,最终生成铵根和FeO(OH),该反应的离子方程式为:
的方法是在酸性污水中加入铁粉,最终生成铵根和FeO(OH),该反应的离子方程式为:
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐1】某校化学研究性学习小组欲设计实验验证Zn、Fe、Cu的金属活动性,他们提出了以下两种方案。请你帮助他们完成有关实验项目:
(1)用三种金属与盐酸反应的现象来判断,实验中除选择大小相同的金属片外,还需要控制___ 、___ 相同;若选用一种盐溶液验证三种金属的活泼性,该试剂为___ 。
(2)某小组同学采用Zn、Fe作为电极,只用一个原电池证明三种金属的活动性,则电解质溶液最好选用___ 。
A.0.5mol·L-1氯化亚铁溶液
B.0.5mol·L-1氯化铜溶液
C.0.5mol·L-1盐酸
D.0.5mol·L-1氯化亚铁和0.5mol·L-1氯化铜混合溶液
(1)用三种金属与盐酸反应的现象来判断,实验中除选择大小相同的金属片外,还需要控制
(2)某小组同学采用Zn、Fe作为电极,只用一个原电池证明三种金属的活动性,则电解质溶液最好选用
A.0.5mol·L-1氯化亚铁溶液
B.0.5mol·L-1氯化铜溶液
C.0.5mol·L-1盐酸
D.0.5mol·L-1氯化亚铁和0.5mol·L-1氯化铜混合溶液
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐2】能源是现代文明的原动力,化学电池在生产生活中有着广泛的应用。
(1)根据构成原电池的本质判断,下列反应可以设计成原电池的是_______ (填标号)。
A.C(s)+H2O(g)=CO(g)+H2(g)
B.NaOH(aq)+HCl(aq)=NaCl(aq)+H2O(l)
C.2CO(g)+O2(g)=2CO2(g)
(2)为了探究化学反应中的能量变化,某同学设计了如图所示两个实验。有关实验现象,下列说法正确的是_______(填标号)。

(3)图Ⅱ中外电路中的电子是从_______ (填“Zn”或“Cu”)电极经导线流向_______ 电极。若反应过程中有0.2 mol电子发生转移,则生成的氢气在标准状况下的体积为_______ 。若电池的总反应为2Fe3++Cu=2Fe2++Cu2+,则负极材料是_______ (填化学式)。
(1)根据构成原电池的本质判断,下列反应可以设计成原电池的是
A.C(s)+H2O(g)=CO(g)+H2(g)
B.NaOH(aq)+HCl(aq)=NaCl(aq)+H2O(l)
C.2CO(g)+O2(g)=2CO2(g)
(2)为了探究化学反应中的能量变化,某同学设计了如图所示两个实验。有关实验现象,下列说法正确的是_______(填标号)。

| A.图Ⅰ和图Ⅱ的气泡均产生于锌棒表面 |
| B.图Ⅱ中产生气体的速率比图Ⅰ快 |
| C.图Ⅰ中温度计的示数高于图Ⅱ的示数 |
| D.图Ⅰ和图Ⅱ中温度计的示数相等,且均高于室温 |
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐1】如图所示,是原电池的装置图。请回答:
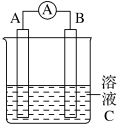
(1)若C为稀H2SO4溶液,电流表指针发生偏转,B电极材料为Fe且做负极,则A电极的材料是_________ (选锌或铜);反应进行一段时间后溶液C的浓度将________ (填“升高”“降低”或“基本不变”)。
(2)若需将反应:Cu+2Fe3+=Cu2++2Fe2+设计成如图所示的原电池装置,则正极电极反应式_________ ,溶液C是________ 。
(3)若C为CuCl2溶液,Zn是________ 极,Cu极发生________ 反应,电极反应为_________ 。反应过程溶液中c(Cu2+)________ (填“变大”“变小”或“不变”)。
(4)CO与H2反应还可制备CH3OH,CH3OH可作为燃料使用,用CH3OH和O2组合形成的质子交换膜燃料电池的结构示意图如图:
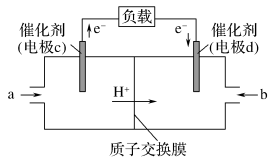
电池总反应为2CH3OH+3O2=2CO2+4H2O,则d电极是_______ (填“正极”或“负极”),c电极的反应方程式为_______ 。d电极反应式______ ,若线路中转移6mol电子,则上述CH3OH燃料电池,消耗的O2在标准状况下的体积为________ L。

(1)若C为稀H2SO4溶液,电流表指针发生偏转,B电极材料为Fe且做负极,则A电极的材料是
(2)若需将反应:Cu+2Fe3+=Cu2++2Fe2+设计成如图所示的原电池装置,则正极电极反应式
(3)若C为CuCl2溶液,Zn是
(4)CO与H2反应还可制备CH3OH,CH3OH可作为燃料使用,用CH3OH和O2组合形成的质子交换膜燃料电池的结构示意图如图:

电池总反应为2CH3OH+3O2=2CO2+4H2O,则d电极是
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐2】氢氧燃料电池是最常见的燃料电池,该电池在正极通入氧气,在负极通入氢气,而电解质溶液通常是KOH溶液。
(1)请写出氢氧燃料电池负极的电极反应方程式___ 。
(2)氢氧燃料电池有何优点:___ 。
(1)请写出氢氧燃料电池负极的电极反应方程式
(2)氢氧燃料电池有何优点:
您最近一年使用:0次

 4NO+6H2O反应。
4NO+6H2O反应。