FeCl3是中学实验室常用的试剂。
(1)写出氯化铁在水中的电离方程式:______ 。
(2)向FeCl3溶液中加入硫氰化钾(KSCN)溶液,溶液变红色。(已知:硫氰化铁为红色)写出该反应的离子方程式______ 。
(3)可利用氯化铁溶液制备氢氧化铁胶体,下列制备氢氧化铁胶体的操作方法正确的是
(4)为了探究离子反应的本质,设计如下实验:

①写出生成A的离子方程式:______ 。
②上述流程中,加入足量稀硝酸的目的是______ 。如何判定无色溶液B与稀硝酸发生了离子反应?______ 。
(1)写出氯化铁在水中的电离方程式:
(2)向FeCl3溶液中加入硫氰化钾(KSCN)溶液,溶液变红色。(已知:硫氰化铁为红色)写出该反应的离子方程式
(3)可利用氯化铁溶液制备氢氧化铁胶体,下列制备氢氧化铁胶体的操作方法正确的是
| A.向饱和氯化铁溶液中滴加适量的氢氧化钠稀溶液 |
| B.加热煮沸氯化铁饱和溶液 |
| C.在氨水中滴加氯化铁浓溶液 |
| D.在沸水中滴加饱和氯化铁溶液,煮沸至出现红褐色液体 |
(4)为了探究离子反应的本质,设计如下实验:

①写出生成A的离子方程式:
②上述流程中,加入足量稀硝酸的目的是
更新时间:2023-12-19 09:31:01
|
相似题推荐
填空题
|
适中
(0.65)
名校
【推荐1】胶体是一种特殊的分散系,有很多特殊的性质。现有下列试剂供选择来制备各种胶体:①饱和FeCl3溶液;②Na2SiO3溶液;③稀盐酸;④蒸馏水;⑤NaOH溶液。
(1)证明有Fe(OH)3胶体生成的实验操作和现象是
(2)制备硅酸胶体所需的试剂为
(3)将上述两种胶体混合,出现的现象是
(4)向Fe(OH)3胶体中逐滴加入HI溶液,出现的现象是先产生沉淀,后沉淀逐渐溶解,写出沉淀溶解的离子反应方程式
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】分类法是学习和研究化学物质的一种常用科学方法。下列“链状连环”图案中,相连的两种物质均可归属为一类,相交部分A、B、C、D为其分类依据代号。请回答:

(1)请将A、B、C、D填入相应的括号内。
( ) 两种物质都是氧化物
( ) 两种物质都是盐
( ) 两种物质都不是电解质
(2)用洁净的烧杯取25mL蒸馏水,加热至沸腾,逐滴加入上图中一种物质的饱和溶液5~6滴,继续加热,制得红褐色的胶体。
①以上反应的化学方程式为_____________________ 。
②简述胶体制取成功的判断依据是___________________ 。
③向该胶体中逐滴加入稀硫酸,观察到:
A.先出现红褐色沉淀,说明胶体发生__________________ 。
B.随后红褐色沉淀溶解,反应的离子方程式是_______________________ 。

(1)请将A、B、C、D填入相应的括号内。
(2)用洁净的烧杯取25mL蒸馏水,加热至沸腾,逐滴加入上图中一种物质的饱和溶液5~6滴,继续加热,制得红褐色的胶体。
①以上反应的化学方程式为
②简述胶体制取成功的判断依据是
③向该胶体中逐滴加入稀硫酸,观察到:
A.先出现红褐色沉淀,说明胶体发生
B.随后红褐色沉淀溶解,反应的离子方程式是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】高铁酸钠( )是水处理过程中的一种新型的绿色多功能净水剂。其净水过程中所发生的化学反应主要为
)是水处理过程中的一种新型的绿色多功能净水剂。其净水过程中所发生的化学反应主要为 。相比传统的用氯气进行水的消毒处理,高铁酸钠安全无异味,投加更方便。请回答下列问题:
。相比传统的用氯气进行水的消毒处理,高铁酸钠安全无异味,投加更方便。请回答下列问题:
(1)高铁酸钠( )属于
)属于___________ (“酸”、“碱”、“盐”或“氧化物”),其中铁的化合价为___________ 价;与 互为同素异形体的物质的化学式为
互为同素异形体的物质的化学式为___________ 。
(2)将上述反应的化学方程式改写成离子方程式___________ ,该反应中物质的氧化性大小关系是:___________ 。
(3)实验室制备 胶体的操作:向烧杯中加入40mL蒸馏水,将烧杯中的蒸馏水加热至沸腾,向沸水中逐滴加入5~6滴
胶体的操作:向烧杯中加入40mL蒸馏水,将烧杯中的蒸馏水加热至沸腾,向沸水中逐滴加入5~6滴___________ 溶液,继续煮沸至溶液呈___________ ,停止加热,写出实验室制备 胶体的化学方程式为
胶体的化学方程式为___________ ,可用___________ 鉴别 胶体与氯化铁溶液。
胶体与氯化铁溶液。
(4)当生成 时,生成的NaOH的质量为
时,生成的NaOH的质量为___________ g。
 )是水处理过程中的一种新型的绿色多功能净水剂。其净水过程中所发生的化学反应主要为
)是水处理过程中的一种新型的绿色多功能净水剂。其净水过程中所发生的化学反应主要为 。相比传统的用氯气进行水的消毒处理,高铁酸钠安全无异味,投加更方便。请回答下列问题:
。相比传统的用氯气进行水的消毒处理,高铁酸钠安全无异味,投加更方便。请回答下列问题:(1)高铁酸钠(
 )属于
)属于 互为同素异形体的物质的化学式为
互为同素异形体的物质的化学式为(2)将上述反应的化学方程式改写成离子方程式
(3)实验室制备
 胶体的操作:向烧杯中加入40mL蒸馏水,将烧杯中的蒸馏水加热至沸腾,向沸水中逐滴加入5~6滴
胶体的操作:向烧杯中加入40mL蒸馏水,将烧杯中的蒸馏水加热至沸腾,向沸水中逐滴加入5~6滴 胶体的化学方程式为
胶体的化学方程式为 胶体与氯化铁溶液。
胶体与氯化铁溶液。(4)当生成
 时,生成的NaOH的质量为
时,生成的NaOH的质量为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】生活离不开化学。家庭厨卫中有许多中学化学常见的物质,下列物质括号内为厨卫物品的主要成分:①食盐 ;②料酒(乙醇);③食醋(乙酸);④碱面
;②料酒(乙醇);③食醋(乙酸);④碱面 ;⑤发酵粉(
;⑤发酵粉( 和酒石酸);⑥“84”消毒液
和酒石酸);⑥“84”消毒液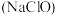 ;⑦洁厕灵
;⑦洁厕灵 。回答下列问题:
。回答下列问题:
(1)写出 在水中的电离方程式:
在水中的电离方程式:_______ 。
(2)当食盐不慎洒落在天然气的火焰上,观察到的现象是_______ 。
(3)②③的主要成分可以归为一类物质,其分类的依据是_______ (填标号)。
A.两种物质都是电解质
B.两种物质都是含碳化合物
C.两种物质都是氧化物
(4)⑥和⑦不能混合使用的原因是_______ (用离子方程式表示)。
(5)用面粉制作馒头的发酵过程中会产生有机酸(一种弱酸),导致口感变差,若在蒸馒头前加入适量④,可使蒸好的馒头松软可口无酸味,用化学方程式解释④的作用:_______ (设有机酸化学式为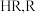 表示有机酸根)。
表示有机酸根)。
(6)欲用 固体配制
固体配制 质量分数为25%、密度为
质量分数为25%、密度为 的“84”消毒液。
的“84”消毒液。
①用电子天平(精确度为 )称量
)称量 的质量为
的质量为_______ g,若配制过程中发现液面超过了刻度线,处理方法为_______ 。
②该“84”消毒液的物质的量浓度约为_______  (保留小数点后一位)。
(保留小数点后一位)。
 ;②料酒(乙醇);③食醋(乙酸);④碱面
;②料酒(乙醇);③食醋(乙酸);④碱面 ;⑤发酵粉(
;⑤发酵粉( 和酒石酸);⑥“84”消毒液
和酒石酸);⑥“84”消毒液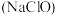 ;⑦洁厕灵
;⑦洁厕灵 。回答下列问题:
。回答下列问题:(1)写出
 在水中的电离方程式:
在水中的电离方程式:(2)当食盐不慎洒落在天然气的火焰上,观察到的现象是
(3)②③的主要成分可以归为一类物质,其分类的依据是
A.两种物质都是电解质
B.两种物质都是含碳化合物
C.两种物质都是氧化物
(4)⑥和⑦不能混合使用的原因是
(5)用面粉制作馒头的发酵过程中会产生有机酸(一种弱酸),导致口感变差,若在蒸馒头前加入适量④,可使蒸好的馒头松软可口无酸味,用化学方程式解释④的作用:
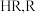 表示有机酸根)。
表示有机酸根)。(6)欲用
 固体配制
固体配制 质量分数为25%、密度为
质量分数为25%、密度为 的“84”消毒液。
的“84”消毒液。①用电子天平(精确度为
 )称量
)称量 的质量为
的质量为②该“84”消毒液的物质的量浓度约为
 (保留小数点后一位)。
(保留小数点后一位)。
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】25℃时,用0.10mol·L-1的氨水滴定 10.00mL0.05 mol·L-1的二元酸 H2Y的溶液,滴定过程中加入氨水的体积(V)与溶液中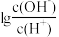 的关系如图所示。下列说法正确的是
的关系如图所示。下列说法正确的是
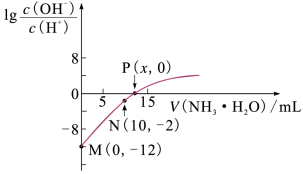
(1)写出H2Y的电离方程式_______
(2)滴定过程中,M、N、P三点对应水电离出的H+浓度由大到小的顺序为_______
(3)用x表示的NH3·H2O电离平衡常数值Kb=_______
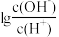 的关系如图所示。下列说法正确的是
的关系如图所示。下列说法正确的是
(1)写出H2Y的电离方程式
(2)滴定过程中,M、N、P三点对应水电离出的H+浓度由大到小的顺序为
(3)用x表示的NH3·H2O电离平衡常数值Kb=
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】按要求回答问题:
(1)KAl(SO4)2的电离方程式_________ 。
(2)向石蕊试液中通入氯气,起始时溶液变红,一段时间后溶液褪色,则使溶液变红和褪色的微粒分别是_________ 、_________ (填微粒符号)。
(3)实验室需配制0.5mol/L的硫酸溶液480mL,在下图所示仪器中,配制上述溶液肯定不需要的是___ (填序号),除图中已有仪器外,配制上述溶液还需要的玻璃仪器是________ 。

(4)化学方程式H2S+H2SO4(浓)=SO2↑+S↓+2H2O,当生成4.48L(标况)SO2时,转移的电子是__________ mol。
(5)下列四个图象中,横坐标表示加入物质的物质的量,纵坐标表示生成沉淀的量或产生气体的量,从A~D中选择符合各题要求的序号填人表中。

(1)KAl(SO4)2的电离方程式
(2)向石蕊试液中通入氯气,起始时溶液变红,一段时间后溶液褪色,则使溶液变红和褪色的微粒分别是
(3)实验室需配制0.5mol/L的硫酸溶液480mL,在下图所示仪器中,配制上述溶液肯定不需要的是

(4)化学方程式H2S+H2SO4(浓)=SO2↑+S↓+2H2O,当生成4.48L(标况)SO2时,转移的电子是
(5)下列四个图象中,横坐标表示加入物质的物质的量,纵坐标表示生成沉淀的量或产生气体的量,从A~D中选择符合各题要求的序号填人表中。

溶液 | 加入的物质 | 序号 |
①AlCl3溶液 | 通入过量的NH3 | |
②Na2CO3和NaOH的溶液 | 滴入过量的盐酸 | |
③NaAlO2溶液 | 滴加稀硫酸至过量 |
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】I.写出下列反应的化学方程式
(1)铁与水蒸气高温反应:_______ ;
(2)用氯化铁溶液刻蚀铜:_______ ;
(3)铜与浓硫酸制 :
:_______ ;
(4) 悬浊液置于空气中:
悬浊液置于空气中:_______ 。
II.写出下列反应的离子方程式
(5)铝与氢氧化钠溶液:_______ ;
(6) 溶于稀硫酸:
溶于稀硫酸:_______ ;
(7)氯化亚铁溶液中通氯气:_______ ;
(8)铜与稀硝酸制NO:_______ 。
(1)铁与水蒸气高温反应:
(2)用氯化铁溶液刻蚀铜:
(3)铜与浓硫酸制
 :
:(4)
 悬浊液置于空气中:
悬浊液置于空气中:II.写出下列反应的
(5)铝与氢氧化钠溶液:
(6)
 溶于稀硫酸:
溶于稀硫酸:(7)氯化亚铁溶液中通氯气:
(8)铜与稀硝酸制NO:
您最近一年使用:0次
填空题
|
适中
(0.64)
【推荐2】根据实验事实,把下列化学方程式改写成离子方程式。
澄清石灰水中加入少量二氧化碳,溶液变浑浊:Ca(OH)2+CO2=CaCO3↓+H2O,离子方程式___________
向氯化镁溶液中滴入氢氧化钠溶液,产生白色的沉淀:MgCl2+2NaOH=Mg(OH)2↓+2NaCl,离子方程式___
向盐酸溶液中加铁:Fe+2HCl=FeCl2+H2↑,离子方程式___________________
澄清石灰水中加入少量二氧化碳,溶液变浑浊:Ca(OH)2+CO2=CaCO3↓+H2O,离子方程式
向氯化镁溶液中滴入氢氧化钠溶液,产生白色的沉淀:MgCl2+2NaOH=Mg(OH)2↓+2NaCl,离子方程式
向盐酸溶液中加铁:Fe+2HCl=FeCl2+H2↑,离子方程式
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】Ⅰ.现有下列物质:①酒精、② 溶液、③稀硫酸、④
溶液、③稀硫酸、④ 、⑤
、⑤ 固体、⑥铁、⑦小苏打、⑧淀粉溶液
固体、⑥铁、⑦小苏打、⑧淀粉溶液
(1)属于电解质的是___________ (填序号,下同),属于非电解质的是___________ 。
(2)②⑧两种分散系的本质区别是___________ 。
(3)胃液中含有盐酸,用⑦治疗胃酸过多的离子方程式为___________ 。
(4)②和⑥反应的离子方程式为___________ 。
(5)将⑤的溶液逐滴加入②中至恰好沉淀完全,反应的离子方程式为___________ 。
Ⅱ.用一种试剂除去下列各物质中的杂质(括号内为杂质)并写出离子方程式。
(6)NaOH溶液[ ],试剂为
],试剂为___________ ,离子方程式为___________ 。
(7) 固体(
固体( ),试剂为
),试剂为___________ ,离子方程式为___________ 。
 溶液、③稀硫酸、④
溶液、③稀硫酸、④ 、⑤
、⑤ 固体、⑥铁、⑦小苏打、⑧淀粉溶液
固体、⑥铁、⑦小苏打、⑧淀粉溶液(1)属于电解质的是
(2)②⑧两种分散系的本质区别是
(3)胃液中含有盐酸,用⑦治疗胃酸过多的离子方程式为
(4)②和⑥反应的离子方程式为
(5)将⑤的溶液逐滴加入②中至恰好沉淀完全,反应的离子方程式为
Ⅱ.用一种试剂除去下列各物质中的杂质(括号内为杂质)并写出离子方程式。
(6)NaOH溶液[
 ],试剂为
],试剂为(7)
 固体(
固体( ),试剂为
),试剂为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】Ⅰ.以下为中学化学常见的物质:①NaOH溶液②铜丝③蔗糖晶体④无水乙醇⑤稀硫酸⑥SO3⑦氨水⑧液态H2S⑨硫酸钡晶体⑩熔融NaCl⑪干冰⑫HCl气体⑬KHSO3溶液
(1)上述状态下可导电的是___ (填序号,下同);
(2)上述状态下的电解质不能导电的是___ 。
(3)上述状态下属于非电解质的是___ 。
(4)写出物质⑬的电离方程式___ 。
(5)⑤和⑦发生反应的离子方程式为___ 。
Ⅱ.按要求填空:
(6)Fe(OH)3胶体是中学常见的胶体,它的制备方法为___ ;制备的化学方程式为___ 。
(7)在酸性条件下,向含铬废水中加入FeSO4,可将Cr2O 还原为Cr3+,该过程的离子方程式为
还原为Cr3+,该过程的离子方程式为___ 。
(8)已知A2O 可将B2-氧化为B单质,A2O
可将B2-氧化为B单质,A2O 则被还原为A3+,又知n个A2O
则被还原为A3+,又知n个A2O 与3n个B2-恰好完全反应,则A2O
与3n个B2-恰好完全反应,则A2O 中的n值为
中的n值为___ 。
(1)上述状态下可导电的是
(2)上述状态下的电解质不能导电的是
(3)上述状态下属于非电解质的是
(4)写出物质⑬的电离方程式
(5)⑤和⑦发生反应的离子方程式为
Ⅱ.按要求填空:
(6)Fe(OH)3胶体是中学常见的胶体,它的制备方法为
(7)在酸性条件下,向含铬废水中加入FeSO4,可将Cr2O
 还原为Cr3+,该过程的离子方程式为
还原为Cr3+,该过程的离子方程式为(8)已知A2O
 可将B2-氧化为B单质,A2O
可将B2-氧化为B单质,A2O 则被还原为A3+,又知n个A2O
则被还原为A3+,又知n个A2O 与3n个B2-恰好完全反应,则A2O
与3n个B2-恰好完全反应,则A2O 中的n值为
中的n值为
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】从废料中制取高纯碳酸钴(CoCO3)的工艺流程如图:

过程Ⅳ沉钴的离子方程式是___ 。

过程Ⅳ沉钴的离子方程式是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】现有6.0gCO和CO2的混合气体,在标准状况下其体积为4.48L。请回答下列问题:
(1)该混合气体的平均摩尔质量为_________ 。
(2)将混合气体依次通过过量的溶液中,装置如图所示,最后收集在气球中(体积在标准状况下测定)。

①NaOH溶液中发生的离子反应方程式_________ 。
②气球的体积为_________  (忽略气球弹性的影响)。
(忽略气球弹性的影响)。
③若将混合气体通入足量的Na2O2中,转移的电子数为_________ (用NA表示)。
(1)该混合气体的平均摩尔质量为
(2)将混合气体依次通过过量的溶液中,装置如图所示,最后收集在气球中(体积在标准状况下测定)。

①NaOH溶液中发生的离子反应方程式
②气球的体积为
 (忽略气球弹性的影响)。
(忽略气球弹性的影响)。③若将混合气体通入足量的Na2O2中,转移的电子数为
您最近一年使用:0次



