根据物质的组成、结构、性质等进行分类,可预测物质的性质及变化:
(1) 是普通玻璃的主要成分,与
是普通玻璃的主要成分,与 一样是酸性氧化物,写出
一样是酸性氧化物,写出 溶于NaOH溶液的化学方程式:
溶于NaOH溶液的化学方程式:______ .
(2)现有:①固体KOH ②稀硫酸 ③氦气 ④熔融NaCl ⑤蔗糖 ⑥铜;其中能导电的是______ (填序号,下同);属于电解质的是______ ,属于非电解质的是______ .
(3)写出 在水溶液中的电离方程式
在水溶液中的电离方程式______ .
Ⅱ.物质的量是联系宏观和微观的桥梁:
(4)40.5g某金属氯化物 中含0.6mol
中含0.6mol ,则M的摩尔质量为
,则M的摩尔质量为______ .
(5)标准状况下,与34g的 气体含相同H原子数的
气体含相同H原子数的 的体积为
的体积为______ .
(6)标准状况下,若aL二氧化碳中含有b个氧原子,则阿伏加德罗常数为______ .
(7)实验室使用的浓盐酸的溶质质量分数为36.5%,密度为 ,则该浓盐酸的物质的量浓度为
,则该浓盐酸的物质的量浓度为______ .
(8)一种加碘盐(配料为NaCl和 )中
)中 的含量为
的含量为 ,则每千克该加碘盐中碘的质量为
,则每千克该加碘盐中碘的质量为______ .
(1)
 是普通玻璃的主要成分,与
是普通玻璃的主要成分,与 一样是酸性氧化物,写出
一样是酸性氧化物,写出 溶于NaOH溶液的化学方程式:
溶于NaOH溶液的化学方程式:(2)现有:①固体KOH ②稀硫酸 ③氦气 ④熔融NaCl ⑤蔗糖 ⑥铜;其中能导电的是
(3)写出
 在水溶液中的电离方程式
在水溶液中的电离方程式Ⅱ.物质的量是联系宏观和微观的桥梁:
(4)40.5g某金属氯化物
 中含0.6mol
中含0.6mol ,则M的摩尔质量为
,则M的摩尔质量为(5)标准状况下,与34g的
 气体含相同H原子数的
气体含相同H原子数的 的体积为
的体积为(6)标准状况下,若aL二氧化碳中含有b个氧原子,则阿伏加德罗常数为
(7)实验室使用的浓盐酸的溶质质量分数为36.5%,密度为
 ,则该浓盐酸的物质的量浓度为
,则该浓盐酸的物质的量浓度为(8)一种加碘盐(配料为NaCl和
 )中
)中 的含量为
的含量为 ,则每千克该加碘盐中碘的质量为
,则每千克该加碘盐中碘的质量为
更新时间:2023-12-04 12:20:17
|
相似题推荐
计算题
|
较易
(0.85)
【推荐1】在潜水艇和消防员的呼吸面具中,常用 粉末作为氧气的来源。已知每人每小时消耗的
粉末作为氧气的来源。已知每人每小时消耗的 在标准状况下的体积约为
在标准状况下的体积约为 。请计算:
。请计算:
(1)每人每小时消耗 的物质的量约为
的物质的量约为_______  ;
;
(2)假设所需的氧气全部由 来提供,则每位消防员工作1小时所消耗
来提供,则每位消防员工作1小时所消耗 的质量为
的质量为_______  ;
;
(3)取久置呼吸面具中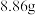 粉末溶于水(杂质为
粉末溶于水(杂质为 ),加入
),加入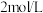 盐酸完全反应至溶液呈中性,共消耗
盐酸完全反应至溶液呈中性,共消耗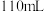 盐酸,则该呼吸面具中的
盐酸,则该呼吸面具中的 的质量分数为
的质量分数为_______ 。
 粉末作为氧气的来源。已知每人每小时消耗的
粉末作为氧气的来源。已知每人每小时消耗的 在标准状况下的体积约为
在标准状况下的体积约为 。请计算:
。请计算:(1)每人每小时消耗
 的物质的量约为
的物质的量约为 ;
;(2)假设所需的氧气全部由
 来提供,则每位消防员工作1小时所消耗
来提供,则每位消防员工作1小时所消耗 的质量为
的质量为 ;
;(3)取久置呼吸面具中
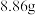 粉末溶于水(杂质为
粉末溶于水(杂质为 ),加入
),加入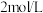 盐酸完全反应至溶液呈中性,共消耗
盐酸完全反应至溶液呈中性,共消耗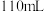 盐酸,则该呼吸面具中的
盐酸,则该呼吸面具中的 的质量分数为
的质量分数为
您最近一年使用:0次
计算题
|
较易
(0.85)
名校
解题方法
【推荐2】(Ⅰ)设NA代表阿伏加德罗常数的值,完成下列填空:
(1)1molCH4含原子个数为______________ ;34gH2O2所含原子数目为____ 。
(2)标准状况下,0.5NA个CO分子所占有的体积为________ L。
(3)标准状况下,33.6LH2和CH4的混合气体所含的分子数目为________ 。
(Ⅱ)某双原子分子构成的气体,其摩尔质量为Mg∙mol-1,该气体的质量为mg,阿伏加德罗常数为NA,则:
(1)该气体在标准状况下的体积为________ L。
(2)该气体在标准状况下的密度为__ g∙L-1。
(3)该气体所含的原子总数为________ 个。
(4)该气体的一个分子的质量为________ g。
(Ⅲ)(1)等质量的CO和CO2,物质的量之比为________ ;氧原子个数之比为________ ;
(2)1.5molH2SO4的质量是________ g,其中含有________ molH,含有________ g氧原子。
(3)9.03×1023个氨分子含______ molNH3,______ mol氢原子,________ mol电子。
(1)1molCH4含原子个数为
(2)标准状况下,0.5NA个CO分子所占有的体积为
(3)标准状况下,33.6LH2和CH4的混合气体所含的分子数目为
(Ⅱ)某双原子分子构成的气体,其摩尔质量为Mg∙mol-1,该气体的质量为mg,阿伏加德罗常数为NA,则:
(1)该气体在标准状况下的体积为
(2)该气体在标准状况下的密度为
(3)该气体所含的原子总数为
(4)该气体的一个分子的质量为
(Ⅲ)(1)等质量的CO和CO2,物质的量之比为
(2)1.5molH2SO4的质量是
(3)9.03×1023个氨分子含
您最近一年使用:0次
计算题
|
较易
(0.85)
【推荐3】回答下列问题:
(1)在标准状况下,CO和CO2的混合气体共39.2L,质量为61g,则两种气体的物质的量之和为_______ mol,其中CO2为_______ mol,CO占总体积的_______ ,混合气体的摩尔质量为_______ 。
(2)同温同压下,同体积的甲烷(CH4)和二氧化碳中,所含分子数之比为_______ ,物质的量之比为_______ ,原子数之比为_______ ,质量之比为_______ ,密度之比为_______ 。
(3)在标准状况下,4gH2、11.2LO2、1molH2O中,所含分子数最多的是_______ ,原子数最多的是_______ ,质量最大的是_______ ,体积最小的是_______ 。
(1)在标准状况下,CO和CO2的混合气体共39.2L,质量为61g,则两种气体的物质的量之和为
(2)同温同压下,同体积的甲烷(CH4)和二氧化碳中,所含分子数之比为
(3)在标准状况下,4gH2、11.2LO2、1molH2O中,所含分子数最多的是
您最近一年使用:0次
计算题
|
较易
(0.85)
【推荐1】(1)等质量的氧气和臭氧其物质的量之比为___ ,原子个数之比为__ 。
(2)标准状况下,36.5gHCl气体的体积约为___ 。将该气体溶于水中得到2L溶液,则该溶液的浓度为____ 。
(3)质量分数为w的MgCl2溶液,密度为dg/mL,该溶液中氯离子的物质的量浓度为____ 。
(2)标准状况下,36.5gHCl气体的体积约为
(3)质量分数为w的MgCl2溶液,密度为dg/mL,该溶液中氯离子的物质的量浓度为
您最近一年使用:0次
计算题
|
较易
(0.85)
解题方法
【推荐2】根据所学知识,回答下列问题:
(1)下图是中学化学中常用于混合物的分离和提纯的装置:
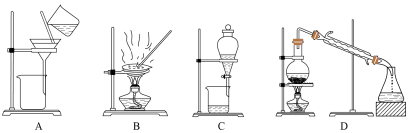
①分离花生油和水的混合物,选择装置_____ (填字母,下同)。
②提纯粗盐,并得到氯化钠晶体,选择装置_____ 。
③用 提取碘水中的碘,选择装置
提取碘水中的碘,选择装置_____ 。
④除去自来水中的 等杂质,选择装置
等杂质,选择装置_____ 。
(2)化学计量在中学化学中占有重要地位。
①标准状况下,体积为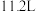 的
的 的质量为
的质量为_____ g。
②标准状况下, 某气体的质量为
某气体的质量为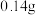 ,则其摩尔质量为
,则其摩尔质量为_____  。
。
③等物质的量的 和
和 中氢原子个数比是
中氢原子个数比是_____ 。
④ 的
的 溶液中含有的
溶液中含有的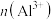 是
是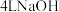 溶液中
溶液中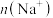 的两倍,则
的两倍,则
_____  。
。
(1)下图是中学化学中常用于混合物的分离和提纯的装置:

①分离花生油和水的混合物,选择装置
②提纯粗盐,并得到氯化钠晶体,选择装置
③用
 提取碘水中的碘,选择装置
提取碘水中的碘,选择装置④除去自来水中的
 等杂质,选择装置
等杂质,选择装置(2)化学计量在中学化学中占有重要地位。
①标准状况下,体积为
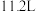 的
的 的质量为
的质量为②标准状况下,
 某气体的质量为
某气体的质量为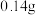 ,则其摩尔质量为
,则其摩尔质量为 。
。③等物质的量的
 和
和 中氢原子个数比是
中氢原子个数比是④
 的
的 溶液中含有的
溶液中含有的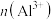 是
是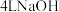 溶液中
溶液中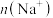 的两倍,则
的两倍,则
 。
。
您最近一年使用:0次
计算题
|
较易
(0.85)
名校
【推荐1】标准状态下,将11.2 LHCl气体溶于水,制成250mL溶液。
(1)试求该盐酸溶液的物质的量浓度______ ;
(2)如果用质量分数为36.5%密度为1.2 g/cm3 的浓盐酸来配制上述溶液,则应量取该浓盐酸多少毫升进行稀释____________ 。
(1)试求该盐酸溶液的物质的量浓度
(2)如果用质量分数为36.5%密度为1.2 g/cm3 的浓盐酸来配制上述溶液,则应量取该浓盐酸多少毫升进行稀释
您最近一年使用:0次
计算题
|
较易
(0.85)
解题方法
【推荐2】(1)0.4molCH4的质量为______ g;标况下,4.48LCO2的分子数为______ 。
(2)12.4gNa2R含Na+0.4mol,则Na2R的摩尔质量为______ 。
(3)将4gNaOH溶解在水中配成10mL溶液,再稀释成1L,从中取出10mL,这10mL溶液的物质的量浓度为_______ mol·L-1。
(4)VLAl2(SO4)3溶液中含有Al3+ag,则溶液中 的物质的量浓度为
的物质的量浓度为________ mol∙L-1
(5)某混合溶液中含有离子:Na+、Mg2+、Cl-、 ,测得Na+、Mg2+、Cl-的物质的量浓度依次为:0.2mol∙L-1、0.25mol∙L-1、0.4mol∙L-1,则
,测得Na+、Mg2+、Cl-的物质的量浓度依次为:0.2mol∙L-1、0.25mol∙L-1、0.4mol∙L-1,则 的物质的量浓度为
的物质的量浓度为_______ mol∙L-1。
(2)12.4gNa2R含Na+0.4mol,则Na2R的摩尔质量为
(3)将4gNaOH溶解在水中配成10mL溶液,再稀释成1L,从中取出10mL,这10mL溶液的物质的量浓度为
(4)VLAl2(SO4)3溶液中含有Al3+ag,则溶液中
 的物质的量浓度为
的物质的量浓度为(5)某混合溶液中含有离子:Na+、Mg2+、Cl-、
 ,测得Na+、Mg2+、Cl-的物质的量浓度依次为:0.2mol∙L-1、0.25mol∙L-1、0.4mol∙L-1,则
,测得Na+、Mg2+、Cl-的物质的量浓度依次为:0.2mol∙L-1、0.25mol∙L-1、0.4mol∙L-1,则 的物质的量浓度为
的物质的量浓度为
您最近一年使用:0次
计算题
|
较易
(0.85)
【推荐1】Ⅰ.根据物质的组成、结构、性质等进行分类,可预测物质的性质及变化:
(1)SiO2是普通玻璃的主要成分,与CO2一样是酸性氧化物,写出SiO2溶于NaOH溶液的化学方程式:___________ 。
(2)现有:①固体KOH②稀硫酸③氨气④熔融NaCl⑤蔗糖⑥铜;其中能导电的是___________ (填序号,下同)属于电解质的是___________ 。
(3)写出NaClO在水溶液中的电离方程式:___________ 。
Ⅱ.物质的量是联系宏观和微观的桥梁:
(4)40.5g某金属氯化物MCl2中含0.6molCl-,则该氯化物的摩尔质量为___________ 。
(5)标准状况下,与34g的H2S气体含相同H原子数的CH4的体积为___________ 。
(6)由CO、CO2两气体组成的混合气体12.8g,标准状况下,体积为8.96L。则CO、CO2的物质的量之比为___________ 。
(7)在VmL的硫酸铁溶液中,含有mgFe3+离子,则此溶液中 的物质的量浓度为
的物质的量浓度为_______ 。
(8)若用容量瓶以质量分数98%、密度为1.84g/cm3的浓硫酸配制480mL浓度0.2mol/L稀硫酸,计算需要用量筒量取___________ mL的浓硫酸。
(9)用4×10-3mol的KZO4恰好将60mL0.1mol/L的Na2SO3溶液氧化为Na2SO4,则元素Z在还原产物中的化合价是___________ 。
(1)SiO2是普通玻璃的主要成分,与CO2一样是酸性氧化物,写出SiO2溶于NaOH溶液的化学方程式:
(2)现有:①固体KOH②稀硫酸③氨气④熔融NaCl⑤蔗糖⑥铜;其中能导电的是
(3)写出NaClO在水溶液中的电离方程式:
Ⅱ.物质的量是联系宏观和微观的桥梁:
(4)40.5g某金属氯化物MCl2中含0.6molCl-,则该氯化物的摩尔质量为
(5)标准状况下,与34g的H2S气体含相同H原子数的CH4的体积为
(6)由CO、CO2两气体组成的混合气体12.8g,标准状况下,体积为8.96L。则CO、CO2的物质的量之比为
(7)在VmL的硫酸铁溶液中,含有mgFe3+离子,则此溶液中
 的物质的量浓度为
的物质的量浓度为(8)若用容量瓶以质量分数98%、密度为1.84g/cm3的浓硫酸配制480mL浓度0.2mol/L稀硫酸,计算需要用量筒量取
(9)用4×10-3mol的KZO4恰好将60mL0.1mol/L的Na2SO3溶液氧化为Na2SO4,则元素Z在还原产物中的化合价是
您最近一年使用:0次
计算题
|
较易
(0.85)
名校
【推荐2】根据所学知识,回答下列问题:
(1)CH4和H2是两种重要的气体燃料
①标准状况下,5.6L的CH4的质量为____ 克。
②4gH2所含的氢原子数约为____ 个。
③相同质量的CH4和H2,所含的原子数之比为____ 。
④标准状况下,11.2LCH4和H2混合气体质量为4.5g,则CH4和H2的分子个数之为____ 。
(2)有以下几种物质:①食盐晶体;②铜;③KNO3溶液:④蔗糖;⑤CO2。请根据要求填空。(填序号)
①属于电解质的是____ ,属于非电解质的是____ 。
②既不是电解质也不是非电解质的是____ 。
(1)CH4和H2是两种重要的气体燃料
①标准状况下,5.6L的CH4的质量为
②4gH2所含的氢原子数约为
③相同质量的CH4和H2,所含的原子数之比为
④标准状况下,11.2LCH4和H2混合气体质量为4.5g,则CH4和H2的分子个数之为
(2)有以下几种物质:①食盐晶体;②铜;③KNO3溶液:④蔗糖;⑤CO2。请根据要求填空。(填序号)
①属于电解质的是
②既不是电解质也不是非电解质的是
您最近一年使用:0次
计算题
|
较易
(0.85)
名校
【推荐3】回答下列问题:
(1)现有下列10种物质:①铝,②纯醋酸,③CO2,④苏打,⑤Ba(OH)2,⑥氢氧化铁胶体,⑦稀盐酸,⑧NaHSO4固体,⑨碳酸钙,⑩氨水。
①上述物质中属于盐的是____ ,属于电解质的有____ 。(填序号)
②简述实验室制备⑥的方法_____ 。
③写出⑧在水中的电离方程式为____ 。
④将⑨和⑦混合,反应的离子方程式为____ 。
(2)完成下列有关物质的量的相关计算:
①3.4gNH3与标准状况下的____ L的H2S含有相同数目的氢原子。
②40.5g某金属氯化物MCl2中含有0.6molCl-,则该金属氯化物的摩尔质量为____ 。
③实验室配制100mL0.2mol•L-1的Na2CO3溶液,通过计算得出可用天平称取Na2CO3固体____ g。若用4mol•L-1的Na2CO3浓溶液配制100mL0.2mol•L-1的稀溶液,应用量筒量取____ mL该浓溶液。
(1)现有下列10种物质:①铝,②纯醋酸,③CO2,④苏打,⑤Ba(OH)2,⑥氢氧化铁胶体,⑦稀盐酸,⑧NaHSO4固体,⑨碳酸钙,⑩氨水。
①上述物质中属于盐的是
②简述实验室制备⑥的方法
③写出⑧在水中的电离方程式为
④将⑨和⑦混合,反应的离子方程式为
(2)完成下列有关物质的量的相关计算:
①3.4gNH3与标准状况下的
②40.5g某金属氯化物MCl2中含有0.6molCl-,则该金属氯化物的摩尔质量为
③实验室配制100mL0.2mol•L-1的Na2CO3溶液,通过计算得出可用天平称取Na2CO3固体
您最近一年使用:0次



