化学实验中需要用到不同纯度的化学试剂,这些试剂需要经过一系列除杂净化过程。实验者需要根据主要成分和杂质的性质,选用合适的分离提纯方法。
(1)以下是化学中常用于混合物的分离和提纯的装置。根据装置回答下列问题:
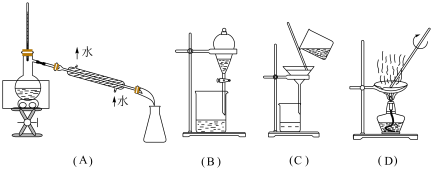
①从氯化钾溶液中得到氯化钾固体,选择装置___________ (填字母,下同)。
②用海水获得纯净水,选择装置___________ 。
③从碘水中分离出 ,选择装置
,选择装置___________ 。
(2)实验室需用250mL 的稀盐酸,现用11.9mol/L的浓盐酸配制。
的稀盐酸,现用11.9mol/L的浓盐酸配制。
①经计算需要___________ mL浓盐酸,在量取时宜选用下列的量筒___________
A.5mL B.10mL C.25mL D.50mL
②在量取浓盐酸后,进行了下列操作:
a.稀释后的盐酸温度降至与室温一致后,沿玻璃棒注入250mL容量瓶中。
b.往容量瓶中小心加蒸馏水至液面接近环形标线2~3cm处,改用胶头滴管加蒸馏水,使溶液的凹面底部与瓶颈的环形标线相切。
c.在盛盐酸的烧杯中注入蒸馏水几十毫升,并用玻璃棒搅动,使其混合均匀。
d.用蒸馏水洗涤烧杯和玻璃棒2至3次,并将洗涤液全部注入容量瓶。
上述操作中,正确的顺序是___________ (填序号)。
③在上述配制过程中,用刚刚洗涤洁净的量筒来量取浓盐酸,其配制的稀盐酸浓度___________ (填“偏高”“偏低”或“无影响”)。若未用蒸馏水洗涤烧杯内壁或未将洗涤液注入容量瓶,则配制的稀盐酸浓度是___________ (填“偏高”“偏低”或“无影响”)。
(1)以下是化学中常用于混合物的分离和提纯的装置。根据装置回答下列问题:

①从氯化钾溶液中得到氯化钾固体,选择装置
②用海水获得纯净水,选择装置
③从碘水中分离出
 ,选择装置
,选择装置(2)实验室需用250mL
 的稀盐酸,现用11.9mol/L的浓盐酸配制。
的稀盐酸,现用11.9mol/L的浓盐酸配制。①经计算需要
A.5mL B.10mL C.25mL D.50mL
②在量取浓盐酸后,进行了下列操作:
a.稀释后的盐酸温度降至与室温一致后,沿玻璃棒注入250mL容量瓶中。
b.往容量瓶中小心加蒸馏水至液面接近环形标线2~3cm处,改用胶头滴管加蒸馏水,使溶液的凹面底部与瓶颈的环形标线相切。
c.在盛盐酸的烧杯中注入蒸馏水几十毫升,并用玻璃棒搅动,使其混合均匀。
d.用蒸馏水洗涤烧杯和玻璃棒2至3次,并将洗涤液全部注入容量瓶。
上述操作中,正确的顺序是
③在上述配制过程中,用刚刚洗涤洁净的量筒来量取浓盐酸,其配制的稀盐酸浓度
更新时间:2023-12-24 22:36:35
|
相似题推荐
解答题-实验探究题
|
适中
(0.65)
名校
【推荐1】实验室要配制一定物质的量浓度的稀盐酸,请按要求回答下列问题:
(1)某市售浓盐酸试剂瓶标签上的部分数据如图所示,则该浓盐酸的物质的量浓度是_______ 。

(2)某次实验需要使用220mL1.6mol/L的稀盐酸,现用上述浓盐酸进行配制,请回答下列问题:
①通过计算可知,需要用量筒一次量取浓盐酸_______ mL。需要的仪器除了量筒、烧杯、玻璃棒外,还需要使用的仪器为_______ 。
②配制时,其正确操作顺序是(用字母表示,每个字母只能用一次)_______ 。还缺少的步骤是_______ ,若缺少该步骤将导致结果_______ (填“偏高”、“偏低”或“无影响”)。
A.加水至溶液凹液面与刻度线相切
B.用量筒准确量取浓盐酸的体积,沿内壁加盛有少量水(约30mL)的烧杯中,用玻璃棒慢慢搅动
C.将已冷却的盐酸溶液沿玻璃棒注入容量瓶中
D.将容量瓶盖紧,颠倒摇匀
E.继续往容量瓶内小心加水,直到液面接近刻度1~2cm处
③该溶液的配制过程中,会导致所配溶液浓度偏低的操作为_______ 。
A.用量筒量取浓盐酸时仰视操作
B.配制前洗涤容量瓶,但是未干燥就进行配制
C.定容时,加蒸馏水超过刻度线,又用胶头滴管吸出
D.定容摇匀后,发现液面低于标线,又用胶头滴管加蒸馏水至刻度线
E.定容时,俯视刻度线
F.转移过程中有少量溶液溅出
(1)某市售浓盐酸试剂瓶标签上的部分数据如图所示,则该浓盐酸的物质的量浓度是

(2)某次实验需要使用220mL1.6mol/L的稀盐酸,现用上述浓盐酸进行配制,请回答下列问题:
①通过计算可知,需要用量筒一次量取浓盐酸
②配制时,其正确操作顺序是(用字母表示,每个字母只能用一次)
A.加水至溶液凹液面与刻度线相切
B.用量筒准确量取浓盐酸的体积,沿内壁加盛有少量水(约30mL)的烧杯中,用玻璃棒慢慢搅动
C.将已冷却的盐酸溶液沿玻璃棒注入容量瓶中
D.将容量瓶盖紧,颠倒摇匀
E.继续往容量瓶内小心加水,直到液面接近刻度1~2cm处
③该溶液的配制过程中,会导致所配溶液浓度偏低的操作为
A.用量筒量取浓盐酸时仰视操作
B.配制前洗涤容量瓶,但是未干燥就进行配制
C.定容时,加蒸馏水超过刻度线,又用胶头滴管吸出
D.定容摇匀后,发现液面低于标线,又用胶头滴管加蒸馏水至刻度线
E.定容时,俯视刻度线
F.转移过程中有少量溶液溅出
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐2】某学生欲配制1000mL6.0mol·L-1的H2SO4,实验室有三种不同浓度的硫酸:
①480mL0.5mol·L-1的硫酸;②150mL25%的硫酸(ρ=1.18g·mL-1);③足量的18mol·L-1的硫酸。有三种规格的容量瓶:250mL、500mL、1000mL。老师要求把①②两种硫酸全部用完,不足的部分由③来补充。
请回答下列问题:
(1)实验所用25%的硫酸的物质的量浓度为___ mol·L-1(保留1位小数)。
(2)配制时,该同学的操作顺序如下,请将操作步骤B、D补充完整。
A.将①②两溶液全部在烧杯中混合均匀;
B.用量筒准确量取所需的18mol·L-1的浓硫酸___ mL,沿玻璃棒倒入上述混合液中。并用玻璃棒搅拌,使其混合均匀;
C.将混合均匀的硫酸沿玻璃棒注入所选的容量瓶中;
D.___ ;
E.振荡,继续向容量瓶中加水,直到液面接近刻度线1~2cm处;
F.改用胶头滴管加水,使溶液的凹液面恰好与刻度线相切;
G.将容量瓶盖紧,振荡,摇匀。
(3)进行操作C前还需注意___ 。
(4)如果省略操作D,对所配溶液浓度有何影响?___ (填“偏大”、“偏小”或“无影响”)。
①480mL0.5mol·L-1的硫酸;②150mL25%的硫酸(ρ=1.18g·mL-1);③足量的18mol·L-1的硫酸。有三种规格的容量瓶:250mL、500mL、1000mL。老师要求把①②两种硫酸全部用完,不足的部分由③来补充。
请回答下列问题:
(1)实验所用25%的硫酸的物质的量浓度为
(2)配制时,该同学的操作顺序如下,请将操作步骤B、D补充完整。
A.将①②两溶液全部在烧杯中混合均匀;
B.用量筒准确量取所需的18mol·L-1的浓硫酸
C.将混合均匀的硫酸沿玻璃棒注入所选的容量瓶中;
D.
E.振荡,继续向容量瓶中加水,直到液面接近刻度线1~2cm处;
F.改用胶头滴管加水,使溶液的凹液面恰好与刻度线相切;
G.将容量瓶盖紧,振荡,摇匀。
(3)进行操作C前还需注意
(4)如果省略操作D,对所配溶液浓度有何影响?
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐3】如图为实验室某浓盐酸试剂瓶上的标签,试根据有关数据回答下列问题:

(1)该浓盐酸中HCl的物质的量浓度为________ mol/L。
(2)某学生欲用上述浓盐酸和蒸馏水配制450 mL物质的量浓度为0.1 mol/L稀盐酸:
①该学生需要量取________ mL上述浓盐酸进行配制。
②配制过程中,除需要使用烧杯、量筒、玻璃棒外,还需要使用的仪器是_____ 、______ (填写名称)
③配制时,其正确的操作顺序是(要求用字母表示,每个字母只能用一次)_______ ;
A.用30mL蒸馏水洗涤烧杯及玻璃棒2—3次,洗涤液均注入容量瓶,振荡
B.用量筒准确量取所需浓盐酸的体积,慢慢沿杯壁注入盛有少量蒸馏水(约30mL)的烧杯中,用玻璃棒慢慢搅动,使其混合均匀
C.将已冷却的盐酸沿玻璃棒注入容量瓶中
D.将容量瓶盖紧,颠倒摇匀
E.改用胶头滴管加蒸馏水,使溶液凹面恰好与刻度线相切
F.继续往容量瓶内小心加蒸馏水,直到液面接近刻线1—2cm处
④在配制过程中,下列实验操作会使所配制的稀盐酸的物质的量浓度偏高的是________
A.摇匀后静置,发现液面低于刻线,继续加水至与刻线相切
B.溶液注入容量瓶前没有恢复到室温就进行定容
C.定容时仰视刻线
D.在配制前用已知浓度的稀盐酸润洗容量瓶

(1)该浓盐酸中HCl的物质的量浓度为
(2)某学生欲用上述浓盐酸和蒸馏水配制450 mL物质的量浓度为0.1 mol/L稀盐酸:
①该学生需要量取
②配制过程中,除需要使用烧杯、量筒、玻璃棒外,还需要使用的仪器是
③配制时,其正确的操作顺序是(要求用字母表示,每个字母只能用一次)
A.用30mL蒸馏水洗涤烧杯及玻璃棒2—3次,洗涤液均注入容量瓶,振荡
B.用量筒准确量取所需浓盐酸的体积,慢慢沿杯壁注入盛有少量蒸馏水(约30mL)的烧杯中,用玻璃棒慢慢搅动,使其混合均匀
C.将已冷却的盐酸沿玻璃棒注入容量瓶中
D.将容量瓶盖紧,颠倒摇匀
E.改用胶头滴管加蒸馏水,使溶液凹面恰好与刻度线相切
F.继续往容量瓶内小心加蒸馏水,直到液面接近刻线1—2cm处
④在配制过程中,下列实验操作会使所配制的稀盐酸的物质的量浓度偏高的是
A.摇匀后静置,发现液面低于刻线,继续加水至与刻线相切
B.溶液注入容量瓶前没有恢复到室温就进行定容
C.定容时仰视刻线
D.在配制前用已知浓度的稀盐酸润洗容量瓶
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐1】苯甲酸及其钠盐可用作乳胶、牙膏、果酱或其他食品的抑菌剂,也可广泛应用于制药和化工行业,某同学尝试用甲苯的氧化反应制备苯甲酸。主要实验装置(回流搅拌装置)如图所示:

反应原理:
 +2KMnO4→
+2KMnO4→ +KOH+2MnO2↓+H2O
+KOH+2MnO2↓+H2O
 +HCl→
+HCl→ +KCl
+KCl
实验方法:将一定量的甲苯和KMnO4溶液置于三颈烧瓶中,在90℃时反应一段时间后,停止反应,按如图流程分离出苯甲酸并回收未反应的甲苯。

(1)无色液体A的结构简式为___ ,操作Ⅱ为___ ;
(2)如果滤液呈紫色,要先加饱和亚硫酸钾溶液,过滤后再进行操作Ⅰ。加饱和亚硫酸钾溶液的目的是___ ,写出该反应的离子方程式:___ ;
(3)冷却水应该从冷凝管___ (填“a”或“b”)口流入;
(4)要由“水层”得到苯甲酸晶体,应进行下列操作,正确的操作顺序是___ (填选项字母):
A.酸化 B.过滤 C.蒸发浓缩 D.冷却结晶
(5)纯度测定:称取1.22g产品,配成100mL溶液,取其中25.00mL溶液,用KOH溶液进行滴定,消耗KOH的物质的量为2.40×10-3mol,则产品中苯甲酸的质量分数为__ 。

反应原理:
 +2KMnO4→
+2KMnO4→ +KOH+2MnO2↓+H2O
+KOH+2MnO2↓+H2O +HCl→
+HCl→ +KCl
+KCl实验方法:将一定量的甲苯和KMnO4溶液置于三颈烧瓶中,在90℃时反应一段时间后,停止反应,按如图流程分离出苯甲酸并回收未反应的甲苯。

(1)无色液体A的结构简式为
(2)如果滤液呈紫色,要先加饱和亚硫酸钾溶液,过滤后再进行操作Ⅰ。加饱和亚硫酸钾溶液的目的是
(3)冷却水应该从冷凝管
(4)要由“水层”得到苯甲酸晶体,应进行下列操作,正确的操作顺序是
A.酸化 B.过滤 C.蒸发浓缩 D.冷却结晶
(5)纯度测定:称取1.22g产品,配成100mL溶液,取其中25.00mL溶液,用KOH溶液进行滴定,消耗KOH的物质的量为2.40×10-3mol,则产品中苯甲酸的质量分数为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐2】氯化苦( )是一种无色或微黄色油状液体,可用于粮食害虫熏蒸,还可用于木材防腐、房屋和船舶消毒等。制备氯化苦的反应原理为
)是一种无色或微黄色油状液体,可用于粮食害虫熏蒸,还可用于木材防腐、房屋和船舶消毒等。制备氯化苦的反应原理为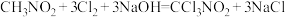
 。已知氯化苦、硝基甲烷(
。已知氯化苦、硝基甲烷( )的性质如下表所示:
)的性质如下表所示:
(一)氯化苦的制备

(1)仪器X的名称是______ 。
(2)装置A中发生反应的化学方程式为 ,将其改写成离子方程式:
,将其改写成离子方程式:______ 。
(3)装置B中饱和食盐水的作用是______ ,装置D的作用是______ 。
(二)氯化苦的提纯
(4)步骤1:将上述制得的氯化苦混合溶液在下图装置中进行分液,氯化苦应该从分液漏斗______ (填“上”或“下”)口倒出。

步骤2:将步骤1分离出的氯化苦混合溶液进行蒸馏,将温度控制在101.2~110℃范围内其目的是______ 。
 )是一种无色或微黄色油状液体,可用于粮食害虫熏蒸,还可用于木材防腐、房屋和船舶消毒等。制备氯化苦的反应原理为
)是一种无色或微黄色油状液体,可用于粮食害虫熏蒸,还可用于木材防腐、房屋和船舶消毒等。制备氯化苦的反应原理为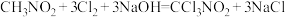
 。已知氯化苦、硝基甲烷(
。已知氯化苦、硝基甲烷( )的性质如下表所示:
)的性质如下表所示:| 名称 | 相对分子质量 | 密度/( ) ) | 熔点/℃ | 沸点/℃ | 溶解性 |
| 氯化苦 | 164.5 | 1.66 | -69.2 | 112 | 不溶于水,溶于乙醇 |
| 硝基甲烷 | 61 | 1.14 | -28.6 | 101.2 | 溶于水、乙醇 |

(1)仪器X的名称是
(2)装置A中发生反应的化学方程式为
 ,将其改写成离子方程式:
,将其改写成离子方程式:(3)装置B中饱和食盐水的作用是
(二)氯化苦的提纯
(4)步骤1:将上述制得的氯化苦混合溶液在下图装置中进行分液,氯化苦应该从分液漏斗

步骤2:将步骤1分离出的氯化苦混合溶液进行蒸馏,将温度控制在101.2~110℃范围内其目的是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐3】丙烯酸甲酯(CH2=CHCOOCH3)是一种重要的有机化工原料。实验室制备少量丙烯酸甲酯的反应为:CH2=CHCOOH+CH3OH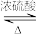 CH2=CHCOOCH3+H2O,步骤如下:
CH2=CHCOOCH3+H2O,步骤如下:
步骤1:在100mL圆底烧瓶中依次加入10.0g丙烯酸、少许碎瓷片、10mL甲醇和2mL浓硫酸,搅拌。
步骤2:如图,连接装置,加热烧瓶中的混合液,用锥形瓶盛接通过分水器分离出的水。当不再有水生成,停止加热。

步骤3:反应液冷却后,依次用5%Na2CO3溶液、饱和食盐水、水洗涤。分离出有机相。
步骤4;向有机相中加无水Na2SO4固体,过滤后蒸馏,收集70~90℃馏分。测得丙烯酸甲酯的质量为6.45g。
可能用到的信息:
请回答下列问题:
(1)步骤1中,加入碎瓷片的目的是__ 。
(2)步骤2中,图中所示装置中仪器A的名称是__ ,其作用为__ 。
(3)步骤3中,用5%Na2CO3溶液洗涤后,分离有机相的操作名称为__ 。
(4)实验中可能生成的有机副产物结构简式为__ (填一种即可)。
(5)本实验中丙烯酸甲酯的产率为__ %。
 CH2=CHCOOCH3+H2O,步骤如下:
CH2=CHCOOCH3+H2O,步骤如下:步骤1:在100mL圆底烧瓶中依次加入10.0g丙烯酸、少许碎瓷片、10mL甲醇和2mL浓硫酸,搅拌。
步骤2:如图,连接装置,加热烧瓶中的混合液,用锥形瓶盛接通过分水器分离出的水。当不再有水生成,停止加热。

步骤3:反应液冷却后,依次用5%Na2CO3溶液、饱和食盐水、水洗涤。分离出有机相。
步骤4;向有机相中加无水Na2SO4固体,过滤后蒸馏,收集70~90℃馏分。测得丙烯酸甲酯的质量为6.45g。
可能用到的信息:
| 密度 | 沸点 | 溶解性 | ||
| 丙烯酸 | 1.05g·cm-3 | 141℃ | 与水互溶,易溶于有机溶剂 | 有毒 |
| 甲醇 | 0.79g·cm-3 | 65℃ | 与水互溶,易溶于有机溶剂 | 易挥发,有毒 |
| 丙烯酸甲酯 | 0.95g·cm-3 | 80.5℃ | 难溶于水,易溶于有机溶剂 | 易挥发 |
(1)步骤1中,加入碎瓷片的目的是
(2)步骤2中,图中所示装置中仪器A的名称是
(3)步骤3中,用5%Na2CO3溶液洗涤后,分离有机相的操作名称为
(4)实验中可能生成的有机副产物结构简式为
(5)本实验中丙烯酸甲酯的产率为
您最近一年使用:0次



