下表是某些短周期元素的电负性值:
(1)通过分析电负性值变化规律,确定 的电负性值范围:
的电负性值范围:_______ 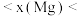
_______ 。
(2)推测 值与原子半径的关系是
值与原子半径的关系是_______ ;根据短周期元素的 值变化特点,体现了元素性质的
值变化特点,体现了元素性质的_______ 变化规律。
(3)分别指出下列两种化合物中氧元素的化合价:
_______ ,
_______ 。
(4)试推断 中化学键类型是
中化学键类型是_______ 。
(5)预测元素周期表中, 值最小的元素位于
值最小的元素位于_______ 周期_______ 族(放射性元素除外)。
| 元素符号 |  |  |  |  |  |  |  |  |  |  |  |  |
电负性值 | 0.98 | 1.57 | 2.04 | 2.55 | 3.44 | 3.98 | 0.93 | 1.61 | 1.90 | 2.19 | 2.58 | 3.16 |
(1)通过分析电负性值变化规律,确定
 的电负性值范围:
的电负性值范围: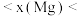
(2)推测
 值与原子半径的关系是
值与原子半径的关系是 值变化特点,体现了元素性质的
值变化特点,体现了元素性质的(3)分别指出下列两种化合物中氧元素的化合价:


(4)试推断
 中化学键类型是
中化学键类型是(5)预测元素周期表中,
 值最小的元素位于
值最小的元素位于
更新时间:2023-12-27 11:45:14
|
相似题推荐
填空题
|
适中
(0.65)
【推荐1】下表是元素周期表的一部分,根据所给的10种元素,完成以下各小题。
(1)金属性最强的元素是___________ (填元素符号)。最不活泼元素的原子结构示意图为___________ 。
(2)第3周期元素中,其最高价氧化物对应的水化物具有两性的元素是___________ (填元素名称)。Na、Mg两种元素中,原子半径较大的是___________ 。
(3)第3周期元素中,其元素的一种氧化物是形成酸雨的主要物质,该氧化物的化学式为___________ 。
(4)工业上可以用Cl2和H2来制取盐酸,该反应的化学方程式为___________ 。
(5)由碳与氢元素形成的最简单有机物的化学式为___________ ,该物质中碳元素与氢元素的质量比为___________ ,其分子立体构型为___________ 。
族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 1 | H | |||||||
| 2 | C | N | F | Ne | ||||
| 3 | Na | Mg | Al | S | Cl |
(2)第3周期元素中,其最高价氧化物对应的水化物具有两性的元素是
(3)第3周期元素中,其元素的一种氧化物是形成酸雨的主要物质,该氧化物的化学式为
(4)工业上可以用Cl2和H2来制取盐酸,该反应的化学方程式为
(5)由碳与氢元素形成的最简单有机物的化学式为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】下表是元素周期表的一部分,请针对表中所列标号为①~⑩的元素回答下列问题。

(1)非金属性最强的元素是______ (填元素符号,下同),形成化合物种类最多的元素是_____ ,最不活泼的元素是___________ 。
(2)第三周期元素除⑩外原子半径最小的是______ (填元素符号),这些元素的最高价氧化物对应水化物中碱性最强的是__________ (填化学式,下同),具有两性的是____________ ,最高价氧化物对应水化物中酸性最强的是__________ 。
(3)⑥⑦⑨形成的简单离子的由小到大的顺序是______________ (用离子符号回答问题),
⑧与⑨对应的氢化物比较稳定的是_________ (填化学式)。
(4)⑤和③可以形成两种化合物,其中可以做呼吸面具供氧剂的物质的电子式为_________ ,所含化学键的类型为 _______________ 。
(5)①与⑧形成的化合物的结构式__________ ,用电子式表示 ⑥与⑨所形成化合物的形成过程 _________________________ 。

(1)非金属性最强的元素是
(2)第三周期元素除⑩外原子半径最小的是
(3)⑥⑦⑨形成的简单离子的由小到大的顺序是
⑧与⑨对应的氢化物比较稳定的是
(4)⑤和③可以形成两种化合物,其中可以做呼吸面具供氧剂的物质的电子式为
(5)①与⑧形成的化合物的结构式
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】下表列出了a~m 13种元素在周期表(已省略了过渡元素 )中的位置:
(1)元素b为________ (填名称);画出g的原子结构示意图__________ 。
(2)元素f、i、j的原子半径从大到小的顺序是____________ (用元素符号表示);这三种原子分别形成简单离子后,离子半径从大到小的顺序是_____________ (用离子符号表示)。
(3)h和k的原子序数相差___________ (填数字)。
(4)元素d和e形成的一种化合物为淡黄色固体,该化合物的电子式为___________ ,该化合物中化学键有____________ ,该化合物与c的最高价氧化物反应的化学方程式为_________________ 。
| 族 周期 | ⅠA | 0 | ||||||
| 1 | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | a | |
| 2 | b | c | d | |||||
| 3 | e | f | g | h | i | |||
| 4 | j | k | l | |||||
| 5 | m |
(1)元素b为
(2)元素f、i、j的原子半径从大到小的顺序是
(3)h和k的原子序数相差
(4)元素d和e形成的一种化合物为淡黄色固体,该化合物的电子式为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】钇及其化合物在航天、电子、超导等方面有着广泛的应用,工业上以硅铍钇矿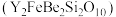 为原料生产氧化钇(
为原料生产氧化钇( )。
)。
(1)钇(Y)与钪同族,位于元素周期表中钪(Sc)的下一周期,基态钇(Y)原子的价电子排布图为______ ,与 元素同周期的基态原子中,未成对电子数与
元素同周期的基态原子中,未成对电子数与 原子相同的元素还有种
原子相同的元素还有种________ 。
(2)在元素周期表中, 和
和 处于第二周期和第三周期的对角线位置,化学性质相似。
处于第二周期和第三周期的对角线位置,化学性质相似。
①写出 的最高价氧化物对应水化物与烧碱溶液反应的离子方程式:
的最高价氧化物对应水化物与烧碱溶液反应的离子方程式:___________ 。
②已知 元素和
元素和 元素的电负性分别为1.5和4.0,则它们形成的化合物是
元素的电负性分别为1.5和4.0,则它们形成的化合物是_______ (填“离子化合物”或“共价化合物”)。
(3) 与
与 均为第二周期元素:
均为第二周期元素:
① 元素的原子核外共有
元素的原子核外共有____ 种不同空间运动状态的电子。
②电离能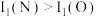 ,原因是
,原因是__________ 。
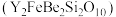 为原料生产氧化钇(
为原料生产氧化钇( )。
)。(1)钇(Y)与钪同族,位于元素周期表中钪(Sc)的下一周期,基态钇(Y)原子的价电子排布图为
 元素同周期的基态原子中,未成对电子数与
元素同周期的基态原子中,未成对电子数与 原子相同的元素还有种
原子相同的元素还有种(2)在元素周期表中,
 和
和 处于第二周期和第三周期的对角线位置,化学性质相似。
处于第二周期和第三周期的对角线位置,化学性质相似。①写出
 的最高价氧化物对应水化物与烧碱溶液反应的离子方程式:
的最高价氧化物对应水化物与烧碱溶液反应的离子方程式:②已知
 元素和
元素和 元素的电负性分别为1.5和4.0,则它们形成的化合物是
元素的电负性分别为1.5和4.0,则它们形成的化合物是(3)
 与
与 均为第二周期元素:
均为第二周期元素:①
 元素的原子核外共有
元素的原子核外共有②电离能
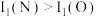 ,原因是
,原因是
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】判断元素的金属性和非金属性。
(1)______________ 的电负性一般小于1.8,______________ 的电负性一般大于1.8,而位于非金属三角区边界的“类金属”(如锗、锑等)元素的电负性则在1.8左右,它们既有金属性,又有非金属性。
(2)一般来说,金属元素的电负性______________ ,金属元素越活泼;非金属元素的电负性______________ ,非金属元素越活泼。
(1)
(2)一般来说,金属元素的电负性
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】已知A、B、C、D、E、F六种元素的原子序数依次递增,前四种元素为短周期元素。A位于元素周期表s区,电子层数与未成对电子数相等;B基态原子中电子占据三种能量不同的原子轨道,且每轨道中的电子总数相同;D原子核外成对电子数为未成对电子数的3倍;F位于第四周期d区,最高能级的原子轨道内只有2个未成对电子;E的一种氧化物具有磁性。
(1)E基态原子的价层电子排布式为__________________ 。第二周期基态原子未成对电子数与F相同且电负性最小的元素名称为____________ 。
(2)CD3- 的空间构型为_______________ 。
(3)A、B、D三元素组成的一种化合物X是家庭装修材料中常含有的一种有害气体,X分子中的中心原子采用_____________ 杂化。
(4)F(BD)n的中心原子价电子数与配体提供电子总数之和为18,则n=________ 。根据等电子原理,B、D 分子内σ键与π键的个数之比为______________ 。
(5)一种EF的合金晶体具有面心立方最密堆积的结构。在晶胞中,F位于顶点,E位于面心,该合金中EF的原子个数之比为_________________ 。若晶胞边长a pm,则合金密度为______________ g·cm3(列式表达,不计算)。
(1)E基态原子的价层电子排布式为
(2)CD3- 的空间构型为
(3)A、B、D三元素组成的一种化合物X是家庭装修材料中常含有的一种有害气体,X分子中的中心原子采用
(4)F(BD)n的中心原子价电子数与配体提供电子总数之和为18,则n=
(5)一种EF的合金晶体具有面心立方最密堆积的结构。在晶胞中,F位于顶点,E位于面心,该合金中EF的原子个数之比为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】下表是元素周期表的一部分。表中所列的字母分别代表一种化学元素。
试回答下列问题:
(1)请写出元素P的基态原子电子排布式___________________________ ;
(2)画出元素E的电子排布图__________________________ ;F氢化物的分子构型
为_____________ ;
(3)第三周期元素中,电负性最小的是_________ (填元素符号);第一电离能最大的是
_________ (填元素符号);
| A | |||||||||||||||||
| B | C | D | E | F | G | ||||||||||||
| H | I | J | K | L | M | N | |||||||||||
| O | P | ||||||||||||||||
试回答下列问题:
(1)请写出元素P的基态原子电子排布式
(2)画出元素E的电子排布图
为
(3)第三周期元素中,电负性最小的是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】已知元素的电负性和原子半径一样,也是元素的一种基本性质。短周期元素的电负性数值表。
请仔细观察表格中的数据,回答下列有关问题:
(1)根据表中的数据,可推测元素的电负性具有的变化规律是:_____ 。
(2)由表中数据可得出同主族元素的电负性变化规律是____ 。
(3)由表中数据预测电负性最大的元素为____ ;电负性较大与电负性较小的两元素之间易形成的化学键类型是____ 。
| 元素 | H | Li | Be | B | C | N | O | F | Na | Mg | Al | Si | P | S | Cl | K |
| 电负性 | 2.1 | 1.0 | 1.5 | 2.0 | 2.5 | 3.0 | 3.5 | 4.0 | 0.9 | 1.2 | 1.5 | 1.8 | 2.1 | 2.5 | 3.0 | 0.8 |
请仔细观察表格中的数据,回答下列有关问题:
(1)根据表中的数据,可推测元素的电负性具有的变化规律是:
(2)由表中数据可得出同主族元素的电负性变化规律是
(3)由表中数据预测电负性最大的元素为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】1932年美国化学家鲍林(L.Pauling)首先提出了电负性的概念。电负性(用X表示)也是元素的一种重要性质,下表给出的是原子序数小于20的16种元素的电负性数值:
请仔细分析,回答下列有关问题:
(1)根据表中所给数据分析,同主族内不同元素X值的变化规律是___________ ;简述元素电负性X的大小与元素金属性、非金属性之间的关系__________________ 。
(2)预测周期表中电负性最大的元素应为_______ ,估计钙(Ca)元素电负性的取值范围 ______ < X <_______ 。
(3)经验规律告诉我们:当形成化学键的两原子相应元素的电负性差值大于1.7时,所形成的化学键一般为离子键;当小于1.7时,一般为共价键。试推断AlBr3中的化学键类型为___________ ,其理由是____________ 。
元素 | H | Li | Be | B | C | N | O | F |
电负性 | 2.1 | 1.0 | 1.5 | 2.0 | 2.5 | 3.0 | 3.5 | 4.0 |
元素 | Na | Mg | Al | Si | P | S | Cl | K |
电负性 | 0.9 | 1.2 | 1.5 | 1.7 | 2.1 | 2.3 | 3.0 | 0.8 |
(1)根据表中所给数据分析,同主族内不同元素X值的变化规律是
(2)预测周期表中电负性最大的元素应为
(3)经验规律告诉我们:当形成化学键的两原子相应元素的电负性差值大于1.7时,所形成的化学键一般为离子键;当小于1.7时,一般为共价键。试推断AlBr3中的化学键类型为
您最近一年使用:0次



