元素周期表是学习物质结构和性质的重要工具,如图是元素周期表的一部分,①~⑧分别代表一种元素。回答下列问题:
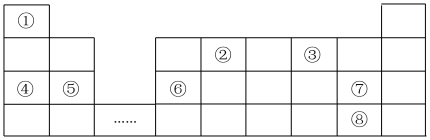
(1)元素①含2个中子的核素为_____ (填符号)。
(2)元素②、③形成的化合物_____ (填“属于”或“不属于”)电解质。
(3)元素③、⑤、⑦形成的简单离子半径由大到小的顺序为_____ (用离子符号填空)。
(4)元素④、⑤、⑥金属性由强到弱的顺序为_____ ,元素④和⑥的最高价氧化物对应的水化物反应的离子方程式为_____ 。
(5)将少量元素⑦的单质通入元素④与元素⑧形成化合物的水溶液中,溶液中的实验现象为_____ ,该反应的离子方程式为_____ 。

(1)元素①含2个中子的核素为
(2)元素②、③形成的化合物
(3)元素③、⑤、⑦形成的简单离子半径由大到小的顺序为
(4)元素④、⑤、⑥金属性由强到弱的顺序为
(5)将少量元素⑦的单质通入元素④与元素⑧形成化合物的水溶液中,溶液中的实验现象为
更新时间:2024-01-10 16:48:59
|
相似题推荐
填空题
|
较易
(0.85)
名校
【推荐1】下表是元素周期表的一部分,回答下列有关问题:
(1)写出①原子结构示意图_______________
(2)在这些元素中,金属性最强的元素是_______ ,(填元素符号)元素⑦与元素⑧相比,非金属性较强的是 _____________ (填元素符号)
(3)⑤的最高价氧化物对应水化物与⑧的最高价氧化物对应水化物反应的离子方程式为:________________
(4)⑤的单质与③的最高价氧化物对应水化物反应的离子方程式为___________________________
(5)已知某元素原子最外层电子数是其次外层电子数的2倍,该元素可以与⑦形成一种AB2型的化合物,请用电子式表示其形成过程:_____________________________ 。
族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
2 | ① | ② | ||||||
3 | ③ | ④ | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ | |
4 | ⑩ | ⑪ | ⑫ |
(1)写出①原子结构示意图
(2)在这些元素中,金属性最强的元素是
(3)⑤的最高价氧化物对应水化物与⑧的最高价氧化物对应水化物反应的离子方程式为:
(4)⑤的单质与③的最高价氧化物对应水化物反应的离子方程式为
(5)已知某元素原子最外层电子数是其次外层电子数的2倍,该元素可以与⑦形成一种AB2型的化合物,请用电子式表示其形成过程:
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐2】下表是元素周期表的一部分,表中所列字母分别代表某一元素。根据表中所列元素,回答下列问题:___________ 。
(2)上表短周期元素中,金属性最强的是___________ (填元素名称);最高价氧化物对应水化物中酸性最强的物质___________ (填化学式,下同);简单气态氢化物最稳定的是___________ 。
(3)表中E、F、G三元素可形成与Ar具有相同电子层结构的简单离子,这些离子的半径由大到小顺序是___________ (用离子符号表示)。
(4)H是目前人类使用最广泛的金属元素。B的最高价含氧酸稀溶液与足量H单质发生反应生成BO的离子方程式为___________ 。

(2)上表短周期元素中,金属性最强的是
(3)表中E、F、G三元素可形成与Ar具有相同电子层结构的简单离子,这些离子的半径由大到小顺序是
(4)H是目前人类使用最广泛的金属元素。B的最高价含氧酸稀溶液与足量H单质发生反应生成BO的离子方程式为
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐3】元素周期表的形式多种多样,下图是扇形元素周期表的一部分,扇面的18折相当于中学化学常见长式元素周期表的18列,1、2、3、4相当于周期,针对表中所给元素,对照中学化学常见长式元素周期表,回答下列问题:
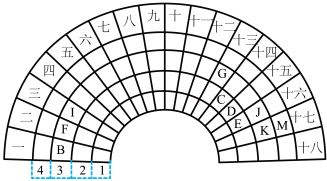
(1)表中金属性最强的元素在长式元素周期表中的位置是___________ ,该元素单质与水反应的化学方程式为______________ 。
(2)表中最高价氧化物对应的水化物酸性最强的是__________ (填酸的化学式)。
(3)元素F与K形成化合物的电子式为__________ 。
(4)写出元素D最高价氧化物对应水化物的稀溶液与铜单质反应的离子方程式_________ 。
(5)元素G的最高价氧化物对应水化物跟氢氧化钠溶液反应的化学方程式________ 。

(1)表中金属性最强的元素在长式元素周期表中的位置是
(2)表中最高价氧化物对应的水化物酸性最强的是
(3)元素F与K形成化合物的电子式为
(4)写出元素D最高价氧化物对应水化物的稀溶液与铜单质反应的离子方程式
(5)元素G的最高价氧化物对应水化物跟氢氧化钠溶液反应的化学方程式
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐1】如图所示为元素周期表的一部分,请回答下列问题:
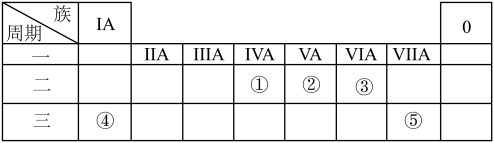
(1)元素②的原子结构示意图是_____ 。
(2)④和⑤两种元素原子半径较小的是______ (填元素符号),①和②两种元素最高价氧化物对应水化物的酸性较强的是_____ (填化学式)。
(3)元素④的单质在元素③的单质中燃烧的化学方程式为_____ 。

(1)元素②的原子结构示意图是
(2)④和⑤两种元素原子半径较小的是
(3)元素④的单质在元素③的单质中燃烧的化学方程式为
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐2】下表是元素周期表的一部分, 针对表中的①~⑨种元素,填写下列空白:
(1)在这些元素中,化学性质最不活泼 的是:_______ (填具体元素符号或化学式 ,下同)。
(2) 在最高价氧化物的水化物中,酸性最强的化合物的分子式是_________ ,第三周期中碱性最强的化合物的化学式是____________________ 。
(3)最高价氧化物是两性氧化物的元素是____________ ;写出它最高价氧化物对应水化物与氢氧化钠反应的化学 方程式_______________________________________ 。
(4)用电子式表示元素④与⑥形成化合物的形成过程:________________________ ,该化合物属于__________________ (填 “共价”或“离子”)化合物。
(5)表示③与①最高价态形成的化合物电子式 ___________________ ,该化合物分子由___________ (填“极性”“非极性”)键形成。
| 族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0族 |
| 2 | ① | ② | ③ | |||||
| 3 | ④ | ⑤ | ⑥ | ⑦ | ⑧ | |||
| 4 | ⑨ |
(1)在这些元素中,化学性质
(2) 在最高价氧化物的水化物中,酸性最强的化合物的分子式是
(3)最高价氧化物是两性氧化物的元素是
(4)用电子式表示元素④与⑥形成化合物的形成过程:
(5)表示③与①最高价态形成的化合物
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐1】1869年俄国化学家门捷列夫制出第一张元素周期表,到现在形成的周期表经过了众多化学家的艰辛努力,历经142年。元素周期表体现了元素位构性的关系,揭示了元素间的内在联系。如图是元素周期表的一部分,回答下列问题:
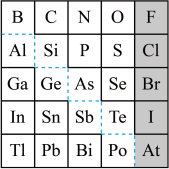
(1)元素Ga在元素周期表中的位置为:第________ 周期第________ 族。
(2)Sn的最高正价为________ ,Cl的最高价氧化物对应水化物的化学式为________ ,Bi的最高价氧化物为________ 。
(3)根据元素周期律,推断:
①阴影部分元素氢化物热稳定性最高的是________ 元素(填元素符号)。
②H3AsO4、H2SeO4的酸性强弱:H3AsO4________ (填“>”“<”或“=”)H2SeO4。
③氢化物的还原性:H2O________ (填“>”“<”或“=”)H2S。
④原子半径比较:N________ (填“>”“<”或“=”)Si。
(4)从下列试剂中选择最佳试剂组合,比较C、Si的非金属性强弱___________________ (可供选择的药品有:CaCO3固体、稀硫酸、盐酸、饱和NaHCO3溶液、饱和Na2CO3溶液、硅酸钠溶液)

(1)元素Ga在元素周期表中的位置为:第
(2)Sn的最高正价为
(3)根据元素周期律,推断:
①阴影部分元素氢化物热稳定性最高的是
②H3AsO4、H2SeO4的酸性强弱:H3AsO4
③氢化物的还原性:H2O
④原子半径比较:N
(4)从下列试剂中选择最佳试剂组合,比较C、Si的非金属性强弱
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐2】液化石油气中常存在少量有毒气体基硫(COS),必须将其脱除以减少环境污染和设备腐蚀。完成下列填空:
(1)羰基硫(COS)所含元素的原子半径从大到小的顺序______ 。
(2)写出羰基硫的电子式______ ,羰基硫分子属于______ (选填“极性”、“非极性”)分子。
(3)下列能说明碳与硫两元素非金属性相对强弱的是______ 。
a.相同条件下水溶液的pH:Na2CO3>Na2SO4 b.酸性:H2SO3>H2CO3
c.CS2中碳元素为+4价,硫元素为-2价 d.浓H2SO4加热能氧化C
(1)羰基硫(COS)所含元素的原子半径从大到小的顺序
(2)写出羰基硫的电子式
(3)下列能说明碳与硫两元素非金属性相对强弱的是
a.相同条件下水溶液的pH:Na2CO3>Na2SO4 b.酸性:H2SO3>H2CO3
c.CS2中碳元素为+4价,硫元素为-2价 d.浓H2SO4加热能氧化C
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐3】下表是元素周期表的一部分,表中所列字母分别代表某一元素。根据表中所列元素,回答下列问题:___________ 。
(2)上表短周期元素中,金属性最强的是___________ (填元素名称);最高价氧化物对应水化物中酸性最强的物质___________ (填化学式,下同);简单气态氢化物最稳定的是___________ 。
(3)表中E、F、G三元素可形成与Ar具有相同电子层结构的简单离子,这些离子的半径由大到小顺序是___________ (用离子符号表示)。
(4)H是目前人类使用最广泛的金属元素。B的最高价含氧酸稀溶液与足量H单质发生反应生成BO的离子方程式为___________ 。

(2)上表短周期元素中,金属性最强的是
(3)表中E、F、G三元素可形成与Ar具有相同电子层结构的简单离子,这些离子的半径由大到小顺序是
(4)H是目前人类使用最广泛的金属元素。B的最高价含氧酸稀溶液与足量H单质发生反应生成BO的离子方程式为
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐1】用A.质子数 B.中子数 C.核外电子数 D.最外层电子数 E.电子层数 填写下列空白:
(1)原子种类由____ 决定;
(2)元素种类由_____ 决定;
(3)核电荷数由____ 决定。
(4)元素的化学性质主要由____ 决定;
(5)元素的原子半径由_______ 决定;
(6)元素的化合价主要由____ 决定。
(1)原子种类由
(2)元素种类由
(3)核电荷数由
(4)元素的化学性质主要由
(5)元素的原子半径由
(6)元素的化合价主要由
您最近一年使用:0次
【推荐2】用 A 质子数 B 中子数 C 核外电子数 D 最外层电子数 E 电子层数 填写下列空白:
(1)原子种类由_______ 决定;
(2)元素种类由_______ 决定;
(3)元素的化学性质主要由_______ 决定;
(4)元素的原子半径由_______ 决定;
(5)元素的化合价主要由_______ 决定。
(1)原子种类由
(2)元素种类由
(3)元素的化学性质主要由
(4)元素的原子半径由
(5)元素的化合价主要由
您最近一年使用:0次

 Cl、
Cl、 Cl;②金刚石、石墨;③O2、O3;④二氧化碳;⑤ H2O、D2O;⑥氯化镁;⑦H、D、T;⑧ Ba(OH)2;⑨ NH4Cl。
Cl;②金刚石、石墨;③O2、O3;④二氧化碳;⑤ H2O、D2O;⑥氯化镁;⑦H、D、T;⑧ Ba(OH)2;⑨ NH4Cl。

