碳酸钠是造纸、玻璃、纺织、制革等工业的重要原料.工业碳酸钠(纯度约为98%)含有 、
、 和
和 等杂质,提纯的工艺如下.
等杂质,提纯的工艺如下.

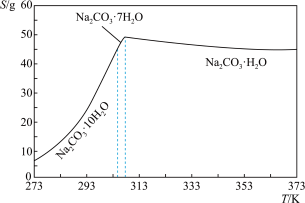
碳酸钠的溶解度(S)随温度变化的曲线如下:
(1)流程中加入NaOH除去的杂质离子是______ .
(2)实验室进行蒸发浓缩结晶用到的主要仪器有______ 、______ .酒精灯、三脚架等.
(3)“趁热过滤”的目的是使析出的晶体为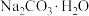 ,防止
,防止______ .
(4)晶体表面沾有母液的处理方法是______ (填操作名称),检测此过程已经完成的操作和现象是______ .
 、
、 和
和 等杂质,提纯的工艺如下.
等杂质,提纯的工艺如下.
碳酸钠的溶解度(S)随温度变化的曲线如下:

(1)流程中加入NaOH除去的杂质离子是
(2)实验室进行蒸发浓缩结晶用到的主要仪器有
(3)“趁热过滤”的目的是使析出的晶体为
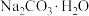 ,防止
,防止(4)晶体表面沾有母液的处理方法是
更新时间:2024-01-03 22:16:06
|
相似题推荐
解答题-实验探究题
|
适中
(0.65)
【推荐1】纯碱在工业上非常重要。
(1)取一定量纯碱细小粉末置于烧杯中,加入一定量的水,可以得到颗粒较大的晶体A。烧杯温度升高,理由是________________________________ ;
(2)从上述烧杯中得到干燥纯净的晶体A,实验程序为:______________ ;(填序号,可重复使用)
①蒸发结晶②放入干燥器③转移入过滤器中④用水洗涤2-3次⑤用乙醇洗涤⑥加热灼烧
(3)取纯净物13.92g晶体A,进行热重分析,直到质量不再改变,生成物质Z,具体数据如下:
通过计算确定样品A的化学式。并写出计算过程。:______________
(1)取一定量纯碱细小粉末置于烧杯中,加入一定量的水,可以得到颗粒较大的晶体A。烧杯温度升高,理由是
(2)从上述烧杯中得到干燥纯净的晶体A,实验程序为:
①蒸发结晶②放入干燥器③转移入过滤器中④用水洗涤2-3次⑤用乙醇洗涤⑥加热灼烧
(3)取纯净物13.92g晶体A,进行热重分析,直到质量不再改变,生成物质Z,具体数据如下:
| 物质 | 样品A | T1℃下得到物质X | T2℃下得到物质Y | 600℃时得到物质Z |
| 质量/g | 13.92 | 11.75 | 7.45 | 6.36 |
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐2】碳酸氢钠用途广泛。可广泛应用于医疗、生活、生产中。回答下列问题:
(1)碳酸氢钠能中和胃酸,碳酸氢钠属于_______ (填“酸”“碱”“盐”)
(2)碳酸氢钠能与醋酸配制复合膨松剂。其蓬松原理是_______ 。(用化学方程式说明)
(3)生活中可用碳酸氢钠蒸馒头,用化学方程式解释其原理_______ 。将碳酸氢钠加入面团中,若理论上生成二氧化碳0.1mol,需要碳酸氢钠的质量是_______ 克。
(4)碳酸钠和碳酸氢钠是厨房中常见用品,为鉴别它们,取等质量的样品分别加入如图所示装置的气囊中做对比实验,依据_______ 现象推断哪种样品为碳酸氢钠;写出该反应的化学方程式_______ 。除酸外还可以选择_______ 试剂进行碳酸钠和碳酸氢钠鉴别(写名称)

(1)碳酸氢钠能中和胃酸,碳酸氢钠属于
(2)碳酸氢钠能与醋酸配制复合膨松剂。其蓬松原理是
(3)生活中可用碳酸氢钠蒸馒头,用化学方程式解释其原理
(4)碳酸钠和碳酸氢钠是厨房中常见用品,为鉴别它们,取等质量的样品分别加入如图所示装置的气囊中做对比实验,依据

您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐3】氢气作为清洁能源有着广泛的应用前景,含硫天然气制备氢气的流程如下。

请回答下列问题:
I.转化脱硫:将天然气压入吸收塔,30℃时,在T.F菌作用下,酸性环境中脱硫过程示意图如下。

(1)过程i的离子反应方程式为_________________________________________ 。
(2)已知:
①Fe3+在pH=l.9时开始沉淀,pH=3.2时沉淀完全。
②30℃时,在T.F菌作用下,不同pH的FeSO4溶液中Fe2+的氧化速率如下表。
在转化脱硫中,请在上表中选择最佳pH范围是_______ <pH<_______ ,这样选择的原因是:_______________________________________________ 。
Ⅱ.蒸气转化:在催化剂的作用下,水蒸气将CH4氧化。结合下图回答问题。

(3)①该过程的热化学方程式是__________________________________________ 。
②比较压强P1和p2的大小关系:P1_________ P2(选填“>”“<”或“=”)。
③在一定温度和一定压强下的体积可变的密闭容器中充入1molCH4和1mol的水蒸气充分反应达平衡后,测得起始时混合气的密度是平衡时混合气密度的1.4倍,若此时容器的体积为2L,则该反应的平衡常数为______________ (结果保留2位有效数字)。
Ⅲ.CO变换:500℃时,CO进一步与水反应生成CO2和H2。
Ⅳ.H2提纯:将CO2和H2分离得到H2的过程如示意图

(4)吸收池中发生反应的离子方程式是____________________________________ 。

请回答下列问题:
I.转化脱硫:将天然气压入吸收塔,30℃时,在T.F菌作用下,酸性环境中脱硫过程示意图如下。

(1)过程i的离子反应方程式为
(2)已知:
①Fe3+在pH=l.9时开始沉淀,pH=3.2时沉淀完全。
②30℃时,在T.F菌作用下,不同pH的FeSO4溶液中Fe2+的氧化速率如下表。
| pH | 0.7 | 1.1 | 1.5 | 1.9 | 2.3 | 2.7 |
| Fe2+的氧化速率/g·L-1·h-1 | 4.5 | 5.3 | 6.2 | 6.8 | 7.0 | 6.6 |
Ⅱ.蒸气转化:在催化剂的作用下,水蒸气将CH4氧化。结合下图回答问题。

(3)①该过程的热化学方程式是
②比较压强P1和p2的大小关系:P1
③在一定温度和一定压强下的体积可变的密闭容器中充入1molCH4和1mol的水蒸气充分反应达平衡后,测得起始时混合气的密度是平衡时混合气密度的1.4倍,若此时容器的体积为2L,则该反应的平衡常数为
Ⅲ.CO变换:500℃时,CO进一步与水反应生成CO2和H2。
Ⅳ.H2提纯:将CO2和H2分离得到H2的过程如示意图

(4)吸收池中发生反应的离子方程式是
您最近一年使用:0次
【推荐1】中药药剂As2O3可从未处理的工业酸性高浓度含砷废水(As主要以H3AsO3形式存在,还含Fe2+、Cu2+)中提炼,其工艺流程如图

已知:①沉渣加碱过程中发生的反应都是非氧化还原反应。
②FeS+2NaOH=Na2S+Fe(OH)2;CuS不与NaOH溶液反应。
(1)H3AsO3中As的化合价为______ 价。
(2)“操作a”是______ (填“过滤”或“分液”),“沉渣”的主要成分是As2S3、_____ (填化学式,下同),“滤液a”中除Na3AsO3和Na3AsS3外,还含有的溶质是______ 。
(3)从绿色化学角度分析,“氧化脱硫”的过程中可以选择的氧化剂是_____ (填标号),该过程还生成了S,该过程中反应的离子方程式为_______ 。
A.浓硝酸 B.酸性KMnO4溶液
C.氯水 D.双氧水
(4)用SO2还原时,氧化剂与还原剂的物质的量之比为____________ 。
(5)通过双氧水氧化(NH4)2[AsCl5]溶液可制得As2O5(溶液中还含有大量NH3·H2O),该反应中As2O5形成胶体,溶液始终接近中性,反应的离子方程式为_________ 。

已知:①沉渣加碱过程中发生的反应都是非氧化还原反应。
②FeS+2NaOH=Na2S+Fe(OH)2;CuS不与NaOH溶液反应。
(1)H3AsO3中As的化合价为
(2)“操作a”是
(3)从绿色化学角度分析,“氧化脱硫”的过程中可以选择的氧化剂是
A.浓硝酸 B.酸性KMnO4溶液
C.氯水 D.双氧水
(4)用SO2还原时,氧化剂与还原剂的物质的量之比为
(5)通过双氧水氧化(NH4)2[AsCl5]溶液可制得As2O5(溶液中还含有大量NH3·H2O),该反应中As2O5形成胶体,溶液始终接近中性,反应的离子方程式为
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
【推荐2】工业上用含有Fe、Cu、Al的合金废料进行一系列化工处理,制胆矾、绿矾(FeSO4·7H2O),并回收得到金属铝,流程如图。
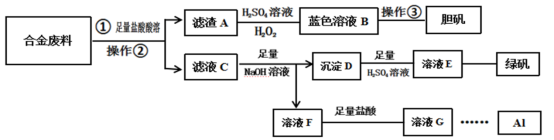
回答下列问题:
(1)操作②为_______ ,用到的玻璃仪器有_______
(2)操作③为_______
(3)能否通过电解溶液G制得金属Al,_______ (填“能”或“不能”)。
(4)沉淀D暴露在空气中容易被空气氧化而使最后制得的绿矾不纯,可以向溶液E中加入过量_______ ,过滤后取滤液再制得绿矾。沉淀D被空气氧化的现象为_______
(5)写出由滤渣A得到蓝色溶液B的化学反应方程式_______
(6)若将①改为加足量的NaOH溶液,发生反应的离子方程式为_______

回答下列问题:
(1)操作②为
(2)操作③为
(3)能否通过电解溶液G制得金属Al,
(4)沉淀D暴露在空气中容易被空气氧化而使最后制得的绿矾不纯,可以向溶液E中加入过量
(5)写出由滤渣A得到蓝色溶液B的化学反应方程式
(6)若将①改为加足量的NaOH溶液,发生反应的离子方程式为
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
【推荐3】二茂铁在常温下为橙黄色粉末,有樟脑气味,用作节能、消烟、助燃添加剂等。可用下列方法合成:

回答下列问题:
(1)室温下,环戊二烯以二聚体的形式存在。某实验小组要得到环戊二烯,需先将环戊二烯二聚体解聚,已知:

①分离得到环戊二烯的操作为_____________________ (填操作名称)。
②由环戊二烯生成C5H5K的化学方程式为___________________ 。
(2)流程中所需的FeCl2·4H2O可通过下列步骤制得。
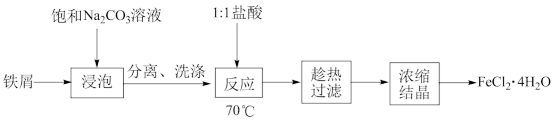
①用饱和Na2CO3溶液“浸泡”铁屑的目的是_____________________________ 。
②采用“趁热过滤”,其原因是____________________________ 。
(3)用电解法制备二茂铁时:
①不断通入N2的目的是__________________________ 。
②Ni电极与电源的____________ (填“正极”或“负极”)相连,电解过程中阳极的电极反应式为__________________ ,理论上电路中每转移1 mol电子,得到产品的质量为____ 。

回答下列问题:
(1)室温下,环戊二烯以二聚体的形式存在。某实验小组要得到环戊二烯,需先将环戊二烯二聚体解聚,已知:

①分离得到环戊二烯的操作为
②由环戊二烯生成C5H5K的化学方程式为
(2)流程中所需的FeCl2·4H2O可通过下列步骤制得。

①用饱和Na2CO3溶液“浸泡”铁屑的目的是
②采用“趁热过滤”,其原因是
(3)用电解法制备二茂铁时:
①不断通入N2的目的是
②Ni电极与电源的
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐1】如图为实验室制取蒸馏水的装置示意图,根据图示回答下列问题。

(1)图中有两处明显的错误是:
①_______ ;②_______ 。
(2)A仪器的名称是_______ , B仪器的名称是_______ 。
(3)实验时A中除加入少量自来水外,还需要加入少量的_______ ,其作用是_______ 。
(4)阅读、分析下列两个材料。
材料1:

材料2:
回答下列问题(填写序号):
A.蒸馏法 B.萃取法 C.“溶解、结晶、过滤”的方法 D.分液法
将纯碱从氯化钠和纯碱的混合物中分离出来,最好应用_______ 。将乙二醇和丙三醇分离的最佳方法是_______ 。

(1)图中有两处明显的错误是:
①
(2)A仪器的名称是
(3)实验时A中除加入少量自来水外,还需要加入少量的
(4)阅读、分析下列两个材料。
材料1:

材料2:
| 物质 | 熔点/℃ | 沸点/℃ | 密度/g/cm | 溶解性 |
| 乙二醇(C2H6O2) | -11.5 | 198 | 1.11 | 易溶于水和乙醇 |
| 丙三醇(C3H8O3) | 17.9 | 290 | 1.26 | 能跟水、酒精以任意比互溶 |
A.蒸馏法 B.萃取法 C.“溶解、结晶、过滤”的方法 D.分液法
将纯碱从氯化钠和纯碱的混合物中分离出来,最好应用
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐2】选择下列实验方法分离物质,将分离方法的序号填在横线上。
A.萃取 B.蒸发 C.结晶 D.过滤 E.蒸馏 F.分液
(1)除去氢氧化钙溶液中悬浮的氢氧化钙颗粒______
(2)从硝酸钾和氯化钾的混合液中获得硝酸钾______
(3)从饱和食盐水中获得食盐______
(4)分离柴油和水的混合物______
(5)提取溴水中的溴______
(6)分离CCl4(沸点为76.75℃)和甲苯(沸点为110.6℃)的混合物______
A.萃取 B.蒸发 C.结晶 D.过滤 E.蒸馏 F.分液
(1)除去氢氧化钙溶液中悬浮的氢氧化钙颗粒
(2)从硝酸钾和氯化钾的混合液中获得硝酸钾
(3)从饱和食盐水中获得食盐
(4)分离柴油和水的混合物
(5)提取溴水中的溴
(6)分离CCl4(沸点为76.75℃)和甲苯(沸点为110.6℃)的混合物
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐3】某工厂排放的废液中含有大量的K+、Cl-、Br-,还有少量的Ca2+、Mg2+、SO42-。某研究性小组利用这种废液来制取较纯净的氯化钾晶体及液溴,他们设计了如下的流程(提示:图中试剂a的作用是将Br-转化为Br2)

试剂b需要从以下试剂中选择:饱和Na2CO3溶液、饱和K2CO3溶液、KOH溶液、BaCl2溶液、Ba(NO3)2溶液、稀盐酸
(1)操作①②③④⑤的名称是________ (填序号)。
A. 萃取、过滤、分液、过滤、蒸发结晶
B. 萃取、分液、蒸馏、过滤、蒸发结晶
C. 分液、萃取、过滤、过滤、蒸发结晶
D. 萃取、分液、分液、过滤、蒸发结晶
(2)除去无色液体Ⅰ中的Ca2+、Mg2+、SO42-,选出试剂b(试剂b代表一组试剂)所代表的试剂,按滴加顺序依次是_____________________________________________________________ 。
(3)调节pH=7的作用是________________________________________ ,所用的试剂是___________ (填名称)
(4)操作⑤中用到的瓷质仪器名称是________________

试剂b需要从以下试剂中选择:饱和Na2CO3溶液、饱和K2CO3溶液、KOH溶液、BaCl2溶液、Ba(NO3)2溶液、稀盐酸
(1)操作①②③④⑤的名称是
A. 萃取、过滤、分液、过滤、蒸发结晶
B. 萃取、分液、蒸馏、过滤、蒸发结晶
C. 分液、萃取、过滤、过滤、蒸发结晶
D. 萃取、分液、分液、过滤、蒸发结晶
(2)除去无色液体Ⅰ中的Ca2+、Mg2+、SO42-,选出试剂b(试剂b代表一组试剂)所代表的试剂,按滴加顺序依次是
(3)调节pH=7的作用是
(4)操作⑤中用到的瓷质仪器名称是
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐1】盐X由三种元素组成,其具有良好的热电性能,在热电转换领域具有广阔的应用前景。为研究它的组成和性质,现取12.30 g化合物X进行如下实验:

试根据以上内容回答下列问题:
(1)组成X的三种元素中除了O元素外的另外两种是_______ (写元素符号)。
(2)无色溶液B中通入过量 产生白色沉淀C的离子方程式为
产生白色沉淀C的离子方程式为_______ 。
(3)蓝色溶液F中通入中 气体会产生白色沉淀,该沉淀仅含两种元素其中氯元素质量分数为35.7%,其离子方程式为
气体会产生白色沉淀,该沉淀仅含两种元素其中氯元素质量分数为35.7%,其离子方程式为_______ 。
(4)白色沉淀C煅烧的固体产物与D高温反应可生成化合物X,并释放出一种无色无味的气体,其化学方程式为_______ 。
(5)写出简要实验步骤检验无色溶液E中的主要阴离子:_______ 。

试根据以上内容回答下列问题:
(1)组成X的三种元素中除了O元素外的另外两种是
(2)无色溶液B中通入过量
 产生白色沉淀C的离子方程式为
产生白色沉淀C的离子方程式为(3)蓝色溶液F中通入中
 气体会产生白色沉淀,该沉淀仅含两种元素其中氯元素质量分数为35.7%,其离子方程式为
气体会产生白色沉淀,该沉淀仅含两种元素其中氯元素质量分数为35.7%,其离子方程式为(4)白色沉淀C煅烧的固体产物与D高温反应可生成化合物X,并释放出一种无色无味的气体,其化学方程式为
(5)写出简要实验步骤检验无色溶液E中的主要阴离子:
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐2】今有一混合物的水溶液,初步确定只可能含有以下离子中的若干种:K+、 、Cl-、Ca2+、Ba2+、
、Cl-、Ca2+、Ba2+、 、
、 ,现取三份该溶液各100 mL进行如下实验:
,现取三份该溶液各100 mL进行如下实验:
第一份溶液中,滴加AgNO3溶液,有沉淀产生;
第二份溶液中,加入足量NaOH浓溶液共热,收集到0.08 mol气体;
第三份溶液中,加入足量BaCl2 溶液后,得到干燥沉淀12.54 g,经足量的盐酸洗涤、干燥后,沉淀质量为4.66 g。
根据上述实验,回答以下问题:
(1)由第一份进行的实验推断该混合物是否一定含有Cl-_____________ (填“是”或“否”)
(2)由第二份进行的实验可知原溶液中含_______ 离子(填化学式),其物质的量浓度为________________________ 。
(3)由第三份进行的实验可知12.54g沉淀的成分为_______________________ (填化学式)。原混合溶液中,形成该沉淀对应的离子的物质的量浓度为________________ 。
(4)综合上述实验结果,你认为以下结论正确的是_____ 。
A.该混合物中一定含有K+、 、
、 、
、 ,可能含有Cl-
,可能含有Cl-
B.该混合物中一定含有 、
、 、
、 、Cl-,可能含有Ca2+、K+
、Cl-,可能含有Ca2+、K+
C.该混合物中一定含有 、
、 、
、 ,可能含有K+、Cl-
,可能含有K+、Cl-
D.该混合物中一定含有 、
、 、Cl-,可能含有Ca2+、K+
、Cl-,可能含有Ca2+、K+
(5)写出向Ba(OH)2溶液中滴入过量NaHSO4溶液反应的离子方程式_______________ 。
 、Cl-、Ca2+、Ba2+、
、Cl-、Ca2+、Ba2+、 、
、 ,现取三份该溶液各100 mL进行如下实验:
,现取三份该溶液各100 mL进行如下实验:第一份溶液中,滴加AgNO3溶液,有沉淀产生;
第二份溶液中,加入足量NaOH浓溶液共热,收集到0.08 mol气体;
第三份溶液中,加入足量BaCl2 溶液后,得到干燥沉淀12.54 g,经足量的盐酸洗涤、干燥后,沉淀质量为4.66 g。
根据上述实验,回答以下问题:
(1)由第一份进行的实验推断该混合物是否一定含有Cl-
(2)由第二份进行的实验可知原溶液中含
(3)由第三份进行的实验可知12.54g沉淀的成分为
(4)综合上述实验结果,你认为以下结论正确的是
A.该混合物中一定含有K+、
 、
、 、
、 ,可能含有Cl-
,可能含有Cl-B.该混合物中一定含有
 、
、 、
、 、Cl-,可能含有Ca2+、K+
、Cl-,可能含有Ca2+、K+C.该混合物中一定含有
 、
、 、
、 ,可能含有K+、Cl-
,可能含有K+、Cl-D.该混合物中一定含有
 、
、 、Cl-,可能含有Ca2+、K+
、Cl-,可能含有Ca2+、K+(5)写出向Ba(OH)2溶液中滴入过量NaHSO4溶液反应的离子方程式
您最近一年使用:0次

 、MnO
、MnO 、CO
、CO 、SO
、SO 中的若干种离子组成,取溶液进行如下连续实验:
中的若干种离子组成,取溶液进行如下连续实验:


