某小组通过实验研究 与水的反应.
与水的反应.
(1) 与水反应的化学方程式是
与水反应的化学方程式是_________________________ .
(2)ii中溶液褪色可能是溶液a中存在较多的 ,
, 与酚酞发生了反应.
与酚酞发生了反应.
Ⅰ.甲同学通过实验证实了 的存在:取少量溶液a,加入试剂
的存在:取少量溶液a,加入试剂_________ (填化学式),有气体产生.
Ⅱ.乙同学查阅资料获悉:用稀 酸化的
酸化的 可以测定
可以测定 的含量.反应过程中会产生气体,则
的含量.反应过程中会产生气体,则 与
与 反应的离子方程式是
反应的离子方程式是___________________________________________________ .
(3)为探究现象ii产生的原因,同学们继续进行了如下实验:
Ⅰ.向 溶液中滴入两滴酚酞,振荡,加入5滴
溶液中滴入两滴酚酞,振荡,加入5滴 溶液,溶液变红且产生气体,10分钟后溶液变无色,该过程无明显热效应.
溶液,溶液变红且产生气体,10分钟后溶液变无色,该过程无明显热效应.
Ⅱ.向 溶液中滴入两滴酚酞,振荡,溶液变红,10分钟后溶液颜色无明显变化;向该溶液中通入氧气,溶液颜色无明显变化.
溶液中滴入两滴酚酞,振荡,溶液变红,10分钟后溶液颜色无明显变化;向该溶液中通入氧气,溶液颜色无明显变化.
① 从实验Ⅰ和Ⅱ中,可得出的结论是______________________________
② 同学们进一步通过实验证实了溶液a中滴入酚酞后, 与酚酞发生了化学反应.实验方案是:取少量溶液a于试管中,
与酚酞发生了化学反应.实验方案是:取少量溶液a于试管中,____________________________
 与水的反应.
与水的反应.| 操作 | 现象 |
向盛有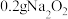 的烧杯中加入50mL蒸馏水 的烧杯中加入50mL蒸馏水 | 剧烈反应,产生能使带火星木条复燃的气体,得到的溶液a能产生丁达尔效应 |
| 向溶液a中滴入两滴酚酞 | i.溶液变红 ii.10分钟后溶液颜色明显变浅,稍后,溶液变为无色 |
(1)
 与水反应的化学方程式是
与水反应的化学方程式是(2)ii中溶液褪色可能是溶液a中存在较多的
 ,
, 与酚酞发生了反应.
与酚酞发生了反应.Ⅰ.甲同学通过实验证实了
 的存在:取少量溶液a,加入试剂
的存在:取少量溶液a,加入试剂Ⅱ.乙同学查阅资料获悉:用稀
 酸化的
酸化的 可以测定
可以测定 的含量.反应过程中会产生气体,则
的含量.反应过程中会产生气体,则 与
与 反应的离子方程式是
反应的离子方程式是(3)为探究现象ii产生的原因,同学们继续进行了如下实验:
Ⅰ.向
 溶液中滴入两滴酚酞,振荡,加入5滴
溶液中滴入两滴酚酞,振荡,加入5滴 溶液,溶液变红且产生气体,10分钟后溶液变无色,该过程无明显热效应.
溶液,溶液变红且产生气体,10分钟后溶液变无色,该过程无明显热效应.Ⅱ.向
 溶液中滴入两滴酚酞,振荡,溶液变红,10分钟后溶液颜色无明显变化;向该溶液中通入氧气,溶液颜色无明显变化.
溶液中滴入两滴酚酞,振荡,溶液变红,10分钟后溶液颜色无明显变化;向该溶液中通入氧气,溶液颜色无明显变化.① 从实验Ⅰ和Ⅱ中,可得出的结论是
② 同学们进一步通过实验证实了溶液a中滴入酚酞后,
 与酚酞发生了化学反应.实验方案是:取少量溶液a于试管中,
与酚酞发生了化学反应.实验方案是:取少量溶液a于试管中,
23-24高一上·北京·阶段练习 查看更多[2]
更新时间:2024-01-05 13:57:10
|
相似题推荐
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐1】如图中A为一种常见的单质,B、C、D、E是含有A元素的常见化合物。它们的焰色试验均为黄色。

(1)等量的钠分别与足量氧气在常温和加热条件下反应,分别生成Na2O和Na2O2。两个反应转移的电子数:_______ (填“前者多”“后者多”“一样多”)
(2)写出反应④的化学方程式为_______ 。
(3)实验室常用饱和的_______ 溶液(从D,E中选择)除去CO2中混有的HCl,写出反应的离子方程式:_______ 。
(4)加热5.00gD和E的固体混合物,使E完全分解。固体混合物的质量减少了0.31g则原混合物中D的质量为_______ 。

(1)等量的钠分别与足量氧气在常温和加热条件下反应,分别生成Na2O和Na2O2。两个反应转移的电子数:
(2)写出反应④的化学方程式为
(3)实验室常用饱和的
(4)加热5.00gD和E的固体混合物,使E完全分解。固体混合物的质量减少了0.31g则原混合物中D的质量为
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐2】含氮化合物是重要的化工原料。存在如下转化关系:

(1)转化Ⅱ中发生的系列反应,在工业上可以用来制备硝酸,写出①中反应的化学方程式:_______ 。
(2)①工业上常用浓氨水检验氯气管道是否泄漏,若泄漏可看到白烟,用化学方程式解释检验原理:_______ 。
②向固体氧化钙中滴加浓氨水,可用于实验室制取少量氨,请写出化学方程式:_______ 。
(3)现代工业常以氯化钠、二氧化碳和氨为原料制备纯碱。
①向一水合氨中通入过量的CO2,该反应的离子方程式为_______ 。
②某工业纯碱样品中含少量NaCl和NaHCO3,为测定该样品中NaHCO3的质量分数,某同学设计方案如下:准确称取100.00g样品,反复加热、冷却、称量,直至所称量的固体质量几乎不变为止,此时所得固体的质量为99.38g。样品中NaHCO3的质量分数为_______ 。

(1)转化Ⅱ中发生的系列反应,在工业上可以用来制备硝酸,写出①中反应的化学方程式:
(2)①工业上常用浓氨水检验氯气管道是否泄漏,若泄漏可看到白烟,用化学方程式解释检验原理:
②向固体氧化钙中滴加浓氨水,可用于实验室制取少量氨,请写出化学方程式:
(3)现代工业常以氯化钠、二氧化碳和氨为原料制备纯碱。
①向一水合氨中通入过量的CO2,该反应的离子方程式为
②某工业纯碱样品中含少量NaCl和NaHCO3,为测定该样品中NaHCO3的质量分数,某同学设计方案如下:准确称取100.00g样品,反复加热、冷却、称量,直至所称量的固体质量几乎不变为止,此时所得固体的质量为99.38g。样品中NaHCO3的质量分数为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐1】一氯化碘(ICl)是一种卤素互化物。卤素互化物具有强氧化性稀溶液,可与金属直接反应,也可用作有机合成中的碘化剂,一般可由卤素单质直接化合制得。有关一氯化碘制备及性质验证,请回答下列问题:
I.海藻提碘可得到I2的CCl4溶液,从其中回收I2的流程如下:
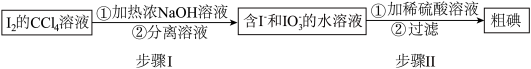
(1)步骤I的分离溶液操作中,主要用到的玻璃仪器有烧杯和_______ ,步骤Ⅱ的反应中氧化剂与还原剂的物质的量之比为_______ 。
(2)回收获得的粗碘可采用如图所示的简易装置分离提纯。将粉状物放入蒸发皿中并小火加热,碘晶体在扎有小孔的滤纸上凝结,该分离提纯方法的名称是_______ 。

Ⅱ.某学习小组在实验室中拟用下图装置制取纯净、干燥的氯气,并利用氯气与碘反应制备一氯化碘。
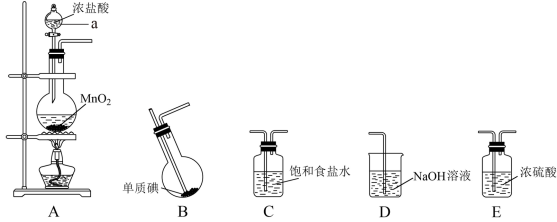
查阅资料了解到以下内容:
①碘与氯气的反应为放热反应
②ICl是一种红棕色液体,沸点97.4℃,不溶于水
③ICl能与KI反应生成I2
请回答下列问题:
(3)各装置连接顺序为A→_______→_______→_______→_______;_______
(4)B装置烧瓶需放在冷水中,其目的是:_______ ,B装置得到的液态产物进一步提纯可得到较纯净的ICl,采取的方法是_______ 。
(5)ICl与稀NaOH溶液可发生非氧化还原反应,请写出该反应的离子方程式_______ 。
(6)请设计简单的实验证明ICl的氧化性比I2强:_______ 。
I.海藻提碘可得到I2的CCl4溶液,从其中回收I2的流程如下:

(1)步骤I的分离溶液操作中,主要用到的玻璃仪器有烧杯和
(2)回收获得的粗碘可采用如图所示的简易装置分离提纯。将粉状物放入蒸发皿中并小火加热,碘晶体在扎有小孔的滤纸上凝结,该分离提纯方法的名称是

Ⅱ.某学习小组在实验室中拟用下图装置制取纯净、干燥的氯气,并利用氯气与碘反应制备一氯化碘。

查阅资料了解到以下内容:
①碘与氯气的反应为放热反应
②ICl是一种红棕色液体,沸点97.4℃,不溶于水
③ICl能与KI反应生成I2
请回答下列问题:
(3)各装置连接顺序为A→_______→_______→_______→_______;
(4)B装置烧瓶需放在冷水中,其目的是:
(5)ICl与稀NaOH溶液可发生非氧化还原反应,请写出该反应的离子方程式
(6)请设计简单的实验证明ICl的氧化性比I2强:
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐2】某校化学课外小组用硫酸铁废液(含少量硫酸铜和稀硫酸),制备硫酸亚铁晶体并进行如下实验。制备硫酸亚铁晶体主要的操作流程如下:

请根据题目要求回答下列问题:
(1)A的化学式为___________ ,上述操作过程中用到的玻璃仪器有:①烧杯、②③玻璃棒、③酒精灯、④温度计、⑤____________ 。
(2)趁热过滤的目的是__________ 。
(3)结晶操作过程中应控制滤液酸性的原因是______________
(4)已知硫酸亚铁铵[(NH4)2Fe(SO4)2]比硫酸亚铁稳定,用在分析化学中。硫酸亚铁铵可用硫酸铵和硫酸亚铁反应制得。实验室利用硫酸亚铁铵溶液和草酸溶液反应生成草酸亚铁沉淀来制备草酸亚铁。写出硫酸亚铁铵溶液与草酸溶液反应的离子方程式________ 。
(5)草酸亚铁晶体(相对分子质量180)受热易分解,某课外小组设计如图的实验装置来检验其分解产物。

①该装置中最不合理的部分_____________ (填字母),原因是_________ 。
②改用正确装置实验开始后,B处变蓝,说明草酸亚铁晶体中有__________ ;C处有白色沉淀,E处部分黑色粉末变为红色,说明草酸亚铁分解产生___ (填化学式)。

请根据题目要求回答下列问题:
(1)A的化学式为
(2)趁热过滤的目的是
(3)结晶操作过程中应控制滤液酸性的原因是
(4)已知硫酸亚铁铵[(NH4)2Fe(SO4)2]比硫酸亚铁稳定,用在分析化学中。硫酸亚铁铵可用硫酸铵和硫酸亚铁反应制得。实验室利用硫酸亚铁铵溶液和草酸溶液反应生成草酸亚铁沉淀来制备草酸亚铁。写出硫酸亚铁铵溶液与草酸溶液反应的离子方程式
(5)草酸亚铁晶体(相对分子质量180)受热易分解,某课外小组设计如图的实验装置来检验其分解产物。

①该装置中最不合理的部分
②改用正确装置实验开始后,B处变蓝,说明草酸亚铁晶体中有
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐3】太和一中理化创新社的同学们为了探究在实验室制备 的过程中有水蒸气和
的过程中有水蒸气和 挥发出来,同时证明氯气的某些性质,甲同学设计了如图所示的实验装置(支撑用的铁架台省略),按要求回答问题。
挥发出来,同时证明氯气的某些性质,甲同学设计了如图所示的实验装置(支撑用的铁架台省略),按要求回答问题。

(1)若用含有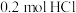 的浓盐酸与足量的
的浓盐酸与足量的 反应制
反应制 ,制得的
,制得的 体积(标准状况下)总是小于
体积(标准状况下)总是小于 的原因是
的原因是_____________________ 。
(2)①装置B的作用是_______________________ ,现象是_____________________ 。
②装置C和D出现的不同现象说明的问题是__________________________ 。
③装置E的作用是_______________________________ 。
(3)乙同学认为甲同学的实验有缺陷,不能确保最终通入 溶液中的气体只有一种。为了确保实验结论的可靠性,证明最终通入
溶液中的气体只有一种。为了确保实验结论的可靠性,证明最终通入 溶液的气体只有一种,乙同学提出在某两个装置之间再加一个装置。你认为该装置应加在
溶液的气体只有一种,乙同学提出在某两个装置之间再加一个装置。你认为该装置应加在_________ 与_________ 之间(填装置字母序号),装置中应放入___________________________ 。
 的过程中有水蒸气和
的过程中有水蒸气和 挥发出来,同时证明氯气的某些性质,甲同学设计了如图所示的实验装置(支撑用的铁架台省略),按要求回答问题。
挥发出来,同时证明氯气的某些性质,甲同学设计了如图所示的实验装置(支撑用的铁架台省略),按要求回答问题。
(1)若用含有
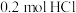 的浓盐酸与足量的
的浓盐酸与足量的 反应制
反应制 ,制得的
,制得的 体积(标准状况下)总是小于
体积(标准状况下)总是小于 的原因是
的原因是(2)①装置B的作用是
②装置C和D出现的不同现象说明的问题是
③装置E的作用是
(3)乙同学认为甲同学的实验有缺陷,不能确保最终通入
 溶液中的气体只有一种。为了确保实验结论的可靠性,证明最终通入
溶液中的气体只有一种。为了确保实验结论的可靠性,证明最终通入 溶液的气体只有一种,乙同学提出在某两个装置之间再加一个装置。你认为该装置应加在
溶液的气体只有一种,乙同学提出在某两个装置之间再加一个装置。你认为该装置应加在
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐1】工业上由含铜废料(含有Cu、CuS、CuSO4等)制备硝酸铜晶体的流程如图:
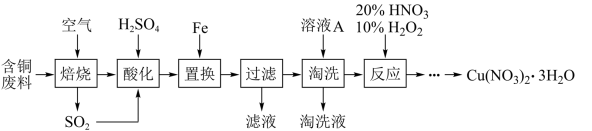
(1)写出CuS“焙烧”生成CuO和SO2的化学反应方程式:___________ 。
(2)图中SO2经转化生成的硫酸可用于“酸化”,转化反应中SO2与O2的物质的量之比为:_____ 。
(3)滤液的主要成分是___________ 。
(4)写出步骤中加10%H2O2的离子方程式:___________ 。
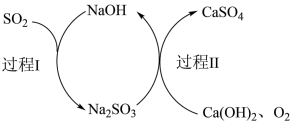
(5)大量排放SO2容易造成酸雨等环境问题,工业上可用双碱脱硫法处理废气。过程如图所示,其中可循环使用的试剂是___________ ,写出双碱脱硫法的总反应的化学方程式:___________ 。

(1)写出CuS“焙烧”生成CuO和SO2的化学反应方程式:
(2)图中SO2经转化生成的硫酸可用于“酸化”,转化反应中SO2与O2的物质的量之比为:
(3)滤液的主要成分是
(4)写出步骤中加10%H2O2的离子方程式:
(5)大量排放SO2容易造成酸雨等环境问题,工业上可用双碱脱硫法处理废气。过程如图所示,其中可循环使用的试剂是

您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐2】硫酸铁铵晶体[NH4Fe(SO4)2•xH2O]用途十分广泛,可用作聚合催化剂、媒染剂等。实验室可用废铁屑制备硫酸铁铵,流程如图所示。

回答下列问题:
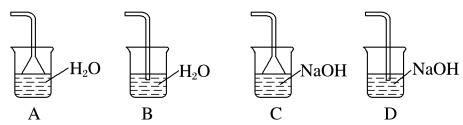
(1)步骤②需要加热的目的是_____ ,温度保持80~95℃,采用的合适加热方式是_____ 。铁屑中含有少量硫化物,反应产生的气体需要净化处理,合适的装置为_____ (填标号)。
(2)步骤③中选用足量的H2O2,理由是____ 。
(3)步骤⑤的具体实验操作有____ 、____ 、____ ,经干燥得到硫酸铁铵晶体样品。
(4)称取硫酸铁铵产品4.820g溶于水中,转入100mL容量瓶定容。每次取20.00mL溶液放入烧杯,加入NaOH溶液调节至碱性,再加入足量BaCl2溶液后过滤,将沉淀干燥并灼烧至恒重,称取固体质量。三次称量固体的平均值为1.092g。通过计算写出该硫酸铁铵晶体的化学式为____ 。

回答下列问题:
(1)步骤②需要加热的目的是

(2)步骤③中选用足量的H2O2,理由是
(3)步骤⑤的具体实验操作有
(4)称取硫酸铁铵产品4.820g溶于水中,转入100mL容量瓶定容。每次取20.00mL溶液放入烧杯,加入NaOH溶液调节至碱性,再加入足量BaCl2溶液后过滤,将沉淀干燥并灼烧至恒重,称取固体质量。三次称量固体的平均值为1.092g。通过计算写出该硫酸铁铵晶体的化学式为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐3】物质A-J有下图转化关系,反应条件均略去。A、B物质的组成元素相同,C、D、G是初中化学中常见的单质,I是金属。H的相对分子质量为100,组成元素的原子个数比为3∶2,其中一种元素的质量分数为28%。E的浓溶液具有挥发性。

试回答:
(1)上述转化中属于分解反应的是___________ (填序号)
(2)A、J、H的化学式为:A___________ ;J____________ ;H____________ ;A的常见用途(任写一种):___________
(3)反应②的化学方程式为___________ ;反应⑤的化学方程式为___________ 。

试回答:
(1)上述转化中属于分解反应的是
(2)A、J、H的化学式为:A
(3)反应②的化学方程式为
您最近一年使用:0次


 的反应中氧化剂与还原剂的物质的量之比为
的反应中氧化剂与还原剂的物质的量之比为

