I.写出下列反应的化学方程式。
(1)NaHCO3受热分解:_______ 。
(2)H2在Cl2中燃烧:_______ 。
(3)Na2O2和水反应:_______ 。
(4)Na2O2和CO2反应:_______ 。
(5)Na在空气中燃烧:_______ 。
(6)HClO见光分解:_______ 。
II.写出下列反应的离子方程式:
(7)Cl2和水反应:_______ 。
(8)Na和水反应:_______ 。
(9)NaOH溶液和NaHCO3溶液反应:_______ 。
(10)NaHCO3与少量石灰水:_______ 。
(11)NaHCO3与过量石灰水:_______ 。
(1)NaHCO3受热分解:
(2)H2在Cl2中燃烧:
(3)Na2O2和水反应:
(4)Na2O2和CO2反应:
(5)Na在空气中燃烧:
(6)HClO见光分解:
II.写出下列反应的离子方程式:
(7)Cl2和水反应:
(8)Na和水反应:
(9)NaOH溶液和NaHCO3溶液反应:
(10)NaHCO3与少量石灰水:
(11)NaHCO3与过量石灰水:
更新时间:2024-01-06 16:35:27
|
相似题推荐
填空题
|
较易
(0.85)
名校
解题方法
【推荐1】I.写出下列典型物质的电离方程式
(1)H2SO4_________________________________________
(2)Fe(OH)3________________________________________
(3)NaHSO4_________________________________________
(4)NaHCO3________________________________________
(5)Al2O3(熔融)____________________________________
II.写出下列典型反应的离子方程式:
(1)在稀H2SO4中加入CH3COONa溶液___________________________________
(2)氧化镁溶于稀硫酸______________________________________________
(3)CuSO4溶液与Ba(OH)2溶液混合_______________________________________
(4)NaHCO3溶液与稀盐酸混合________________________________________
(5)NaHSO4溶液与NaOH溶液混合_____________________________________
(1)H2SO4
(2)Fe(OH)3
(3)NaHSO4
(4)NaHCO3
(5)Al2O3(熔融)
II.写出下列典型反应的离子方程式:
(1)在稀H2SO4中加入CH3COONa溶液
(2)氧化镁溶于稀硫酸
(3)CuSO4溶液与Ba(OH)2溶液混合
(4)NaHCO3溶液与稀盐酸混合
(5)NaHSO4溶液与NaOH溶液混合
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐2】(1)写出Ba(OH)2溶液和K2CO3溶液反应的离子方程式:_______ 。
(2)写出NaOH溶液和CH3COOH溶液反应的离子方程式:________________ 。
(3)向NaOH溶液中通入足量CO2,发生反应的离子方程式:__________________ 。
(2)写出NaOH溶液和CH3COOH溶液反应的离子方程式:
(3)向NaOH溶液中通入足量CO2,发生反应的离子方程式:
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐3】NaCl是一种重要的化工原料,可以制备多种物质,请根据下图信息回答问题

(1)框图中的几种单质,常温常压下可以导电的是___________ 。(写化学式)
(2)请把框图中含氯的电解质按照氯元素化合价由低到高的顺序写出来(写化学式):___________ 。
(3)写出反应①的离子方程式:___________ ,该反应中氧化产物与还原产物的质量比为:___________ 。
(4)若NaHCO3溶液中混有少量Na2CO3杂质,最好的除杂方法用离子方程式表示为___________ 。
(5)题目框图中反应④只给出了部分产物,且该反应只有一种元素的化合价发生变化,请完成反应④的化学方程式,___________ 。

(1)框图中的几种单质,常温常压下可以导电的是
(2)请把框图中含氯的电解质按照氯元素化合价由低到高的顺序写出来(写化学式):
(3)写出反应①的离子方程式:
(4)若NaHCO3溶液中混有少量Na2CO3杂质,最好的除杂方法用离子方程式表示为
(5)题目框图中反应④只给出了部分产物,且该反应只有一种元素的化合价发生变化,请完成反应④的化学方程式,
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐1】自来水的消毒关系到每个人的饮水安全问题。很早以前自来水厂常用氯气作自来水的消毒剂,后来发现用氯气有不妥之处,就改用了ClO2或者Na2FeO4作消毒剂。
(1)请写出氯原子的结构示意图:___________ ;氯离子的电子式:___________ 。
(2)氯气曾被选作消毒剂是因为溶于水时能生成一种可以杀菌消毒的化学物质,请写出氯气溶于水生成该物质的化学反应方程式:___________ 。
(3)84 消毒液(主要成分是NaClO和NaCl)和洁厕灵(主要成分是盐酸)混用会产生有毒气体,试写出反应的离子方程式:___________ 。
(1)请写出氯原子的结构示意图:
(2)氯气曾被选作消毒剂是因为溶于水时能生成一种可以杀菌消毒的化学物质,请写出氯气溶于水生成该物质的化学反应方程式:
(3)84 消毒液(主要成分是NaClO和NaCl)和洁厕灵(主要成分是盐酸)混用会产生有毒气体,试写出反应的离子方程式:
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐2】含氯化合物具有广泛的应用,回答下列问题。
(1)1mol 含有的中子数为
含有的中子数为_______  。
。
(2)将氯气持续通入紫色石蕊试液中,溶液颜色如图变化:

溶液中导致变色的微粒Ⅰ是_______ (填微粒符号,下同),Ⅱ是_______ ,Ⅲ是_______ 。
(3) 是高效、广谱、绿色的消毒剂。下列能判断Cl、O两种元素非金属性强弱的是
是高效、广谱、绿色的消毒剂。下列能判断Cl、O两种元素非金属性强弱的是_______ (填字母)。
a.原子得电子能力 b.与金属钠反应得电子的数目
c.最简单气态氢化物的稳定性 d.单质的沸点
(4)由Cu、C、 溶液组成的原电池如图所示:
溶液组成的原电池如图所示:

该电池中负极为_______ (填化学式),电子移动方向为_______ (填“Cu→C”或“C→Cu”),正极上发生的电极反应式为_______ 。
(1)1mol
 含有的中子数为
含有的中子数为 。
。(2)将氯气持续通入紫色石蕊试液中,溶液颜色如图变化:

溶液中导致变色的微粒Ⅰ是
(3)
 是高效、广谱、绿色的消毒剂。下列能判断Cl、O两种元素非金属性强弱的是
是高效、广谱、绿色的消毒剂。下列能判断Cl、O两种元素非金属性强弱的是a.原子得电子能力 b.与金属钠反应得电子的数目
c.最简单气态氢化物的稳定性 d.单质的沸点
(4)由Cu、C、
 溶液组成的原电池如图所示:
溶液组成的原电池如图所示:
该电池中负极为
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐3】写出相应的化学方程式:
(1)湿润的氯气具有漂白性的原因:____________________ 。
(2)漂白粉显现“漂白”效力的反应:____________________ 。
(3)金属钠与水的反应:____________________ 。
(4)(CN)2是一种无色带苦杏仁味的剧毒气体,其化学性质与氯气非常相似。试写出(CN)2与NaOH溶液的反应的化学方程式:____________________ 。
(5)过氧化钠与二氧化碳的反应:____________________ 。
(1)湿润的氯气具有漂白性的原因:
(2)漂白粉显现“漂白”效力的反应:
(3)金属钠与水的反应:
(4)(CN)2是一种无色带苦杏仁味的剧毒气体,其化学性质与氯气非常相似。试写出(CN)2与NaOH溶液的反应的化学方程式:
(5)过氧化钠与二氧化碳的反应:
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐1】金属及其化合物在工业生产和生活中有重要用途,根据所学知识回答下列问题。
(1)将绿豆大的钠投入到水和煤油的混合体系中,观察到的现象是___________ 。
(2)CO和H2的混合气体10.0g,与足量的O2反应后,通过足量Na2O2,写出通过Na2O2时发生的化学方程式___________ 、___________ ,固体Na2O2质量增加___________ g。
(3)有一杯澄清溶液,可能含有的离子有Ca2+、Cu2+、Mg2+、K+、CO ,检验该溶液中阳离子的操作方法是
,检验该溶液中阳离子的操作方法是___________ 。
(1)将绿豆大的钠投入到水和煤油的混合体系中,观察到的现象是
(2)CO和H2的混合气体10.0g,与足量的O2反应后,通过足量Na2O2,写出通过Na2O2时发生的化学方程式
(3)有一杯澄清溶液,可能含有的离子有Ca2+、Cu2+、Mg2+、K+、CO
 ,检验该溶液中阳离子的操作方法是
,检验该溶液中阳离子的操作方法是
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐2】钠、铝和铁是三种重要的金属.请回答:
Ⅰ、(1)钠原子的结构示意图是_____ ;铝原子的结构示意图是______ .
(2)将一小块金属钠长期露置于空气中发生一系列变化,最终产物是______ .
(3)取一小块金属钠放在滴有酚酞的水中,实验现象正确的是(填选项)_____ .
①钠浮在水面迅速反应 ②钠沉在水底迅速反应 ③钠熔成小球并快速游动 ④反应中可以听到嘶嘶的响声 ⑤反应后的溶液变为红色
Ⅱ、(1)写出这三种金属中能与氢氧化钠溶液反应的离子方程式___________________
(2)铁、铝是常用的金属材料,在空气中铝比铁更耐腐蚀.对此合理的解释是______ .
Ⅰ、(1)钠原子的结构示意图是
(2)将一小块金属钠长期露置于空气中发生一系列变化,最终产物是
(3)取一小块金属钠放在滴有酚酞的水中,实验现象正确的是(填选项)
①钠浮在水面迅速反应 ②钠沉在水底迅速反应 ③钠熔成小球并快速游动 ④反应中可以听到嘶嘶的响声 ⑤反应后的溶液变为红色
Ⅱ、(1)写出这三种金属中能与氢氧化钠溶液反应的离子方程式
(2)铁、铝是常用的金属材料,在空气中铝比铁更耐腐蚀.对此合理的解释是
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐1】根据所学知识回答下列问题:
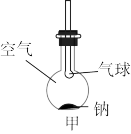
(1)将一小块新切的金属钠迅速放入平底烧瓶底部,按图甲所示塞紧瓶塞。过一段时间后可观察到的现象有_______ ,发生反应的化学方程式为_______
(2)按图乙所示的装置,进行钠与水反应的实验,实验开始时,振动细铁丝使钠块掉入滴有酚酞的水溶液中,可观察到钠与水反应的现象,不同的现象反映钠的不同性质。

①能证明钠的密度比水的小的现象是_______
②能证明钠的熔点低的现象是_______
③能证明有氢氧化钠生成的现象是_______
(3)向Na2O2中滴加浓盐酸,试管壁发热,有刺激性气味的气体产生,反应后所得溶液呈浅黄绿色。推测产生该气体的反应的化学方程式,并用单线桥法标出电子转移的方向和数目:_______ ,该反应中被还原的元素是_______ (填元素符号),氧化产物是_______ (填化学式)。
(1)将一小块新切的金属钠迅速放入平底烧瓶底部,按图甲所示塞紧瓶塞。过一段时间后可观察到的现象有

(2)按图乙所示的装置,进行钠与水反应的实验,实验开始时,振动细铁丝使钠块掉入滴有酚酞的水溶液中,可观察到钠与水反应的现象,不同的现象反映钠的不同性质。

①能证明钠的密度比水的小的现象是
②能证明钠的熔点低的现象是
③能证明有氢氧化钠生成的现象是
(3)向Na2O2中滴加浓盐酸,试管壁发热,有刺激性气味的气体产生,反应后所得溶液呈浅黄绿色。推测产生该气体的反应的化学方程式,并用单线桥法标出电子转移的方向和数目:
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐2】完成下列问题
(1)过氧化钠___ 色固体,与CO2反应,方程式___ 。因此,过氧化钠可作为呼吸面具和潜水艇的氧气来源。
(2)计算机芯片的主要成分____
(3)将钠投入水中后,钠融化成一个小球,根据这一现象你能得出的结论是①____ ,②____ 。钠与水反应的离子方程式是____
(4)用一只长滴管,深入液面下,向盛有FeCl2溶液的试管中滴加NaOH溶液,可观察到有白色沉淀生成。生成白色沉淀的离子方程式____ ,在空气中放置的现象是____
(1)过氧化钠
(2)计算机芯片的主要成分
(3)将钠投入水中后,钠融化成一个小球,根据这一现象你能得出的结论是①
(4)用一只长滴管,深入液面下,向盛有FeCl2溶液的试管中滴加NaOH溶液,可观察到有白色沉淀生成。生成白色沉淀的离子方程式
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐3】某研究性学习小组在探究淡黄色过氧化钠与水反应是放出热量还是吸收热量时设计了如图所示的实验装置。

在小试管里加入1g淡黄色过氧化钠,把小试管套在带支管的试管内。在U形管内加入少量红墨水。打开T形管螺旋夹,使U形管内两边的液面处于同一水平面。再夹紧螺旋夹,把水滴入小试管内,可观察到U形管右侧的液面立即下降,左侧的液面上升。
(1)过氧化钠的电子式__ 。
(2)写出上述反应的化学方程式__ 。
(3)下列各图中,表示过氧化钠与水反应的图是( )
A. B.
B.
C. D.
D.

在小试管里加入1g淡黄色过氧化钠,把小试管套在带支管的试管内。在U形管内加入少量红墨水。打开T形管螺旋夹,使U形管内两边的液面处于同一水平面。再夹紧螺旋夹,把水滴入小试管内,可观察到U形管右侧的液面立即下降,左侧的液面上升。
(1)过氧化钠的电子式
(2)写出上述反应的化学方程式
(3)下列各图中,表示过氧化钠与水反应的图是
A.
 B.
B.
C.
 D.
D.
您最近一年使用:0次



