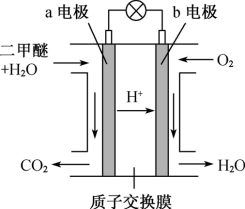
氢氧燃料电池(构造示意图如图)单位质量输出电能较高,可以用于载人航天工程,反应生成的水可作为航天员的饮用水,氧气可以作为备用氧源供给航天员呼吸。
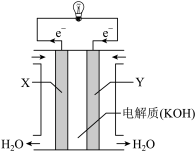
(1)判断Y极为电池的_______ 极,发生_______ 反应。
(2)X电极的电极反应式为_______ 。
(3)若电解质更换为以稀硫酸为电解质,则X电极的电极反应式为_______ 。
(4)Y电极的电极反应式为_______ 。

(1)判断Y极为电池的
(2)X电极的电极反应式为
(3)若电解质更换为以稀硫酸为电解质,则X电极的电极反应式为
(4)Y电极的电极反应式为
更新时间:2024-01-11 09:24:41
|
相似题推荐
填空题
|
适中
(0.65)
解题方法
【推荐1】被誉为改变未来世界的十大新科技之一的燃料电池具有无污染、无噪音、高效率的特点。如图为氢氧燃料电池的结构示意图,回答下列问题:
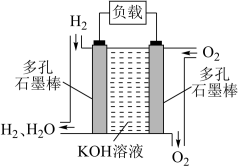
(1)O2进入的电极为___________ 极。
(2)电池工作时溶液的OH-向___________ (填“正极”或“负极”)移动,通___________ (填“H2”或“O2”)的一极电势较低。
(3)写出电池工作时的负极反应式:___________ 。
(4)若电池工作时转移0.1 mol电子,理论上消耗标准状况下___________ mLO2。
(5)若将此燃料电池改为以CH4和O2为原料进行工作时,负极反应式为___________ 。

(1)O2进入的电极为
(2)电池工作时溶液的OH-向
(3)写出电池工作时的负极反应式:
(4)若电池工作时转移0.1 mol电子,理论上消耗标准状况下
(5)若将此燃料电池改为以CH4和O2为原料进行工作时,负极反应式为
您最近半年使用:0次
填空题
|
适中
(0.65)
【推荐2】能源是现代文明的原动力,电池与我们的生活和生产密切相关。
(1)事实证明,能设计成原电池的反应通常是放热反应,下列化学反应在理论上可以设计成原电池的是_______(填字母)。
(2)下图为原电池装置示意图:
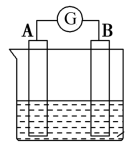
①若A为Zn片,B为石墨棒,电解质溶液为稀硫酸,写出正极的电极反应式:_______ ,反应过程中溶液的酸性_______ (填“增强”、“减弱”或“不变”)。一段时间后,当电池中放出1.68 L(标准状况)气体时,电路中有_______ 个电子通过了导线(用NA表示阿伏加德罗常数的值)。
②若A为镁片,B为铝片,电解质为NaOH溶液,则铝片为_______ (填“正极”或“负极”);写出该电极的电极反应式:_______ 。
③燃料电池是一种具有应用前景的绿色电源, 和
和 组合形成的燃料电池的结构如图(电解质溶液是稀硫酸,质子交换膜只允许
组合形成的燃料电池的结构如图(电解质溶液是稀硫酸,质子交换膜只允许 通过)。则电极d是
通过)。则电极d是_______ (填“正极”或“负极”),若线路中转移2 mol电子,则该燃料电池理论上消耗的 在标准状况下的体积为
在标准状况下的体积为_______ L。

④为证明铁的金属活动性比铜强,某同学设计了如下一些方案。其中能证明铁的金属活动性比铜强的方案是_______ (填序号)。
(1)事实证明,能设计成原电池的反应通常是放热反应,下列化学反应在理论上可以设计成原电池的是_______(填字母)。
A. | B. |
C. | D. |

①若A为Zn片,B为石墨棒,电解质溶液为稀硫酸,写出正极的电极反应式:
②若A为镁片,B为铝片,电解质为NaOH溶液,则铝片为
③燃料电池是一种具有应用前景的绿色电源,
 和
和 组合形成的燃料电池的结构如图(电解质溶液是稀硫酸,质子交换膜只允许
组合形成的燃料电池的结构如图(电解质溶液是稀硫酸,质子交换膜只允许 通过)。则电极d是
通过)。则电极d是 在标准状况下的体积为
在标准状况下的体积为
④为证明铁的金属活动性比铜强,某同学设计了如下一些方案。其中能证明铁的金属活动性比铜强的方案是
| 方案 | 现象或产物 |
A.将铁片置于 溶液中 溶液中 | 铁片上有亮红色物质析出 |
| B.将铁丝和铜丝分别在氯气燃烧 | 产物分别为 和 和 |
| C.将铁片和铜片分别置于稀硫酸溶液中 | 铁片上有气泡产生,铜片上无气泡产生 |
| D.将铁片和铜片置于盛有稀硫酸的烧杯中,并用导线连 | 铁片溶解,铜片上有气泡产生 |
您最近半年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】已知炼铁过程中发生
 ;回答下列问题:
;回答下列问题:
(1) 时,向容积为2L的恒容密闭容器中加入3mol
时,向容积为2L的恒容密闭容器中加入3mol  和3mol CO发生反应,5min时达到平衡,平衡时测得混合气体中
和3mol CO发生反应,5min时达到平衡,平衡时测得混合气体中 的体积分数为80%。
的体积分数为80%。
①0~5min内反应的平均速率
_______ 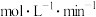 。
。
②该温度下反应的平衡常数为_______ 。
③下列选项中能够说明该反应已经达到平衡状态的是_______ (填字母)
a. 的物质的量不再变化 b.体系的压强保持不变
的物质的量不再变化 b.体系的压强保持不变
c.混合气体的平均摩尔质量保持不变 d.单位时间内消耗CO和生成 的物质的量相等
的物质的量相等
④若平衡后再向容器中加入1mol 、1mol CO、2mol Fe和1mol
、1mol CO、2mol Fe和1mol  ,判断此时
,判断此时 、
、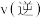 的大小关系为:
的大小关系为:
_______ 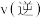 (填“>”、“=”或“<”)。
(填“>”、“=”或“<”)。
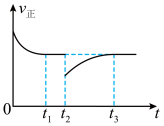
(2)一定条件下,正向反应速率与时间的关系如图所示, 时刻改变了一个外界条件,可能是
时刻改变了一个外界条件,可能是_______ 。
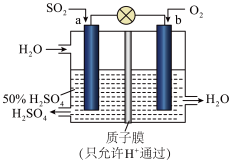
(3)科研人员设想用如图原电池装置生产硫酸(设通入的气体完全参与反应)。导线中电子移动方向为_______ (用字母a,b填写)负极发生的电极反应为_______ 。

 ;回答下列问题:
;回答下列问题:(1)
 时,向容积为2L的恒容密闭容器中加入3mol
时,向容积为2L的恒容密闭容器中加入3mol  和3mol CO发生反应,5min时达到平衡,平衡时测得混合气体中
和3mol CO发生反应,5min时达到平衡,平衡时测得混合气体中 的体积分数为80%。
的体积分数为80%。①0~5min内反应的平均速率

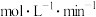 。
。②该温度下反应的平衡常数为
③下列选项中能够说明该反应已经达到平衡状态的是
a.
 的物质的量不再变化 b.体系的压强保持不变
的物质的量不再变化 b.体系的压强保持不变c.混合气体的平均摩尔质量保持不变 d.单位时间内消耗CO和生成
 的物质的量相等
的物质的量相等④若平衡后再向容器中加入1mol
 、1mol CO、2mol Fe和1mol
、1mol CO、2mol Fe和1mol  ,判断此时
,判断此时 、
、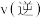 的大小关系为:
的大小关系为:
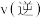 (填“>”、“=”或“<”)。
(填“>”、“=”或“<”)。(2)一定条件下,正向反应速率与时间的关系如图所示,
 时刻改变了一个外界条件,可能是
时刻改变了一个外界条件,可能是
(3)科研人员设想用如图原电池装置生产硫酸(设通入的气体完全参与反应)。导线中电子移动方向为

您最近半年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】如图是氢氧燃料电池示意图,请根据示意图判断正负极________ ,并试写出在不同电解质中的电极反应。


| 介质 | 电池反应:2H2+O2=2H2O |
| 酸性(H+) | 负极 |
| 正极 | |
| 中性(Na2SO4) | 负极 |
| 正极 | |
| 碱性(OH-) | 负极 |
| 正极 |
您最近半年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】完成下列问题。
(1)氢氧燃料电池是一种高效无污染的清洁电池它分碱性(用KOH做电解质)和酸性(用硫酸做电解质)燃料电池。如果是酸性燃料电池,则正极反应方程式是_______ 。
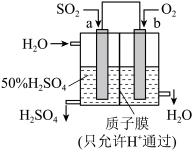
(2)科研人员设想用如图原电池装置生产硫酸,则负极的电极反应式为_______ 。
(3)某甲烷—氧气燃料电池的工作原理如下图所示。
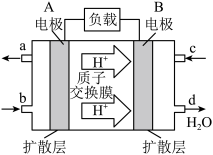
①A极发生的电极反应式为_______ 。
②工作一段时间后,当3.2g甲烷完全反应生成CO2时,有_______ molH+通过质子交换膜。
(4)已知:H2O2是一种强氧化剂。MgH2O2电池可用于驱动无人驾驶的潜航器。该电池以海水为电解质溶液,示意图如图所示。

该电池工作时,H2O2在石墨电极上发生反应的电极反应式是_______ 。
(1)氢氧燃料电池是一种高效无污染的清洁电池它分碱性(用KOH做电解质)和酸性(用硫酸做电解质)燃料电池。如果是酸性燃料电池,则正极反应方程式是
(2)科研人员设想用如图原电池装置生产硫酸,则负极的电极反应式为

(3)某甲烷—氧气燃料电池的工作原理如下图所示。

①A极发生的电极反应式为
②工作一段时间后,当3.2g甲烷完全反应生成CO2时,有
(4)已知:H2O2是一种强氧化剂。MgH2O2电池可用于驱动无人驾驶的潜航器。该电池以海水为电解质溶液,示意图如图所示。

该电池工作时,H2O2在石墨电极上发生反应的电极反应式是
您最近半年使用:0次