被誉为改变未来世界的十大新科技之一的燃料电池具有无污染、无噪音、高效率的特点。如图为氢氧燃料电池的结构示意图,回答下列问题:
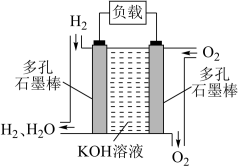
(1)O2进入的电极为___________ 极。
(2)电池工作时溶液的OH-向___________ (填“正极”或“负极”)移动,通___________ (填“H2”或“O2”)的一极电势较低。
(3)写出电池工作时的负极反应式:___________ 。
(4)若电池工作时转移0.1 mol电子,理论上消耗标准状况下___________ mLO2。
(5)若将此燃料电池改为以CH4和O2为原料进行工作时,负极反应式为___________ 。

(1)O2进入的电极为
(2)电池工作时溶液的OH-向
(3)写出电池工作时的负极反应式:
(4)若电池工作时转移0.1 mol电子,理论上消耗标准状况下
(5)若将此燃料电池改为以CH4和O2为原料进行工作时,负极反应式为
更新时间:2021-01-09 04:56:31
|
相似题推荐
填空题
|
适中
(0.65)
名校
【推荐1】化学电池在通讯、交通及日常生活中有着广泛的应用。
(1)碱性锌锰干电池(如图所示)是应用最普遍的电池之一,电池总反应为 ,碱性锌锰干电池的负极材料是
,碱性锌锰干电池的负极材料是______ (填名称),负极上发生的电极反应为______ 。若反应消耗13g负极材料,则电池中转移电子的物质的量______ mol。 。下列说法正确的是______(填标号)。
。下列说法正确的是______(填标号)。
(3)镁铝电池的构造如图所示,当电解质溶液为 溶液时,可知电池的负极材料为
溶液时,可知电池的负极材料为______ (填“Mg”或“Al”)反应式为______ 。
(1)碱性锌锰干电池(如图所示)是应用最普遍的电池之一,电池总反应为
 ,碱性锌锰干电池的负极材料是
,碱性锌锰干电池的负极材料是
 。下列说法正确的是______(填标号)。
。下列说法正确的是______(填标号)。A.电解液中 的浓度始终保持不变 的浓度始终保持不变 |
B.放电时正极上的电极反应式为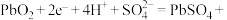 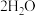 |
C.放电时,当外电路通过 电子时,理论上负极质量增加 电子时,理论上负极质量增加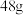 |
D.放电时,溶液中的 向正极移动 向正极移动 |
(3)镁铝电池的构造如图所示,当电解质溶液为
 溶液时,可知电池的负极材料为
溶液时,可知电池的负极材料为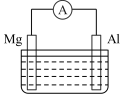
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
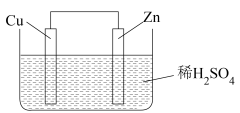
【推荐2】Zn—Cu原电池的装置如图所示,试回答下列问题:___________ 极,发生___________ 反应,溶液中H+向___________ (填“Zn”或“Cu”)电极方向移动。
(2)正极的现象是___________ ,负极的电极反应式为___________ 。
(3)若反应过程中有0.4 mol电子发生转移,则生成的氢气在标准状况下的体积为___________ L。
(2)正极的现象是
(3)若反应过程中有0.4 mol电子发生转移,则生成的氢气在标准状况下的体积为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】电化学知识在生活中应用广泛,但形成原电池和电解池均需要一定的条件。
(1)现有下列装置:

其中,能构成原电池的是______ (填字母代号),能构成电解池的是______ (填字母代号)。
(2)下列化学方程式正确且能设计成原电池的有______(填字母代号)。
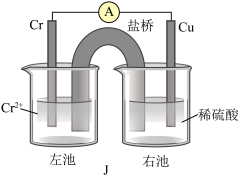
(3)已知Cr比Fe的金属性稍活泼,铜铬构成原电池如装置J所示(盐桥中装的是饱和KCl琼脂溶液)。
则Cr为______ 极(填“正”或“负”),盐桥中 移向
移向______ (填“左池”或“右池”),盛稀硫酸烧杯中的现象为______ 。
(4)甲、乙两同学利用原电池反应检测金属的活动性顺序,设计如下实验装置。
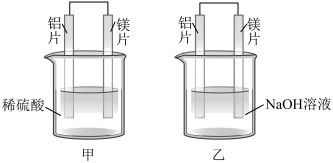
甲装置用______ (填“铝片”或“镁片”)作负极,两同学实验现象的不同之处为______ ,由此得出不能简单根据金属的活动性来判断原电池的正负极的结论,正确的判断方法是______ 。
(1)现有下列装置:

其中,能构成原电池的是
(2)下列化学方程式正确且能设计成原电池的有______(填字母代号)。
A. |
B.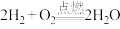 |
C.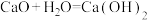 |
D. |
则Cr为
 移向
移向
(4)甲、乙两同学利用原电池反应检测金属的活动性顺序,设计如下实验装置。

甲装置用
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】燃料电池是利用燃料(如 、CO、
、CO、 、
、 、
、 等)与
等)与 反应从而将化学能转化为电能的装置。
反应从而将化学能转化为电能的装置。
(1)甲烷燃料电池(NaOH溶液作电解质溶液)的负极反应式为___________ ,正极反应式为___________ ,放电过程中溶液的pH___________ (填“增大”“减小”或“不变”)。
(2)瑞典ASES公司设计的曾用于驱动潜艇的液氨-液氧燃料电池示意图如下,下列有关说法正确的是___________ 。
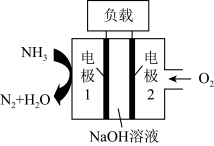
a.电池工作时, 向负极移动
向负极移动
b.电子由电极2经外电路流向电极1
c.电池总反应为
d.电极2发生的电极反应为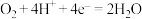
(3)铅酸蓄电池是常用的化学电源,其电极材料分别是Pb和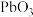 ,电解质溶液为稀硫酸,该电池工作时发生的总反应为
,电解质溶液为稀硫酸,该电池工作时发生的总反应为 。试回答下列问题。
。试回答下列问题。
①铅酸蓄电池的负极材料是___________ ,正极反应为___________ 。
②若有1mol电子从某电极流出,则参加反应的 是
是___________ mol,负极的质量变化是___________ (填“增大”或“减小”)___________ g。
 、CO、
、CO、 、
、 、
、 等)与
等)与 反应从而将化学能转化为电能的装置。
反应从而将化学能转化为电能的装置。(1)甲烷燃料电池(NaOH溶液作电解质溶液)的负极反应式为
(2)瑞典ASES公司设计的曾用于驱动潜艇的液氨-液氧燃料电池示意图如下,下列有关说法正确的是

a.电池工作时,
 向负极移动
向负极移动b.电子由电极2经外电路流向电极1
c.电池总反应为

d.电极2发生的电极反应为
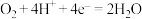
(3)铅酸蓄电池是常用的化学电源,其电极材料分别是Pb和
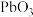 ,电解质溶液为稀硫酸,该电池工作时发生的总反应为
,电解质溶液为稀硫酸,该电池工作时发生的总反应为 。试回答下列问题。
。试回答下列问题。①铅酸蓄电池的负极材料是
②若有1mol电子从某电极流出,则参加反应的
 是
是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
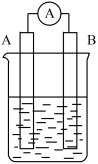
【推荐3】原电池装置如图所示,回答下列问题。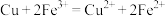 设计原电池,电极A为石墨、则电极B为电池的
设计原电池,电极A为石墨、则电极B为电池的________ 极,发生的电极反应式为:________________ ,电极A上发生的电极反应为________ (填“氧化”或“还原”)反应。
(2)若A、B均为铂片,分别从A、B两极通入 和
和 。当烧杯内的液体为稀硫酸溶液,A为
。当烧杯内的液体为稀硫酸溶液,A为________ (填正极或负极)写出B电极的电极反应式:________________ ,溶液中的 向
向________ (填“A”或“B”)极移动;当烧杯内的液体为氢氧化钾溶液,此时A电极的电极反应式:________ ,当消耗0.2mo1氧气时,电路中通过电子数为________ 。
(3)若A为 ,B为
,B为 ,烧杯内的液体为浓硫酸,电池反应为:
,烧杯内的液体为浓硫酸,电池反应为: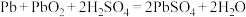 。写出B电极的电极反应式:
。写出B电极的电极反应式:________________ 。
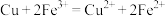 设计原电池,电极A为石墨、则电极B为电池的
设计原电池,电极A为石墨、则电极B为电池的(2)若A、B均为铂片,分别从A、B两极通入
 和
和 。当烧杯内的液体为稀硫酸溶液,A为
。当烧杯内的液体为稀硫酸溶液,A为 向
向(3)若A为
 ,B为
,B为 ,烧杯内的液体为浓硫酸,电池反应为:
,烧杯内的液体为浓硫酸,电池反应为: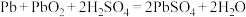 。写出B电极的电极反应式:
。写出B电极的电极反应式:
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】(1)Cu、Fe作两极,稀硫酸作电解质溶液的原电池中:
①Cu作______ 极,
②Fe作_______ 极。
③电极反应式是:负极:___________ ;正极_________________
④总反应式是_________________ 。
(2)技术上使用的氢氧燃料电池具有高能、轻便、无污染的优点。氢氧燃料电池有酸式和碱式两种,它们放电时的总反应都可以表示为2H2+O2=2H2O。酸式电池中电解质是酸,其负极反应可表示为2H2-4e-=4H+,则其正极反应式为___________________ 。碱式电池的电解质是碱,其正极反应式为O2+2H2O+4e- =4OH-,则其负极反应可表示为___________________ 。
(3)氢气是燃料电池最简单的燃料,虽然使用方便,却受到价格和来源的限制。常用的燃料往往是某些碳氢化合物,如:甲烷、汽油等。请写出将图中氢气换成甲烷时所构成的甲烷燃料电池中a极的电极反应式:_______________ ,此时电池内总的反应式:_________

①Cu作
②Fe作
③电极反应式是:负极:
④总反应式是
(2)技术上使用的氢氧燃料电池具有高能、轻便、无污染的优点。氢氧燃料电池有酸式和碱式两种,它们放电时的总反应都可以表示为2H2+O2=2H2O。酸式电池中电解质是酸,其负极反应可表示为2H2-4e-=4H+,则其正极反应式为
(3)氢气是燃料电池最简单的燃料,虽然使用方便,却受到价格和来源的限制。常用的燃料往往是某些碳氢化合物,如:甲烷、汽油等。请写出将图中氢气换成甲烷时所构成的甲烷燃料电池中a极的电极反应式:

您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】电池研发与生产、生活和军事等领域的发展密切相关。电池研发人员的工作包括电池构成材料的研制、电池性能的改进和应用拓展等。如图为简易原电池装置示意图。

(1)将锌片和铜片用导线相连,烧杯中盛放的是硫酸铜溶液,电流表指针发生偏转,在这个原电池中,负极材料是___________ ,正极发生的实验现象是:___________ ;写出总反应的离子方程式:___________ ;
(2)将铝片和镁片用导线相连,烧杯中盛放的是氢氧化钠溶液,电流表指针发生偏转,在这个原电池中,负极材料是___________ ,负极反应的离子方程式:___________ ;
(3)若A、B均为铂片,电解质为KOH溶液,分别从A、B两极通入H2和O2,该电池即为碱性氢氧燃料电池,写出A电极反应式:___________ ;该电池在工作一段时间后,溶液的pH将___________ (填“增大”“减小”或“不变”)。

(1)将锌片和铜片用导线相连,烧杯中盛放的是硫酸铜溶液,电流表指针发生偏转,在这个原电池中,负极材料是
(2)将铝片和镁片用导线相连,烧杯中盛放的是氢氧化钠溶液,电流表指针发生偏转,在这个原电池中,负极材料是
(3)若A、B均为铂片,电解质为KOH溶液,分别从A、B两极通入H2和O2,该电池即为碱性氢氧燃料电池,写出A电极反应式:
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】任何化学反应都伴随着能量的变化,通过化学反应,化学能可转化为热能、电能等不同形式的能量。
(1)H2可用于工业合成氨气,已知拆开1molH—H、1molN≡N分别需要吸收的能量为436kJ、946kJ,形成1molN-H会放出能量391kJ,则在反应N2+3H2 2NH3中,每生成2molNH3
2NH3中,每生成2molNH3_______ (填“吸收”或“放出”)热量_______ kJ。
(2)Mg、Al设计成如图所示原电池装置:_______ 极,正极电极反应式为_______ 。
②若溶液为氢氧化钠溶液,负极的电极反应为_______ 。
(3)电化学法处理SO2是目前研究的热点。利用过氧化氢吸收SO2可消除SO2污染,设计装置如图所示。_______ (填“正极”或“负极”);
②正极的电极反应式为_______ 。
③若11.2L(标准状况)SO2参与反应,则迁移H+的物质的量为_______ 。
(1)H2可用于工业合成氨气,已知拆开1molH—H、1molN≡N分别需要吸收的能量为436kJ、946kJ,形成1molN-H会放出能量391kJ,则在反应N2+3H2
 2NH3中,每生成2molNH3
2NH3中,每生成2molNH3(2)Mg、Al设计成如图所示原电池装置:
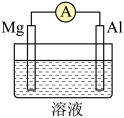
②若溶液为氢氧化钠溶液,负极的电极反应为
(3)电化学法处理SO2是目前研究的热点。利用过氧化氢吸收SO2可消除SO2污染,设计装置如图所示。
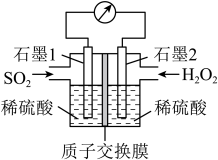
②正极的电极反应式为
③若11.2L(标准状况)SO2参与反应,则迁移H+的物质的量为
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】微生物燃料电池是一种利用微生物将化学能直接转化成电能的装置。已知某种甲醇微生物燃料电池中,电解质溶液呈酸性,示意图如图:
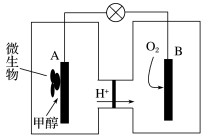
(1)该电池中外电路电子的流动方向为_____ (填“从A到B”或“从B到A”)。
(2)B电极附近氧气发生的电极反应为_____ 。

(1)该电池中外电路电子的流动方向为
(2)B电极附近氧气发生的电极反应为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】电动汽车、燃料电池汽车等逐步进入人们的生活,其中钴酸锂、锰酸锂、磷酸铁锂电池是目前主流的锂离子电池。
(1)①写出基态 原子的价层电子表示式
原子的价层电子表示式___________ 。 与
与 离子中未成对的电子数之比为
离子中未成对的电子数之比为___________ 。
②比较第四电离能大小
___________ 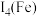 (填“>”“<”或“=”)。(原子序数
(填“>”“<”或“=”)。(原子序数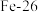
 )
)
(2)某公司研发的甲醇汽车,是利用甲醇 ——空气燃料电池,其工作原理如图:
——空气燃料电池,其工作原理如图:
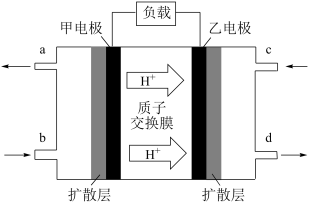
①图中甲电极为___________ (填“负极”、“正极”),乙电极的电极反应式为:___________ 。
②标准状况下,通入 甲醇(
甲醇( 其中C的化合价为
其中C的化合价为 )蒸汽,测得电路中转移
)蒸汽,测得电路中转移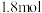 电子,则甲醇的利用率为
电子,则甲醇的利用率为___________ 。
(1)①写出基态
 原子的价层电子表示式
原子的价层电子表示式 与
与 离子中未成对的电子数之比为
离子中未成对的电子数之比为②比较第四电离能大小

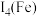 (填“>”“<”或“=”)。(原子序数
(填“>”“<”或“=”)。(原子序数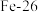
 )
)(2)某公司研发的甲醇汽车,是利用甲醇
 ——空气燃料电池,其工作原理如图:
——空气燃料电池,其工作原理如图:
①图中甲电极为
②标准状况下,通入
 甲醇(
甲醇( 其中C的化合价为
其中C的化合价为 )蒸汽,测得电路中转移
)蒸汽,测得电路中转移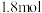 电子,则甲醇的利用率为
电子,则甲醇的利用率为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】电池在我们的生活中有着重要的应用,请回答下列问题:
(1)为了验证Fe2+与Cu2+氧化性强弱,下列装置能达到实验目的的是____ (填序号),写出正极的电极反应式____ 。若构建原电池时两个电极的质量相等,当导线中通过0.05mol电子时,两个电极的质量差为____ 。
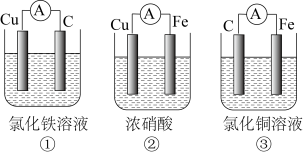
(2)将CH4设计成燃料电池,其利用率更高,装置如图所示(A、B为多孔碳棒)。
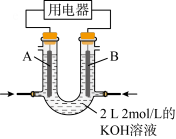
实验测得OH-向B电极定向移动,则___ (填“A”或“B”)处电极入口通甲烷,该电池正极的电极反应式为___ 当消耗甲烷的体积为33.6L(标准状况下)时,正极消耗氧气的物质的量为___ 。
(1)为了验证Fe2+与Cu2+氧化性强弱,下列装置能达到实验目的的是
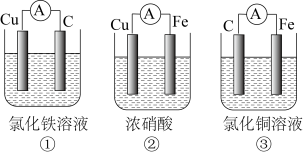
(2)将CH4设计成燃料电池,其利用率更高,装置如图所示(A、B为多孔碳棒)。

实验测得OH-向B电极定向移动,则
您最近一年使用:0次



