按要求完成下列填空:
(1) 溶液分别恰好使相同体积的硫酸铁、硫酸铜两种溶液中的
溶液分别恰好使相同体积的硫酸铁、硫酸铜两种溶液中的 完全转化成沉淀,则硫酸铁、硫酸铜两种溶液的物质的量浓度之比是
完全转化成沉淀,则硫酸铁、硫酸铜两种溶液的物质的量浓度之比是___________ 。
(2)某物质 加热时按化学方程式
加热时按化学方程式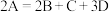 分解,产物均为气体,测得相同条件下由生成物组成的混合物气体对
分解,产物均为气体,测得相同条件下由生成物组成的混合物气体对 的相对密度为20,则反应物
的相对密度为20,则反应物 的相对分子质量为
的相对分子质量为___________ 。
(3)一定量的液态化合物 ,在一定量
,在一定量 中恰好完全反应:
中恰好完全反应: ,冷却后在标准状况下,测得生成物的体积为
,冷却后在标准状况下,测得生成物的体积为 (l表示液态,g表示气态)。
(l表示液态,g表示气态)。
①反应前 的体积是
的体积是___________  。
。
②在 分子中,
分子中, 两元素的质量比为
两元素的质量比为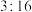 ,则
,则 两元素的相对原子质量之比为
两元素的相对原子质量之比为______ 。
(4)向 某物质的量浓度的
某物质的量浓度的 溶液中缓慢通入一定量的
溶液中缓慢通入一定量的 充分反应后,得到
充分反应后,得到 和
和 的混合溶液,向上述所得溶液中,逐滴滴加
的混合溶液,向上述所得溶液中,逐滴滴加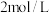 的盐酸,所得气体的体积与所加盐酸的体积关系如图所示:
的盐酸,所得气体的体积与所加盐酸的体积关系如图所示:
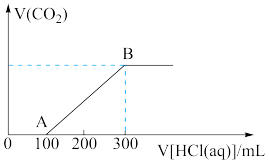
①OA段发生反应的化学方程式___________ 。
② 物质的量浓度为
物质的量浓度为___________ 。
③混合溶液中 和
和 的质量比是
的质量比是___________ 。
(1)
 溶液分别恰好使相同体积的硫酸铁、硫酸铜两种溶液中的
溶液分别恰好使相同体积的硫酸铁、硫酸铜两种溶液中的 完全转化成沉淀,则硫酸铁、硫酸铜两种溶液的物质的量浓度之比是
完全转化成沉淀,则硫酸铁、硫酸铜两种溶液的物质的量浓度之比是(2)某物质
 加热时按化学方程式
加热时按化学方程式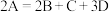 分解,产物均为气体,测得相同条件下由生成物组成的混合物气体对
分解,产物均为气体,测得相同条件下由生成物组成的混合物气体对 的相对密度为20,则反应物
的相对密度为20,则反应物 的相对分子质量为
的相对分子质量为(3)一定量的液态化合物
 ,在一定量
,在一定量 中恰好完全反应:
中恰好完全反应: ,冷却后在标准状况下,测得生成物的体积为
,冷却后在标准状况下,测得生成物的体积为 (l表示液态,g表示气态)。
(l表示液态,g表示气态)。①反应前
 的体积是
的体积是 。
。②在
 分子中,
分子中, 两元素的质量比为
两元素的质量比为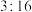 ,则
,则 两元素的相对原子质量之比为
两元素的相对原子质量之比为(4)向
 某物质的量浓度的
某物质的量浓度的 溶液中缓慢通入一定量的
溶液中缓慢通入一定量的 充分反应后,得到
充分反应后,得到 和
和 的混合溶液,向上述所得溶液中,逐滴滴加
的混合溶液,向上述所得溶液中,逐滴滴加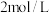 的盐酸,所得气体的体积与所加盐酸的体积关系如图所示:
的盐酸,所得气体的体积与所加盐酸的体积关系如图所示:
①OA段发生反应的化学方程式
②
 物质的量浓度为
物质的量浓度为③混合溶液中
 和
和 的质量比是
的质量比是
更新时间:2024-01-19 15:41:52
|
相似题推荐
填空题
|
适中
(0.65)
名校
【推荐1】回答下列问题
(1)某混合物由 组成,已知
组成,已知 三元素的质量之比为
三元素的质量之比为 ,则
,则 和
和 ,物质的量之比为
,物质的量之比为_______ ,含 的该混合物的质量为
的该混合物的质量为_______ 。
(2) 含
含 ,则
,则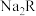 的摩尔质量为
的摩尔质量为_______ ,R的相对原子质量为_______ 。含R的质量为 的
的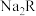 ,其物质的量为
,其物质的量为_______ 。
(1)某混合物由
 组成,已知
组成,已知 三元素的质量之比为
三元素的质量之比为 ,则
,则 和
和 ,物质的量之比为
,物质的量之比为 的该混合物的质量为
的该混合物的质量为(2)
 含
含 ,则
,则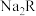 的摩尔质量为
的摩尔质量为 的
的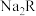 ,其物质的量为
,其物质的量为
您最近一年使用:0次
【推荐2】生活污水中氮是造成水体富营养化的主要原因。若某污水中NH4Cl含量为180mg/L。
(1)写出NH4Cl电子式:___ 。
(2)氮原子的电子排布式是:___ ,写出与氯同周期,有2个未成对电子的原子的元素符号为___ 、___ 。
(3)为除去废水中的NH4+,向103L该污水中加入0.1mol/LNaOH溶液,理论上需要NaOH溶液的体积为___ L(计算结果保留两位小数)。
(4)可先在酸性污水中加入铁屑将NO3-转化为NH4+后再除去,请配平下列离子方程式并标出电子转移的方向和数目___ 。
___ Fe+___ NO3-+___ H+→___ Fe2++___ NH4++___ H2O
(1)写出NH4Cl电子式:
(2)氮原子的电子排布式是:
(3)为除去废水中的NH4+,向103L该污水中加入0.1mol/LNaOH溶液,理论上需要NaOH溶液的体积为
(4)可先在酸性污水中加入铁屑将NO3-转化为NH4+后再除去,请配平下列离子方程式并标出电子转移的方向和数目
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】通过实验探究,能更好的体会化学知识如何服务我们的生产生活。
某化学小组根据质量守恒定律,对本地石灰石样品的成分含量进行研究,该样品主要成分是碳酸钙。研究过程中,该小组先取12.8g样品放入锥形瓶,再逐滴加入稀盐酸溶液,所得实验数据如图所示(假设其它成分均为杂质,不参与反应,也不溶于水)。

(1)首先该小组查阅资料,了解了质量守恒定律的内容,知道了如果根据反应前后物质的总质量来验证质量守恒定律,为保证实验成功,整个装置必须在_______ 环境中进行。
(2)该实验中,装置的气密性对测定结果_______ (填“有”或“无”)影响。
(3)实验完毕,将杂质过滤出来,洗涤、烘干,得到杂质_______ g。
(4)计算恰好反应时,瓶内剩余物质的质量_______ (写出计算过程)。
某化学小组根据质量守恒定律,对本地石灰石样品的成分含量进行研究,该样品主要成分是碳酸钙。研究过程中,该小组先取12.8g样品放入锥形瓶,再逐滴加入稀盐酸溶液,所得实验数据如图所示(假设其它成分均为杂质,不参与反应,也不溶于水)。

(1)首先该小组查阅资料,了解了质量守恒定律的内容,知道了如果根据反应前后物质的总质量来验证质量守恒定律,为保证实验成功,整个装置必须在
(2)该实验中,装置的气密性对测定结果
(3)实验完毕,将杂质过滤出来,洗涤、烘干,得到杂质
(4)计算恰好反应时,瓶内剩余物质的质量
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】取2.3克的钠投入500mL水中,完全反应后:
(1)生成的气体体积在标准状态下为_______ 升。
(2)形成的溶液的物质的量浓度为_______ 。
(1)生成的气体体积在标准状态下为
(2)形成的溶液的物质的量浓度为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】填空题
(1)当SO2、SO3的分子个数之比为1:1时,原子总数之比为_________ ,质量之比为________ 。
(2)中和含0. 2 mo lHCl的稀盐酸,需NaOH的质量为_____ g .
(3)将5 mo l/ L的Mg(NO3)2溶液a mL稀释至b mL,稀释后溶液中NO 的物质的量浓度是
的物质的量浓度是_________ mol·L-1.
(4)用等体积的0. 1mol·L-1的BaCl2溶液,可使相同体积的Fe2(SO4)3、Na2SO4、KAl(SO4)2三种溶液中的SO 完全沉淀,则三种硫酸盐的物质的量浓度之比为
完全沉淀,则三种硫酸盐的物质的量浓度之比为_____ 。
(1)当SO2、SO3的分子个数之比为1:1时,原子总数之比为
(2)中和含0. 2 mo lHCl的稀盐酸,需NaOH的质量为
(3)将5 mo l/ L的Mg(NO3)2溶液a mL稀释至b mL,稀释后溶液中NO
 的物质的量浓度是
的物质的量浓度是(4)用等体积的0. 1mol·L-1的BaCl2溶液,可使相同体积的Fe2(SO4)3、Na2SO4、KAl(SO4)2三种溶液中的SO
 完全沉淀,则三种硫酸盐的物质的量浓度之比为
完全沉淀,则三种硫酸盐的物质的量浓度之比为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】金属钠及其化合物在人类生产生活中起着重要作用。回答下列问题:
(1)将一定物质的量的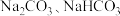 组成的混合物溶于水,配成
组成的混合物溶于水,配成 溶液。取出
溶液。取出 溶液,逐滴加入一定物质的量浓度的盐酸与它反应,变化如图,请回答下列问题。
溶液,逐滴加入一定物质的量浓度的盐酸与它反应,变化如图,请回答下列问题。

①原混合物中 的物质的量为
的物质的量为_____ 。
②盐酸的浓度为_____ 。
③盐酸加到 时,放出的
时,放出的 气体在标准状况下的体积为
气体在标准状况下的体积为_____ 。
(2)将 和
和 的混合物置于真空密闭容器中加热,充分反应后经检测气体产物为
的混合物置于真空密闭容器中加热,充分反应后经检测气体产物为 和水蒸气,其总质量为
和水蒸气,其总质量为 ,冷却至标准状况下的体积为
,冷却至标准状况下的体积为 。则剩余固体的成分为
。则剩余固体的成分为_____ ,原混合物中 的质量为
的质量为_____ 。
(3)为探究 的某些化学性质进行如下实验:向锥形瓶内加入饱和
的某些化学性质进行如下实验:向锥形瓶内加入饱和 溶液,用
溶液,用 传感器测定密闭装置中
传感器测定密闭装置中 分压(
分压( 的分压
的分压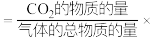 气体总压强),测得
气体总压强),测得 分压与温度的变化关系如图所示。温度在
分压与温度的变化关系如图所示。温度在 前,装置中
前,装置中 分压逐渐增大的主要原因是
分压逐渐增大的主要原因是_____ ;温度升高到 之后,装置中
之后,装置中 分压急剧增大的原因是
分压急剧增大的原因是_____ 。

(1)将一定物质的量的
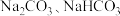 组成的混合物溶于水,配成
组成的混合物溶于水,配成 溶液。取出
溶液。取出 溶液,逐滴加入一定物质的量浓度的盐酸与它反应,变化如图,请回答下列问题。
溶液,逐滴加入一定物质的量浓度的盐酸与它反应,变化如图,请回答下列问题。
①原混合物中
 的物质的量为
的物质的量为②盐酸的浓度为
③盐酸加到
 时,放出的
时,放出的 气体在标准状况下的体积为
气体在标准状况下的体积为(2)将
 和
和 的混合物置于真空密闭容器中加热,充分反应后经检测气体产物为
的混合物置于真空密闭容器中加热,充分反应后经检测气体产物为 和水蒸气,其总质量为
和水蒸气,其总质量为 ,冷却至标准状况下的体积为
,冷却至标准状况下的体积为 。则剩余固体的成分为
。则剩余固体的成分为 的质量为
的质量为(3)为探究
 的某些化学性质进行如下实验:向锥形瓶内加入饱和
的某些化学性质进行如下实验:向锥形瓶内加入饱和 溶液,用
溶液,用 传感器测定密闭装置中
传感器测定密闭装置中 分压(
分压( 的分压
的分压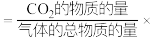 气体总压强),测得
气体总压强),测得 分压与温度的变化关系如图所示。温度在
分压与温度的变化关系如图所示。温度在 前,装置中
前,装置中 分压逐渐增大的主要原因是
分压逐渐增大的主要原因是 之后,装置中
之后,装置中 分压急剧增大的原因是
分压急剧增大的原因是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】向100 mL氢氧化钠溶液中通入一定量的二氧化碳气体充分反应后,再向所得溶液中逐滴加入0.2 mol/L的盐酸,产生二氧化碳的体积(标准状况下)与所加盐酸体积之间的关系如图所示:

据图回答下列问题:
(1)原NaOH溶液的浓度为____________ ;
(2)标准状况下,通入CO2体积是____________ ;
(3)所得溶液中溶质的成分和物质的量之比为_______________________ (溶质成分用化学式表示)。

据图回答下列问题:
(1)原NaOH溶液的浓度为
(2)标准状况下,通入CO2体积是
(3)所得溶液中溶质的成分和物质的量之比为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】Ⅰ.钠的化合物广泛应用于工业生产。
(1) 能与水剧烈反应,反应方程式为
能与水剧烈反应,反应方程式为 ,
, 与液氨也有类似的反应,写出反应的化学方程式
与液氨也有类似的反应,写出反应的化学方程式___________ 。
(2)在高温下氢化钠( )可将四氯化钛(
)可将四氯化钛( )还原成金属钛,写出该反应的化学方程式
)还原成金属钛,写出该反应的化学方程式___________ 。
(3)硼氢化钠( )与
)与 反应生成
反应生成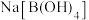 和
和 (已知反应过程中
(已知反应过程中 的化合价不变)。写出该反应的化学方程式
的化合价不变)。写出该反应的化学方程式___________ 。
(4)现有由两种含钠化合物组成的混合物,溶于水后,逐滴加入某浓度盐酸,所得 的粒子数目与所耗
的粒子数目与所耗 的粒子数目关系如图,两种含钠化合物的化学式和粒子数目之比为
的粒子数目关系如图,两种含钠化合物的化学式和粒子数目之比为___________ 、___________ 。

(1)
 能与水剧烈反应,反应方程式为
能与水剧烈反应,反应方程式为 ,
, 与液氨也有类似的反应,写出反应的化学方程式
与液氨也有类似的反应,写出反应的化学方程式(2)在高温下氢化钠(
 )可将四氯化钛(
)可将四氯化钛( )还原成金属钛,写出该反应的化学方程式
)还原成金属钛,写出该反应的化学方程式(3)硼氢化钠(
 )与
)与 反应生成
反应生成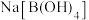 和
和 (已知反应过程中
(已知反应过程中 的化合价不变)。写出该反应的化学方程式
的化合价不变)。写出该反应的化学方程式(4)现有由两种含钠化合物组成的混合物,溶于水后,逐滴加入某浓度盐酸,所得
 的粒子数目与所耗
的粒子数目与所耗 的粒子数目关系如图,两种含钠化合物的化学式和粒子数目之比为
的粒子数目关系如图,两种含钠化合物的化学式和粒子数目之比为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】已知某水泥样品的主要成分为成分为CaO、SiO2,并含有一定量的铁、铝和镁等金属的氧化物。现一实验小组利用实验室中的几种药品对该水泥样品进行检测,以确定其中各金属元素的含量
(1)取水泥样品10.0g,加入足量稀盐酸、氯化铵,使之完全溶解。待充分反应后发现仍有不溶物。将沉淀过滤后加热、干燥,所得固体为________ (填化学式)
(2)在分析水泥样品溶解过滤后的滤液成分时,实验小组的同学认为其中含有Ca2+、Al3+、Mg2+、Fe2+、Fe3+等阳离子,现欲准确测量各成分含量,需先加入试剂X将Fe2+转化为Fe3+,待滤液中的Fe2+全部转化为Fe3+后,再向其中加入足量的溶液Y并加热,可使滤液中的Al3+、Mg2+、Fe3+全部形成沉淀,则溶液Y名称是________ ,而试剂X可选用下列物质中的__________ (填选项)
a. HNO3 b. H2O2 c. KMnO4 d. Zn
(3)若将溶液Y改为氢氧化钠溶液,发现所得沉淀共1.008g,比原来减少了0.39g,而这些沉淀能恰好完全溶解于1mol/L,32mL的稀盐酸中,则上述说法中所涉及的水泥样品中金属元素种类及其分别占水泥样品的质量分数为____________ 、_____________ 、______________
(4)若最初的水泥样品改为用氢氧化钠溶液溶解,则可能发生的离子反应方程式是:________
(1)取水泥样品10.0g,加入足量稀盐酸、氯化铵,使之完全溶解。待充分反应后发现仍有不溶物。将沉淀过滤后加热、干燥,所得固体为
(2)在分析水泥样品溶解过滤后的滤液成分时,实验小组的同学认为其中含有Ca2+、Al3+、Mg2+、Fe2+、Fe3+等阳离子,现欲准确测量各成分含量,需先加入试剂X将Fe2+转化为Fe3+,待滤液中的Fe2+全部转化为Fe3+后,再向其中加入足量的溶液Y并加热,可使滤液中的Al3+、Mg2+、Fe3+全部形成沉淀,则溶液Y名称是
a. HNO3 b. H2O2 c. KMnO4 d. Zn
(3)若将溶液Y改为氢氧化钠溶液,发现所得沉淀共1.008g,比原来减少了0.39g,而这些沉淀能恰好完全溶解于1mol/L,32mL的稀盐酸中,则上述说法中所涉及的水泥样品中金属元素种类及其分别占水泥样品的质量分数为
(4)若最初的水泥样品改为用氢氧化钠溶液溶解,则可能发生的离子反应方程式是:
您最近一年使用:0次
填空题
|
适中
(0.65)
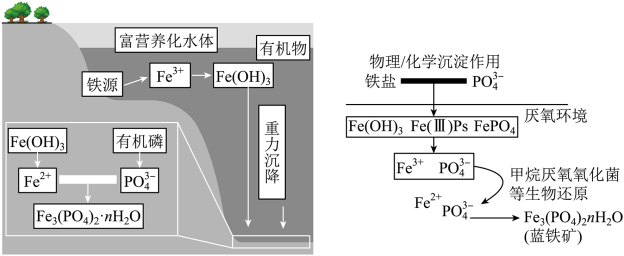
【推荐2】一方面,磷矿藏在地球上分布不均匀且储量有限;另一方面,污水中含有较多的磷元素。因此在污水处理生物污泥中的蓝铁矿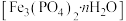 因其潜在的特殊用途以及经济价值而备受关注。蓝铁矿在自然水体中形成的过程如图。
因其潜在的特殊用途以及经济价值而备受关注。蓝铁矿在自然水体中形成的过程如图。
(1)水处理时,加入的高铁酸钾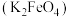 作为净水消毒剂,发生反应的化学方程式为
作为净水消毒剂,发生反应的化学方程式为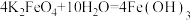 (胶体)
(胶体)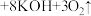 。
。
① 中
中 的化合价为
的化合价为_______ 价,上述反应涉及的物质中属于盐的是_______ 。
②高铁酸钾可用于净水消毒的原因是_______ 。
(2)在甲烷厌氧氧化菌的作用下,氢氧化铁和甲烷发生如下反应,配平该离子方程式:_______ 。

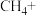

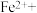
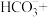

(3)无氧条件下加热,蓝铁矿(无杂质)发生分解: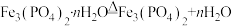 ,蓝铁矿的质量由5.02g减小为3.58g,则n=
,蓝铁矿的质量由5.02g减小为3.58g,则n=_______ ,蓝铁矿的相对分子质量为_______ 。
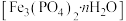 因其潜在的特殊用途以及经济价值而备受关注。蓝铁矿在自然水体中形成的过程如图。
因其潜在的特殊用途以及经济价值而备受关注。蓝铁矿在自然水体中形成的过程如图。
(1)水处理时,加入的高铁酸钾
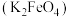 作为净水消毒剂,发生反应的化学方程式为
作为净水消毒剂,发生反应的化学方程式为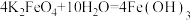 (胶体)
(胶体)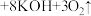 。
。①
 中
中 的化合价为
的化合价为②高铁酸钾可用于净水消毒的原因是
(2)在甲烷厌氧氧化菌的作用下,氢氧化铁和甲烷发生如下反应,配平该离子方程式:

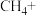

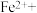
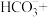

(3)无氧条件下加热,蓝铁矿(无杂质)发生分解:
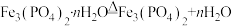 ,蓝铁矿的质量由5.02g减小为3.58g,则n=
,蓝铁矿的质量由5.02g减小为3.58g,则n=
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】Ⅰ.分别只用一种试剂除去下列各组中所含的少量杂质(括号内为杂质),在空格中填上需加入最适合的一种试剂:
(1)FeCl3溶液(FeCl2)________________ ,
(2)FeCl2溶液(FeCl3)________________ ,
(3)Fe 粉末(Al)_______________ ,
Ⅱ.为测定某镁铝合金样品中铝的含量,进行了下列实验:取一定量合金,加入100 mL 0.3 mol·L-1稀硝酸,合金完全溶解,产生的气体在标准状况下体积为560 mL;再加入0.2 mol·L-1 NaOH溶液至沉淀质量恰好不再变化,用去300 mL NaOH溶液。则所取样品中铝的物质的量为___________ ,反应中转移的电子数为______________ 。
(1)FeCl3溶液(FeCl2)
(2)FeCl2溶液(FeCl3)
(3)Fe 粉末(Al)
Ⅱ.为测定某镁铝合金样品中铝的含量,进行了下列实验:取一定量合金,加入100 mL 0.3 mol·L-1稀硝酸,合金完全溶解,产生的气体在标准状况下体积为560 mL;再加入0.2 mol·L-1 NaOH溶液至沉淀质量恰好不再变化,用去300 mL NaOH溶液。则所取样品中铝的物质的量为
您最近一年使用:0次



