钠元素在自然界中分布很广,储量极为丰富,且都以化合态存在,如氯化钠、碳酸钠、硫酸钠等,钠元素及其化合物在生产、生活中被广泛应用。请回答以下问题:
I.钠的价类二维图 中H元素的化合价是
中H元素的化合价是___________ 。
(2)钠单质通常保存在___________ 中。
(3)把钠放到装有水的烧杯中,钠会浮在水面上,原因是___________ ;能得出“该反应是放热反应”这一结论的实验现象是___________ 。
(4)请写出①中某种淡黄色固体的用途___________ 。
II.碳酸钠溶液的配制
(5)侯德榜是我国近代化学工业的奠基人之一,他提出的联合制法,也称侯氏制碱法。侯氏制碱法获得的产品常为碳酸钠和碳酸氢钠的混合物,若要除去碳酸钠粉末中混有的少量碳酸氢钠,最好的方法是___________ 。
(6)某同学利用提纯后的碳酸钠固体配制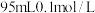 碳酸钠溶液,完成此实验将用到的仪器除量筒、烧杯、玻璃棒外还有
碳酸钠溶液,完成此实验将用到的仪器除量筒、烧杯、玻璃棒外还有___________ ,其中移液步骤中玻璃棒的作用是___________ 。
(7)下列操作会导致所配溶液浓度偏低的是___________ (填字母)
a.将烧杯中的溶液转移到容量瓶时不慎洒到容量瓶外
b.加水时不慎超过刻度线,把液体倒出一些
c.干净的容量瓶未经干燥就用于配制溶液
d.定容时俯视刻度线
III.焰色试验
节日燃放的五彩缤纷的烟花,所呈现的就是锂、钠、钾、锶、钡等金属元素的焰色。
(8)焰色试验中上述金属元素发生___________ (填“物理变化”或“化学变化”)。
(9)若使用某样品直接进行焰色试验时,火焰呈现黄色,说明该样品的元素组成中一定有___________ 元素,可能有___________ 元素(填元素名称)。
I.钠的价类二维图
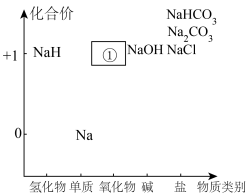
 中H元素的化合价是
中H元素的化合价是(2)钠单质通常保存在
(3)把钠放到装有水的烧杯中,钠会浮在水面上,原因是
(4)请写出①中某种淡黄色固体的用途
II.碳酸钠溶液的配制
(5)侯德榜是我国近代化学工业的奠基人之一,他提出的联合制法,也称侯氏制碱法。侯氏制碱法获得的产品常为碳酸钠和碳酸氢钠的混合物,若要除去碳酸钠粉末中混有的少量碳酸氢钠,最好的方法是
(6)某同学利用提纯后的碳酸钠固体配制
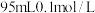 碳酸钠溶液,完成此实验将用到的仪器除量筒、烧杯、玻璃棒外还有
碳酸钠溶液,完成此实验将用到的仪器除量筒、烧杯、玻璃棒外还有(7)下列操作会导致所配溶液浓度偏低的是
a.将烧杯中的溶液转移到容量瓶时不慎洒到容量瓶外
b.加水时不慎超过刻度线,把液体倒出一些
c.干净的容量瓶未经干燥就用于配制溶液
d.定容时俯视刻度线
III.焰色试验
节日燃放的五彩缤纷的烟花,所呈现的就是锂、钠、钾、锶、钡等金属元素的焰色。
(8)焰色试验中上述金属元素发生
(9)若使用某样品直接进行焰色试验时,火焰呈现黄色,说明该样品的元素组成中一定有
更新时间:2024-01-21 21:24:52
|
相似题推荐
填空题
|
适中
(0.65)
名校
【推荐1】化学物质丰富多彩,在生产、生活、科研等方面都起着重要的作用。
(1) 的电子式为
的电子式为___________ 。
(2)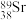 与
与 二者互为
二者互为___________ ;食盐不慎洒落在天然气的火焰上,观察的现象是___________ 。
(3)沾有水的铁制器皿在高温火焰上会发黑,该反应的化学方程式是___________ 。
(4)小苏打可用于烘焙糕点,在烘焙受热过程中涉及的化学方程式是___________ 。
(5)家庭厨卫管道常因留有菜渣、毛发而造成堵塞,可用管道疏通剂疏通。常用的管道疏通剂主要成分有铝粉和氢氧化钠,请用离子方程式表达其疏通原理:___________ 。
(6)工业上用焦炭还原石英砂可以制得含有少量杂质的粗硅。请写出化学方程式:___________ 。
(1)
 的电子式为
的电子式为(2)
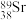 与
与 二者互为
二者互为(3)沾有水的铁制器皿在高温火焰上会发黑,该反应的化学方程式是
(4)小苏打可用于烘焙糕点,在烘焙受热过程中涉及的化学方程式是
(5)家庭厨卫管道常因留有菜渣、毛发而造成堵塞,可用管道疏通剂疏通。常用的管道疏通剂主要成分有铝粉和氢氧化钠,请用离子方程式表达其疏通原理:
(6)工业上用焦炭还原石英砂可以制得含有少量杂质的粗硅。请写出化学方程式:
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】请回答下列问题:
(1)云、雾属于胶体,鉴别胶体和溶液的方法是___________ ,胶体和溶液的本质区别是___________ 。
(2)钠的焰色试验的焰色为___________ 色;钠着火了不能用水而需要用干燥的沙土来灭火,请用离子方程式来表示其原因___________ 。
(3)过氧化钠是一种___________ 色的固体,可作漂白剂和呼吸面具中的供氧剂,写出过氧化钠和二氧化碳反应的化学方程式,并用双线桥法表示电子转移的方向和数目:___________ 。
(4)小苏打可用于治疗胃酸过多,其原理用离子反应方程式表示为___________
(5)漂白粉是将氯气通入冷的石灰乳中制得的,写出该制备原理的化学方程式___________ 。
(1)云、雾属于胶体,鉴别胶体和溶液的方法是
(2)钠的焰色试验的焰色为
(3)过氧化钠是一种
(4)小苏打可用于治疗胃酸过多,其原理用离子反应方程式表示为
(5)漂白粉是将氯气通入冷的石灰乳中制得的,写出该制备原理的化学方程式
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】下表列出了A-R9种元素在周期表中的位置(填元素符号)
(1)这9种元素中化学性质最不活泼的是___________ ;G的最高价氧化物的水化物化学式是___________ 。
(2)A、D元素的最高价氧化物对应水化物反应的离子方程式是___________ 。
(3)A、B、C三种元素按原子半径由大到小的顺序排列为___________ 。
(4)F元素氢化物的化学式是___________ ,该氢化物在常温下跟B发生反应的化学方程式是___________ ,所得溶液的pH___________ 7。(填“>”、“=”或“<”)
(5)H元素跟A元素形成化合物的化学式是___________ ,高温灼烧该化合物时,火焰呈___________ 色。
| 周期/族 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
2 | E | F | ||||||
3 | A | C | D | G | R | |||
4 | B | H |
(2)A、D元素的最高价氧化物对应水化物反应的离子方程式是
(3)A、B、C三种元素按原子半径由大到小的顺序排列为
(4)F元素氢化物的化学式是
(5)H元素跟A元素形成化合物的化学式是
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】在进行钠和水的反应实验中,有如下操作和实验现象,回答下列各问题。
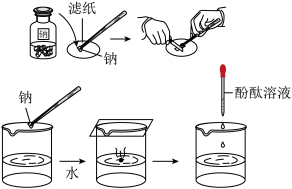
(1)金属钠保存在___________ 中。
(2)金属钠块投入水中后,观察到___________ (说明反应放热)。
(3)钠小球在水面上迅速游动,发出“嘶嘶”的声响,说明反应有___________ 生成。
(4)如果水中事先已滴入酚酞溶液,反应后溶液由无色变为___________ 色。
(5)在①发生的离子方程式为:___________ 。

(1)金属钠保存在
(2)金属钠块投入水中后,观察到
(3)钠小球在水面上迅速游动,发出“嘶嘶”的声响,说明反应有
(4)如果水中事先已滴入酚酞溶液,反应后溶液由无色变为
(5)在①发生的离子方程式为:
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】元素的价类二维图是我们学习元素及其化合物相关知识的重要模型和工具。如图是钠的价类二维图:
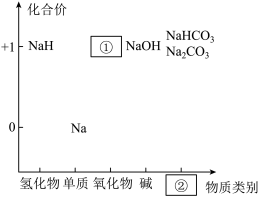
(1)②处应填的物质类别是___________ ;
(2)将钠放入水中发生反应的离子方程式是___________ ;
(3)Na可用石蜡封存,实验室少量Na保存于___________ 中;
(4)将Na2O2投入盛有CuSO4溶液的烧杯中,观察到的现象是___________(填标号);
(5)向酸性KMnO4溶液中加入Na2O2粉末,观察到溶液褪色,发生如下反应:
____ +____Na2O2+______→ ______Mn2++______Na++_____+_____H2O(未配平)
+____Na2O2+______→ ______Mn2++______Na++_____+_____H2O(未配平)
首先请补全方程式并配平__________ ,然后回答反应中被还原的元素是___________ ;反应中每消耗1molNa2O2的同时有___________ mol电子转移。

(1)②处应填的物质类别是
(2)将钠放入水中发生反应的离子方程式是
(3)Na可用石蜡封存,实验室少量Na保存于
(4)将Na2O2投入盛有CuSO4溶液的烧杯中,观察到的现象是___________(填标号);
| A.有气体生成 | B.无气体生成 | C.有蓝色沉淀生成 | D.大量红色固体铜生成 |
(5)向酸性KMnO4溶液中加入Na2O2粉末,观察到溶液褪色,发生如下反应:
____
 +____Na2O2+______→ ______Mn2++______Na++_____+_____H2O(未配平)
+____Na2O2+______→ ______Mn2++______Na++_____+_____H2O(未配平)首先请补全方程式并配平
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】按要求回答下列问题
(1)我国古代的黑火药是由硫磺粉、硝酸钾和木炭粉按一定比例混合而成,爆炸时的反应为: 。该反应的还原剂是
。该反应的还原剂是___________ ,当3.2 g S参与反应时,生成的气体体积为___________ L(标准状况下)。
(2)下列物质:①Ca(ClO)2;②Na2O2;③Fe2O3;④La-Ni合金分别用来做供氧剂、油漆涂料、储氢材料、漂粉精的是___________ (按顺序填对应序号)。
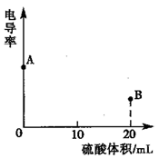
(3)已知溶液电导率越大,导电性越强。向20 mL0.1 mol/LBa(OH)2溶液中漓入几滴酚酞溶液,然后向其中逐滴加入20 mL0.2 mol/LH2SO4溶液,测定溶液电导率的变化。实验过程中溶液中的现象为______ ,该反应的离子方程式___________ ,在下图画出反应过程中溶液电导率变化示意图___________ (起点为A,终点为B)。
(1)我国古代的黑火药是由硫磺粉、硝酸钾和木炭粉按一定比例混合而成,爆炸时的反应为:
 。该反应的还原剂是
。该反应的还原剂是(2)下列物质:①Ca(ClO)2;②Na2O2;③Fe2O3;④La-Ni合金分别用来做供氧剂、油漆涂料、储氢材料、漂粉精的是
(3)已知溶液电导率越大,导电性越强。向20 mL0.1 mol/LBa(OH)2溶液中漓入几滴酚酞溶液,然后向其中逐滴加入20 mL0.2 mol/LH2SO4溶液,测定溶液电导率的变化。实验过程中溶液中的现象为

您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】2021年10月16日,神舟十三号载人飞船顺利进入预定轨道。飞船的轨道舱内安装盛有 颗粒的装置,为宇航员供氧。回答下列问题:
颗粒的装置,为宇航员供氧。回答下列问题:

(1) 的制取。将金属钠加热至熔化,通入一定量已除去
的制取。将金属钠加热至熔化,通入一定量已除去 的干燥空气,加热并维持温度在180~200℃之间,钠被氧化成
的干燥空气,加热并维持温度在180~200℃之间,钠被氧化成 ,进而增加空气流量,迅速升温至300~400℃,制得过氧化钠。过氧化钠要密封保存,避免与水蒸气和二氧化碳反应,其中
,进而增加空气流量,迅速升温至300~400℃,制得过氧化钠。过氧化钠要密封保存,避免与水蒸气和二氧化碳反应,其中 与水蒸气反应的化学方程式为
与水蒸气反应的化学方程式为_______ 。
(2) 的供氧。过氧化钠能与人体呼出的酸性氧化物发生反应,其化学方程式为
的供氧。过氧化钠能与人体呼出的酸性氧化物发生反应,其化学方程式为_______ ,该反应中的还原剂是_______ (填写化学式)。
(3)反应后组成的探究。 使用后会失去供氧能力(又称失效供氧剂),某“失效供氧剂”的化学组成可能是
使用后会失去供氧能力(又称失效供氧剂),某“失效供氧剂”的化学组成可能是 或
或 或两者的混合物。为探究“失效供氧剂”的化学组成,化学探究小组进行如下实验:
或两者的混合物。为探究“失效供氧剂”的化学组成,化学探究小组进行如下实验:
①取适量“失效供氧剂”于试管中,加热,产生能使澄清石灰水变浑浊的气体,产生该气体的化学反应方程式为_______ 。
②称取19.0g“失效供氧剂”加入足量稀硫酸,将生成的气体用浓硫酸干燥后,再用碱石灰完全吸收,碱石灰增重8.8g,该“失效供氧剂”的化学组成为_______ (只填写化学式)。
 颗粒的装置,为宇航员供氧。回答下列问题:
颗粒的装置,为宇航员供氧。回答下列问题:
(1)
 的制取。将金属钠加热至熔化,通入一定量已除去
的制取。将金属钠加热至熔化,通入一定量已除去 的干燥空气,加热并维持温度在180~200℃之间,钠被氧化成
的干燥空气,加热并维持温度在180~200℃之间,钠被氧化成 ,进而增加空气流量,迅速升温至300~400℃,制得过氧化钠。过氧化钠要密封保存,避免与水蒸气和二氧化碳反应,其中
,进而增加空气流量,迅速升温至300~400℃,制得过氧化钠。过氧化钠要密封保存,避免与水蒸气和二氧化碳反应,其中 与水蒸气反应的化学方程式为
与水蒸气反应的化学方程式为(2)
 的供氧。过氧化钠能与人体呼出的酸性氧化物发生反应,其化学方程式为
的供氧。过氧化钠能与人体呼出的酸性氧化物发生反应,其化学方程式为(3)反应后组成的探究。
 使用后会失去供氧能力(又称失效供氧剂),某“失效供氧剂”的化学组成可能是
使用后会失去供氧能力(又称失效供氧剂),某“失效供氧剂”的化学组成可能是 或
或 或两者的混合物。为探究“失效供氧剂”的化学组成,化学探究小组进行如下实验:
或两者的混合物。为探究“失效供氧剂”的化学组成,化学探究小组进行如下实验:①取适量“失效供氧剂”于试管中,加热,产生能使澄清石灰水变浑浊的气体,产生该气体的化学反应方程式为
②称取19.0g“失效供氧剂”加入足量稀硫酸,将生成的气体用浓硫酸干燥后,再用碱石灰完全吸收,碱石灰增重8.8g,该“失效供氧剂”的化学组成为
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】在我国青海湖地区有一种说法:“冬天捞碱,夏天晒盐”,这里的碱是指Na2CO3,盐是指NaCl。
(1)湖水晒盐的原理与化学实验中的______ (填一种实验操作的名称)原理相似,该过程是______ 变化(填“物理”或“化学”)。
(2)Na2CO3的摩尔质量为______ ,Na2CO3是属于______ 类物质(填“酸”、“碱”、“盐”或“氧化物”)。
(3)将捞得的碱提纯得到纯净的Na2CO3固体,实验需要0.05mol/L的Na2CO3溶液950mL,配制时应选用容量瓶的规格和称取Na2CO3的质量分别为______ (填序号)。
(4)若配制溶液定容时俯视刻度线,则对所配溶液的浓度有何影响______ (填“偏大”“偏小”或“无影响”)。
(5)若配制溶液时的操作完全正确,则下列有关该溶液的说法正确的是______ 。
(1)湖水晒盐的原理与化学实验中的
(2)Na2CO3的摩尔质量为
(3)将捞得的碱提纯得到纯净的Na2CO3固体,实验需要0.05mol/L的Na2CO3溶液950mL,配制时应选用容量瓶的规格和称取Na2CO3的质量分别为
| A.1000mL,5.3g | B.950mL,5.04g | C.1000mL,5.04g | D.950mL,5.3g |
(5)若配制溶液时的操作完全正确,则下列有关该溶液的说法正确的是
| A.1L该溶液中含有Na+的个数为6.02×1022 |
| B.从该溶液中取出10mL,溶质的物质的量浓度仍为0.05mol/L |
| C.2L该溶液中Na+的物质的量浓度为0.20mol/L |
| D.1L该溶液中含有氧原子的个数为9.03×1022 |
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】物质的量是联系宏观量与微观粒子数量的重要桥梁。回答下列问题:
(1)某汽车安全气囊的气体发生剂为叠氮化钠(NaN3),在受到撞击时分解生成Na和N2,130 g NaN3分解产生的N2在标准状况下的体积为______ L。
(2)SO2和O2组成的混合气体在标准状况下的密度为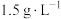 ,其中SO2的物质的量分数为
,其中SO2的物质的量分数为______ 。
(3)64 g铜与300 mL一定浓度的硝酸恰好完全反应,产生的NO和NO2混合气体在标准状况下的体积共22.4 L。NO与NO2的体积比为______ ,该硝酸的物质的量浓度为______  。
。
(4)实验室需使用240 mL物质的量浓度为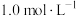 的稀硫酸进行有关实验,现用98%的浓硫酸进行配制。
的稀硫酸进行有关实验,现用98%的浓硫酸进行配制。
①需用量筒量取98%的浓硫酸(密度为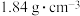 )
)______ mL。
②下列情况会导致所配溶液浓度偏高的是______ (填标号)。
a.定容后摇匀时有少量溶液溅出
b.定容时仰视容量瓶瓶颈上的刻度线
c.使用量筒量取浓硫酸时仰视刻度线
d.硫酸溶液移入容量瓶后没有洗涤烧杯
e.稀释后未冷却即进行移液、定容等操作
(1)某汽车安全气囊的气体发生剂为叠氮化钠(NaN3),在受到撞击时分解生成Na和N2,130 g NaN3分解产生的N2在标准状况下的体积为
(2)SO2和O2组成的混合气体在标准状况下的密度为
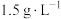 ,其中SO2的物质的量分数为
,其中SO2的物质的量分数为(3)64 g铜与300 mL一定浓度的硝酸恰好完全反应,产生的NO和NO2混合气体在标准状况下的体积共22.4 L。NO与NO2的体积比为
 。
。(4)实验室需使用240 mL物质的量浓度为
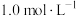 的稀硫酸进行有关实验,现用98%的浓硫酸进行配制。
的稀硫酸进行有关实验,现用98%的浓硫酸进行配制。①需用量筒量取98%的浓硫酸(密度为
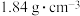 )
)②下列情况会导致所配溶液浓度偏高的是
a.定容后摇匀时有少量溶液溅出
b.定容时仰视容量瓶瓶颈上的刻度线
c.使用量筒量取浓硫酸时仰视刻度线
d.硫酸溶液移入容量瓶后没有洗涤烧杯
e.稀释后未冷却即进行移液、定容等操作
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】如图为某市售盐酸试剂瓶标签上的部分数据。
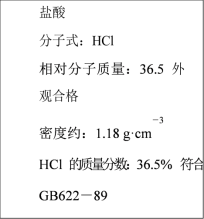
回答下列问题:
(1)该盐酸的物质的量浓度为___________ 。
(2)下列实验操作会导致实验结果偏低的是___________ (填序号)。
①配制 100 g 10%的 CuSO4 溶液,称取 10 g 硫酸铜晶体溶于 90 g 水中;
②测定碳酸钠晶体中结晶水的百分含量时,所用的晶体已经受潮;
③配制一定物质的量浓度的溶液时,药品与砝码放反了,游码读数为 0.2 g, 所得溶液的浓度;
④用酸式滴定管量取用 98%,密度为 1.84 g·cm-3 的浓 H2SO4 配制 200 mL 2mol·L-1 的稀 H2SO4 时,先平视后仰视。
(3)已知 CO 和 CO2 的混合气体 14.4 g,在标准状况下所占的体积为 8.96 L。则该混合气体中,CO 的质量为____ g,CO2 的物质的量为______ mol。
(4)1 mol 氧气在放电条件下,有 30%转化为臭氧(O3),则放电后所得混合气体对氢气的相对密度是___________ (填字母)。
A.16 B.17.8 C.18.4 D.35.6
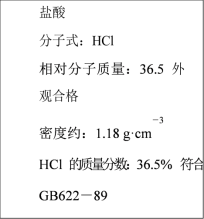
回答下列问题:
(1)该盐酸的物质的量浓度为
(2)下列实验操作会导致实验结果偏低的是
①配制 100 g 10%的 CuSO4 溶液,称取 10 g 硫酸铜晶体溶于 90 g 水中;
②测定碳酸钠晶体中结晶水的百分含量时,所用的晶体已经受潮;
③配制一定物质的量浓度的溶液时,药品与砝码放反了,游码读数为 0.2 g, 所得溶液的浓度;
④用酸式滴定管量取用 98%,密度为 1.84 g·cm-3 的浓 H2SO4 配制 200 mL 2mol·L-1 的稀 H2SO4 时,先平视后仰视。
(3)已知 CO 和 CO2 的混合气体 14.4 g,在标准状况下所占的体积为 8.96 L。则该混合气体中,CO 的质量为
(4)1 mol 氧气在放电条件下,有 30%转化为臭氧(O3),则放电后所得混合气体对氢气的相对密度是
A.16 B.17.8 C.18.4 D.35.6
您最近一年使用:0次

 中含有的阴离子个数约为
中含有的阴离子个数约为 和
和 ,其质量之比为
,其质量之比为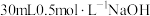 溶液加水稀释到
溶液加水稀释到 ,稀释后溶液中
,稀释后溶液中 的物质的量浓度为
的物质的量浓度为 某二价金属的氯化物
某二价金属的氯化物 中含有
中含有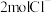 ,则
,则 的摩尔质量为
的摩尔质量为

