氯化铁 FeCl3是一种化学常用试剂,在化学实验和工农业生产有着重要的用途。
(1)实验室常用饱和FeCl3溶液来制备Fe(OH)3胶体。
已知:在25℃时,FeCl3的溶解度为90g/100g水。
实验Ⅰ:配置20.0g饱和FeCl3溶液。
①需要用到的仪器有:药匙、托盘天平、玻璃棒、___________ 、___________ 、烧杯。
②该实验需称量FeCl3固体___________ g。
实验Ⅱ:制备Fe(OH)3胶体。
甲同学取一小烧杯,加入25mL蒸馏水,加热至沸腾,向沸水中逐滴加入1~2mL饱和氯化铁溶液,继续煮沸至液体呈红褐色,停止加热。
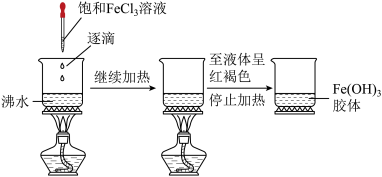
③写出此过程中的化学方程式:___________ 。
④除去氢氧化铁胶体中的氯化铁采用的方法是___________ (填写字母)。
A.过滤 B.渗析 C.蒸发
(2)工业上制印刷电路板时常用FeCl3溶液做“腐蚀液”,原理为利用FeCl3溶液将Cu溶解。某化学兴趣小组根据此原理在覆铜板上制作“化学”字样的图案。
实验Ⅲ:利用覆铜板制作图案
①写出制作过程发生反应的离子方程式:___________ 。
②使用过的“腐蚀液”会失效,但还可以回收利用,其中有一步反应需要将Fe2+转化为Fe3+,下列试剂能实现上述变化的是___________ (填序号)。
A.氯气 B.铁 C.酸性KMnO4溶液 D.稀硫酸
(1)实验室常用饱和FeCl3溶液来制备Fe(OH)3胶体。
已知:在25℃时,FeCl3的溶解度为90g/100g水。
实验Ⅰ:配置20.0g饱和FeCl3溶液。
①需要用到的仪器有:药匙、托盘天平、玻璃棒、
②该实验需称量FeCl3固体
实验Ⅱ:制备Fe(OH)3胶体。
甲同学取一小烧杯,加入25mL蒸馏水,加热至沸腾,向沸水中逐滴加入1~2mL饱和氯化铁溶液,继续煮沸至液体呈红褐色,停止加热。

③写出此过程中的化学方程式:
④除去氢氧化铁胶体中的氯化铁采用的方法是
A.过滤 B.渗析 C.蒸发
(2)工业上制印刷电路板时常用FeCl3溶液做“腐蚀液”,原理为利用FeCl3溶液将Cu溶解。某化学兴趣小组根据此原理在覆铜板上制作“化学”字样的图案。
实验Ⅲ:利用覆铜板制作图案
| 实验原理 | 利用FeCl3溶液做“腐蚀液”,将覆铜板上不需要的铜腐蚀。 |
| 实验操作 | 1.取一小块覆铜板,用油性笔在覆铜板画上设计好的“化学”图案; 2.浸入盛有FeCl3溶液的小烧杯中; 3.一段时间后,取出覆铜板并用水清洗干净; 4.观察实验现象,并展示制作的图案。  |
| 实验现象 | 用油性笔画出的图案处不被腐蚀,洗净后板上留下设计的“化学”图案。 |
| 离子方程式 | |
| 实验结论 | 铜可以被FeCl3溶液腐蚀。 |
②使用过的“腐蚀液”会失效,但还可以回收利用,其中有一步反应需要将Fe2+转化为Fe3+,下列试剂能实现上述变化的是
A.氯气 B.铁 C.酸性KMnO4溶液 D.稀硫酸
更新时间:2024-01-24 10:48:48
|
相似题推荐
解答题-实验探究题
|
适中
(0.65)
【推荐1】已知FeSO4·7H2O晶体在加热条件下发生如下反应:2FeSO4·7H2O Fe2O3+SO2↑+SO3↑+14H2O↑;如图的装置可用来检验上述反应中所有的气体产物,请回答下列问题:
Fe2O3+SO2↑+SO3↑+14H2O↑;如图的装置可用来检验上述反应中所有的气体产物,请回答下列问题:
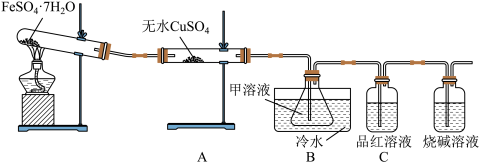
(1)用于检验SO2气体的装置是______ (填装置的字母),确认水蒸气存在的现象是______ ;
(2)利用装置B可以确认的产物是______ ,装置B中的甲溶液可选(填序号)______ 。
①足量澄清石灰水 ②足量氯化钡溶液 ③足量硝酸钡溶液
该装置中冷水的作用是______ ;
(3)为探究Fe2O3的性质和用途,取试管中少许固体溶于适量盐酸中制备饱和铁盐溶液,将此饱和溶液逐滴加入沸水中加热片刻,观察液体的颜色变为______ ,检验该分散系最简方法的操作为______ .
 Fe2O3+SO2↑+SO3↑+14H2O↑;如图的装置可用来检验上述反应中所有的气体产物,请回答下列问题:
Fe2O3+SO2↑+SO3↑+14H2O↑;如图的装置可用来检验上述反应中所有的气体产物,请回答下列问题:
(1)用于检验SO2气体的装置是
(2)利用装置B可以确认的产物是
①足量澄清石灰水 ②足量氯化钡溶液 ③足量硝酸钡溶液
该装置中冷水的作用是
(3)为探究Fe2O3的性质和用途,取试管中少许固体溶于适量盐酸中制备饱和铁盐溶液,将此饱和溶液逐滴加入沸水中加热片刻,观察液体的颜色变为
您最近半年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐2】AgI是难溶于水的黄色沉淀,在一定条件下也可以形成胶体。某兴趣小组设计如下实验探究某种条件对AgI胶体粒子所带电性的影响:
实验①:将稀AgNO3溶液逐滴加入过量的稀KI溶液中,得到AgI胶体Ⅰ;
实验②:将稀KI溶液逐滴加入过量的稀AgNO3溶液中,得到AgI胶体Ⅱ;
实验③:将提纯后的AgI胶体Ⅰ与AgI胶体Ⅱ进行混合,出现了黄色沉淀。
完成下列填空:
(1)写出制备AgI胶体Ⅰ的化学方程式:_______ 。确认AgI胶体Ⅰ中胶体粒子所带电性的实验方法称为_______ 。
(2)提纯AgI胶体的方法如图所示。材料X称为_______ 。用该法提纯AgI胶体Ⅱ,进入蒸馏水中而被除去的离子有_______ (写出三种)。

(3)本实验的探究结论是制备AgI胶体时_______ 对胶体粒子所带电性_______ (选填“有”或“无”)影响。简述作出此判断的理由_______ 。
(4)有同学认为在进行实验③时无需提纯,直接将实验①、②中得到的分散系混合,也能得到相同的探究结论。判断他的说法是否合理并说明理由。_______ 。
实验①:将稀AgNO3溶液逐滴加入过量的稀KI溶液中,得到AgI胶体Ⅰ;
实验②:将稀KI溶液逐滴加入过量的稀AgNO3溶液中,得到AgI胶体Ⅱ;
实验③:将提纯后的AgI胶体Ⅰ与AgI胶体Ⅱ进行混合,出现了黄色沉淀。
完成下列填空:
(1)写出制备AgI胶体Ⅰ的化学方程式:
(2)提纯AgI胶体的方法如图所示。材料X称为

(3)本实验的探究结论是制备AgI胶体时
(4)有同学认为在进行实验③时无需提纯,直接将实验①、②中得到的分散系混合,也能得到相同的探究结论。判断他的说法是否合理并说明理由。
您最近半年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐3】由工业明胶制成的胶囊往往含有超标的重金属铬,从而对人体造成伤害。明胶是水溶性蛋白质混合物,溶于水形成胶体。
(1)已知Fe(CrO2)2中铬元素是+3价,则其中铁元素是_________ 价。
(2)明胶的水溶液和K2SO4溶液共同具备的性质是_________ (填字母)。
a.都不稳定,密封放置沉淀
b.两者均有丁达尔效应
c.分散质粒子可通过滤纸
(3)现有10mL明胶的水溶液与5mLNaCl溶液混合装入半透膜内,将此半透膜袋浸入盛蒸馏水的烧杯中,设计实验证明NaCl中氯离子能够透过半透膜:取烧杯中溶液少许于试管中,先加入稀硝酸,再加入_________ 溶液,若有_________ 生成,则证明有氯离子透过半透膜。
(4)取少量Fe2O3粉末(红棕色)加入适量盐酸,反应后得到的FeCl3溶液呈棕黄色。用此溶液进行以下实验:
①取少量FeCl3溶液置于试管中,滴入NaOH溶液,可观察到有红褐色沉淀生成,反应的化学方程式为_________ 。
②在小烧杯中加入20mL蒸馏水,加热至沸腾后,向沸水中滴入几滴FeCl3溶液,继续煮沸至溶液呈红褐色,停止加热,制得的分散系为_________ ,鉴别此分散系和溶液的方法是_________ 。写出该制备过程的化学方程式:_________ 。
(1)已知Fe(CrO2)2中铬元素是+3价,则其中铁元素是
(2)明胶的水溶液和K2SO4溶液共同具备的性质是
a.都不稳定,密封放置沉淀
b.两者均有丁达尔效应
c.分散质粒子可通过滤纸
(3)现有10mL明胶的水溶液与5mLNaCl溶液混合装入半透膜内,将此半透膜袋浸入盛蒸馏水的烧杯中,设计实验证明NaCl中氯离子能够透过半透膜:取烧杯中溶液少许于试管中,先加入稀硝酸,再加入
(4)取少量Fe2O3粉末(红棕色)加入适量盐酸,反应后得到的FeCl3溶液呈棕黄色。用此溶液进行以下实验:
①取少量FeCl3溶液置于试管中,滴入NaOH溶液,可观察到有红褐色沉淀生成,反应的化学方程式为
②在小烧杯中加入20mL蒸馏水,加热至沸腾后,向沸水中滴入几滴FeCl3溶液,继续煮沸至溶液呈红褐色,停止加热,制得的分散系为
您最近半年使用:0次
【推荐1】Ni(OH)2作为合成镍钴锰三元电极材料的原料,工业上可用红土镍矿(主要成分为NiO、FeO、Fe2O3、MgO和SiO2)制备,工艺流程如图所示。回答下列问题:
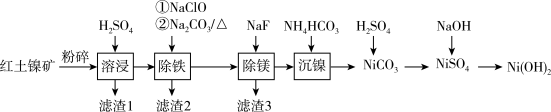
(1)“滤渣l”的成分为_____________ (写化学式)。
(2)“除铁"中,加入NaClO的目的是将溶液中的Fe2+氧化为Fe3+,写出该反应的离子方程式:________________________________________ ,为了证明加入NaClO已足量,可选择的试剂是__________ (填字母标号)。
a.KSCN溶液、氯水 b.K3[Fe(CN)6]溶液 c.NaOH溶液
(3)Na2CO3的作用是调节溶液pH使Fe3+沉淀,根据下表的数据,则调节溶液pH的范围是__________ 。
(4)“除镁”中,若溶液pH过小,Mg2+沉淀不完全,用化学平衡移动的原理解释其原因是______________________________________________________________________ 。
(5)“沉镍”时有能使澄清石灰水变浑浊的气体生成,则该反应的离子方程式为_______ 。

(1)“滤渣l”的成分为
(2)“除铁"中,加入NaClO的目的是将溶液中的Fe2+氧化为Fe3+,写出该反应的离子方程式:
a.KSCN溶液、氯水 b.K3[Fe(CN)6]溶液 c.NaOH溶液
(3)Na2CO3的作用是调节溶液pH使Fe3+沉淀,根据下表的数据,则调节溶液pH的范围是
金属离子 | Fe2+ | Fe3+ | Mg2+ | Ni2+ |
开始沉淀的pH | 6.3 | 1.5 | 8.9 | 6.9 |
沉淀完全的pH | 8.3 | 2.8 | 10.9 | 8.9 |
(4)“除镁”中,若溶液pH过小,Mg2+沉淀不完全,用化学平衡移动的原理解释其原因是
(5)“沉镍”时有能使澄清石灰水变浑浊的气体生成,则该反应的离子方程式为
您最近半年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐2】某溶液A中可能含有 、
、 、
、 、
、 、
、 、Fe2+、Al3+、Fe3+中的几种离子,且溶液中各离子的物质的量浓度均为0.1 mol/L。现取100 mL该溶液A进行如下实验:
、Fe2+、Al3+、Fe3+中的几种离子,且溶液中各离子的物质的量浓度均为0.1 mol/L。现取100 mL该溶液A进行如下实验:
实验1:向该溶液中逐滴滴入过量的(NH4)2CO3溶液,产生白色沉淀B,并有无色气泡产生。
实验2:静置后,再向溶液中加入过量Ba(OH)2溶液,加热,仍然存在白色沉淀C,并有无色气泡产生。
实验3:静置后,继续向溶液中加入Cu片和过量的盐酸,仍然存在白色沉淀D,溶液变蓝色,并有气泡E产生。
(1)白色沉淀C的成分为_________________ (填化学式);气体E的成分为_______________ 、_______________ (写名称)。
(2)实验1中发生反应的离子方程式为_________________________________________ 。
(3)实验3中发生所有反应的离子方程式为________________________________________ ,
________________________________________________________________________________ 。
(4)溶液A中__________ (填“一定”“可能”或“一定不”)存在 ,理由是
,理由是________________________________________________________ 。
 、
、 、
、 、
、 、
、 、Fe2+、Al3+、Fe3+中的几种离子,且溶液中各离子的物质的量浓度均为0.1 mol/L。现取100 mL该溶液A进行如下实验:
、Fe2+、Al3+、Fe3+中的几种离子,且溶液中各离子的物质的量浓度均为0.1 mol/L。现取100 mL该溶液A进行如下实验:实验1:向该溶液中逐滴滴入过量的(NH4)2CO3溶液,产生白色沉淀B,并有无色气泡产生。
实验2:静置后,再向溶液中加入过量Ba(OH)2溶液,加热,仍然存在白色沉淀C,并有无色气泡产生。
实验3:静置后,继续向溶液中加入Cu片和过量的盐酸,仍然存在白色沉淀D,溶液变蓝色,并有气泡E产生。
(1)白色沉淀C的成分为
(2)实验1中发生反应的离子方程式为
(3)实验3中发生所有反应的离子方程式为
(4)溶液A中
 ,理由是
,理由是
您最近半年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
【推荐3】煅烧黄铁矿 会生成一种红棕色物质,以煅烧黄铁矿
会生成一种红棕色物质,以煅烧黄铁矿 (杂质为石英等)产生的红渣为原料制备铵铁蓝
(杂质为石英等)产生的红渣为原料制备铵铁蓝 颜料。工艺流程如下:
颜料。工艺流程如下:
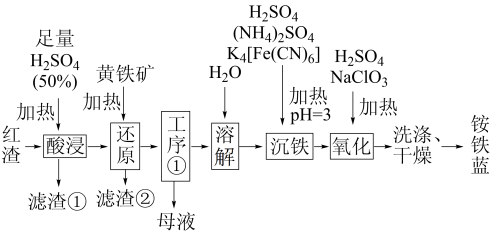
回答下列问题:
(1)煅烧黄铁矿的化学方程式为_______ ,滤渣①的主要成分为_______ (填化学式)。
(2)还原工序中,不生成S单质的反应的离子方程式为_______ 。
(3)沉铁工序产生的白色沉淀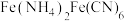 中
中 的化合价为
的化合价为_______ ,氧化工序发生反应的离子方程式为_______ 。
(4)若用还原工序得到的滤液制备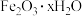 和
和 ,所加试剂为
,所加试剂为_______ 和_______ (填化学式,不引入杂质)。
 会生成一种红棕色物质,以煅烧黄铁矿
会生成一种红棕色物质,以煅烧黄铁矿 (杂质为石英等)产生的红渣为原料制备铵铁蓝
(杂质为石英等)产生的红渣为原料制备铵铁蓝 颜料。工艺流程如下:
颜料。工艺流程如下:
回答下列问题:
(1)煅烧黄铁矿的化学方程式为
(2)还原工序中,不生成S单质的反应的离子方程式为
(3)沉铁工序产生的白色沉淀
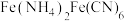 中
中 的化合价为
的化合价为(4)若用还原工序得到的滤液制备
 和
和 ,所加试剂为
,所加试剂为
您最近半年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐1】某工业矿渣中主要含有Cu2O,还有少部分Al2O3、Fe2O3、SiO2 ,从该矿渣中提取铜的操作流程如下:(已知:Cu2O+2H+═Cu+Cu2++H2O)
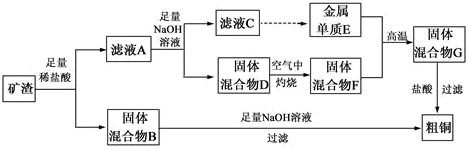
(1)固体混合物B与氢氧化钠溶液反应的化学方程式为_________________ 。
该反应物的一种重要用途为___________________________ 。
(2)滤液A中铁元素的存在形式只能为Fe2+,理由是_________________ 。涉及的离子方程式为(不必书写Cu2O与盐酸的反应)_________________ 、_________________ 。检验滤液A中Fe2+的试剂为________________ 。
(3)若将滤液C中的铝元素以沉淀形式析出,可选用的最佳试剂为______ (填序号)。
A.氢氧化钠溶液 B.硫酸溶液 C.氨水 D.二氧化碳
金属E与固体F某一成分发生的反应可用于焊接钢轨,该反应的化学方程为______________ 。

(1)固体混合物B与氢氧化钠溶液反应的化学方程式为
该反应物的一种重要用途为
(2)滤液A中铁元素的存在形式只能为Fe2+,理由是
(3)若将滤液C中的铝元素以沉淀形式析出,可选用的最佳试剂为
A.氢氧化钠溶液 B.硫酸溶液 C.氨水 D.二氧化碳
金属E与固体F某一成分发生的反应可用于焊接钢轨,该反应的化学方程为
您最近半年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
解题方法
【推荐2】铜及其化合物在生产、生活中有广泛的应用。
(1)铜可采用如下方法制备:
火法炼铜:Cu2S+O2 2Cu+SO2
2Cu+SO2
湿法炼铜:CuSO4+Fe=FeSO4+Cu
上述两种方法中,铜元素均被__ (填“氧化”或“还原”)成铜单质。
(2)印刷电路板上使用的铜需要回收利用。
方法一:用FeCl3溶液浸泡印刷电路板制备CuCl2·2H2O,实验室模拟回收过程如图:

①步骤1的离子方程式为__ ,证明步骤1所加FeCl3溶液过量的方法是__ 。
②步骤2中所加的氧化剂最适宜的是__ 。
A.HNO3 B.H2O2 C.KMnO4 D.氯水
写出加氧化剂相关的离子方程式__ (写一个即可)。
③步骤3的目的是使溶液的pH升高到4.2,此时Fe3+完全沉淀,可选用的试剂1是___ 。(写出一种即可)
④蒸发浓缩CuCl2溶液时,要滴加浓盐酸,目的是___ (用化学方程式并结合简要的文字说明),再经___ 、过滤得到CuCl2·2H2O。
(3)方法二:用H2O2和硫酸共同浸泡印刷电路板制备硫酸铜,其热化学方程式是:
Cu(s)+H2O2(l)+H2SO4(aq)=CuSO4(aq)+2H2O(l) △H1=-320kJ/mol
又知:2H2O2(l)=2H2O(l)+O2(g) △H2=-196kJ/mol
H2(g)+ O2(g)=H2O(l) △H3=-286kJ/mol
O2(g)=H2O(l) △H3=-286kJ/mol
则反应Cu(s)+H2SO4(aq)=CuSO4(aq)+H2(g)的△H=___ 。
(1)铜可采用如下方法制备:
火法炼铜:Cu2S+O2
 2Cu+SO2
2Cu+SO2湿法炼铜:CuSO4+Fe=FeSO4+Cu
上述两种方法中,铜元素均被
(2)印刷电路板上使用的铜需要回收利用。
方法一:用FeCl3溶液浸泡印刷电路板制备CuCl2·2H2O,实验室模拟回收过程如图:

①步骤1的离子方程式为
②步骤2中所加的氧化剂最适宜的是
A.HNO3 B.H2O2 C.KMnO4 D.氯水
写出加氧化剂相关的离子方程式
③步骤3的目的是使溶液的pH升高到4.2,此时Fe3+完全沉淀,可选用的试剂1是
④蒸发浓缩CuCl2溶液时,要滴加浓盐酸,目的是
(3)方法二:用H2O2和硫酸共同浸泡印刷电路板制备硫酸铜,其热化学方程式是:
Cu(s)+H2O2(l)+H2SO4(aq)=CuSO4(aq)+2H2O(l) △H1=-320kJ/mol
又知:2H2O2(l)=2H2O(l)+O2(g) △H2=-196kJ/mol
H2(g)+
 O2(g)=H2O(l) △H3=-286kJ/mol
O2(g)=H2O(l) △H3=-286kJ/mol则反应Cu(s)+H2SO4(aq)=CuSO4(aq)+H2(g)的△H=
您最近半年使用:0次
【推荐3】铁是人类较早使用的金属之一,运用铁及其化合物的知识,完成下列问题。印刷电路板(PCB)是用腐蚀液(FeCl3溶液)将覆铜板上的部分铜腐蚀掉而制得。一种制作PCB 并将腐蚀后废液(其中金属阳离子主要含 Fe3+、Cu2+、Fe2+ )回收再生的流程如图。
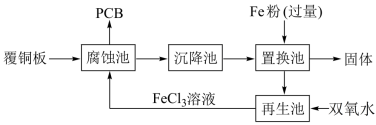
(1)腐蚀池中发生反应的化学方程式是_______ 。
(2)上述各池中,没有发生化学变化的是_______ 池。
(3)由置换池中得到固体的操作名称是_______ 。
(4)向再生池中通入Cl2也可以使废液再生,请写出通入氯气后再生池中发生的离子方程式:_______ 。相比Cl2,用双氧水的优点是_______ 。
(5)若取少量循环使用的氯化铁溶液于烧杯中,同时加入铁粉和铜粉。反应结束后,下列结果不可能出现的是_______。(填写编号)

(1)腐蚀池中发生反应的化学方程式是
(2)上述各池中,没有发生化学变化的是
(3)由置换池中得到固体的操作名称是
(4)向再生池中通入Cl2也可以使废液再生,请写出通入氯气后再生池中发生的离子方程式:
(5)若取少量循环使用的氯化铁溶液于烧杯中,同时加入铁粉和铜粉。反应结束后,下列结果不可能出现的是_______。(填写编号)
| A.有铜无铁 | B.有铁无铜 | C.铁、铜都有 | D.铁、铜都无 |
您最近半年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐1】某课外活动小组进行Fe(OH)3胶体的制备实验并检验其性质。
(1)制备方法:将饱和FeCl3溶液滴入沸水中。继续煮沸至液体变为___ 色,停止加热,可得到Fe(OH)3胶体,发生反应的化学方程式是___ ,提纯所制氢氧化铁胶体的常用方法是___ 。
(2)Fe(OH)3胶体稳定存在的主要原因是___ 。
A.胶粒小,不受重力作用 B.胶粒带同种电荷
C.胶体具有丁达尔效应 D.胶粒能透过滤纸
(3)Fe(OH)3胶体区别于FeCl3溶液最本质的特征是___ 。
A.Fe(OH)3胶体粒子的直径在1~100nm之间
B.Fe(OH)3胶体具有丁达尔效应
C.Fe(OH)3胶体是均一的分散系
D.Fe(OH)3胶体的分散质能透过滤纸
(1)制备方法:将饱和FeCl3溶液滴入沸水中。继续煮沸至液体变为
(2)Fe(OH)3胶体稳定存在的主要原因是
A.胶粒小,不受重力作用 B.胶粒带同种电荷
C.胶体具有丁达尔效应 D.胶粒能透过滤纸
(3)Fe(OH)3胶体区别于FeCl3溶液最本质的特征是
A.Fe(OH)3胶体粒子的直径在1~100nm之间
B.Fe(OH)3胶体具有丁达尔效应
C.Fe(OH)3胶体是均一的分散系
D.Fe(OH)3胶体的分散质能透过滤纸
您最近半年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
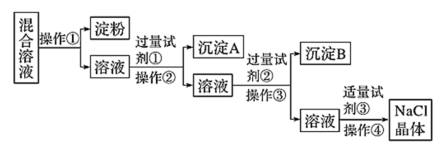
【推荐2】混合物分离和提纯常用下图装置进行,按要求回答下列问题:
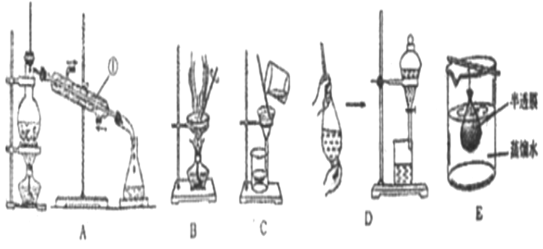
(1)仪器①的名称________________________ 。
(2)明胶是水溶性蛋白质混合物,溶于水形成胶体。分离明胶的水溶液与Na2CO3、Na2SO4的混合溶液应选用装置的为(用上图字母填写)____________________ 。如何证明SO42-已分离出来______________________ 。
(3)在装置D中加入10 mL碘水,然后再注入4 mL苯,盖好玻璃塞,按操作规则反复振荡后静置观察到的现象是:________________________ 。操作完毕后,为得到碘并回收苯可用______________ 法。

(1)仪器①的名称
(2)明胶是水溶性蛋白质混合物,溶于水形成胶体。分离明胶的水溶液与Na2CO3、Na2SO4的混合溶液应选用装置的为(用上图字母填写)
(3)在装置D中加入10 mL碘水,然后再注入4 mL苯,盖好玻璃塞,按操作规则反复振荡后静置观察到的现象是:
您最近半年使用:0次