下表为元素周期表的一部分,请参照元素在表中的位置,回答下列问题:
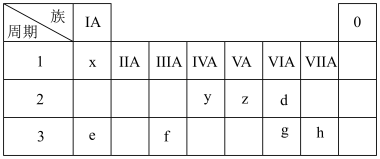
(1)比较d、e常见离子的半径大小(用化学式表示,下同):_______ >_______ ;
(2)比较g、h的最高价氧化物对应水化物的酸性强弱:_______ >_______ 。
(3)用电子式表示e、g组成的简单化合物的形成过程:_______ 。
(4)下列说法不正确的是_______。
(5)由表中两种元素的原子按 组成的常见液态化合物
组成的常见液态化合物 的稀溶液易被
的稀溶液易被 催化分解,查阅资料可知:在催化过程中发生了两步氧化还原反应,第一步反应中
催化分解,查阅资料可知:在催化过程中发生了两步氧化还原反应,第一步反应中 表现还原性;第二步反应中
表现还原性;第二步反应中 表现氧化性;请写出第二步反应的离子方程式(Q用化学式表示)
表现氧化性;请写出第二步反应的离子方程式(Q用化学式表示)_______ 。
(6)上述元素可组成盐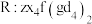 ,向盛有一定量
,向盛有一定量 盐溶液的烧杯中逐滴滴加
盐溶液的烧杯中逐滴滴加 溶液,沉淀物质的量随
溶液,沉淀物质的量随 溶液体积的变化如下图所示:
溶液体积的变化如下图所示:
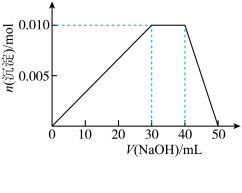
若向上述 盐溶液中改加
盐溶液中改加 溶液,充分反应后,溶液中产生沉淀的物质的量为
溶液,充分反应后,溶液中产生沉淀的物质的量为_______  。
。

(1)比较d、e常见离子的半径大小(用化学式表示,下同):
(2)比较g、h的最高价氧化物对应水化物的酸性强弱:
(3)用电子式表示e、g组成的简单化合物的形成过程:
(4)下列说法不正确的是_______。
A.最简单的氢化物的稳定性 |
B.最高价氧化物对应的水化物的碱性 |
| C.与y元素同主族的第四周期元素的单质是半导体材料 |
| D.y、h两元素组成的化合物中一定只含共价键 |
(5)由表中两种元素的原子按
 组成的常见液态化合物
组成的常见液态化合物 的稀溶液易被
的稀溶液易被 催化分解,查阅资料可知:在催化过程中发生了两步氧化还原反应,第一步反应中
催化分解,查阅资料可知:在催化过程中发生了两步氧化还原反应,第一步反应中 表现还原性;第二步反应中
表现还原性;第二步反应中 表现氧化性;请写出第二步反应的离子方程式(Q用化学式表示)
表现氧化性;请写出第二步反应的离子方程式(Q用化学式表示)(6)上述元素可组成盐
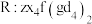 ,向盛有一定量
,向盛有一定量 盐溶液的烧杯中逐滴滴加
盐溶液的烧杯中逐滴滴加 溶液,沉淀物质的量随
溶液,沉淀物质的量随 溶液体积的变化如下图所示:
溶液体积的变化如下图所示:
若向上述
 盐溶液中改加
盐溶液中改加 溶液,充分反应后,溶液中产生沉淀的物质的量为
溶液,充分反应后,溶液中产生沉淀的物质的量为 。
。
更新时间:2024-01-27 10:34:12
|
相似题推荐
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐1】某同学为探究元素周期表中元素性质的递变规律,设计了如下系列实验:
(1)将大小相同的钠、镁、铝(除去氧化膜)分别投入到冷水中,反应最剧烈的是___________ ;分别向新制取的 沉淀中滴加稀盐酸和氢氧化钠溶液,结果沉淀都溶解,说明
沉淀中滴加稀盐酸和氢氧化钠溶液,结果沉淀都溶解,说明 是
是___________ 氢氧化物,其中 与氢氧化钠溶液反应的离子方程式为
与氢氧化钠溶液反应的离子方程式为___________ 。
(2)利用如图装置验证碳、硅、硫三种元素的非金属性强弱。
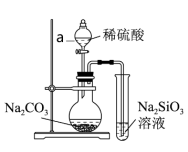
①图中仪器a的名称是___________ ,圆底烧瓶中发生反应的离子方程式为___________ 。
②能说明碳元素的非金属性比硅元素非金属性强的实验现象是___________ ,该实验能证明非金属性强弱,依据的原理是___________ 。
(1)将大小相同的钠、镁、铝(除去氧化膜)分别投入到冷水中,反应最剧烈的是
 沉淀中滴加稀盐酸和氢氧化钠溶液,结果沉淀都溶解,说明
沉淀中滴加稀盐酸和氢氧化钠溶液,结果沉淀都溶解,说明 是
是 与氢氧化钠溶液反应的离子方程式为
与氢氧化钠溶液反应的离子方程式为(2)利用如图装置验证碳、硅、硫三种元素的非金属性强弱。

①图中仪器a的名称是
②能说明碳元素的非金属性比硅元素非金属性强的实验现象是
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
【推荐2】硫酸亚铁广泛应用于临床医疗,主要用于治疗各种因素导致的缺铁性贫血,如慢性失血、营养不良等,同时也可以治疗铁吸收障碍、儿童或婴儿期需铁量增加等因素引起的缺铁性贫血。絮凝剂聚合氯化铝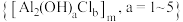 广泛用于废水处理。利用马矿的矿渣(成分为
广泛用于废水处理。利用马矿的矿渣(成分为 、
、 、
、 、
、 )制备绿矾(
)制备绿矾( )和聚合氯化铝的一种工艺流程如下:
)和聚合氯化铝的一种工艺流程如下:
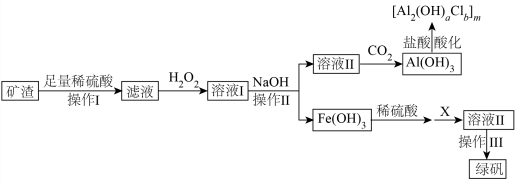
已知: 不溶于稀硫酸;硫酸铝和过量
不溶于稀硫酸;硫酸铝和过量 溶液反应生成
溶液反应生成 ;
; 的絮凝效果可用盐基度(盐基度
的絮凝效果可用盐基度(盐基度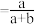 )衡量,当盐基度为0.60~0.85时,絮凝效果较好。
)衡量,当盐基度为0.60~0.85时,絮凝效果较好。
回答下列问题:
(1)操作I的名称是___________ ,需用到的玻璃仪器有___________ 。
(2)“滤液”中加入 发生的离子反应方程式是
发生的离子反应方程式是___________ ,发生该反应时可适当加热加快反应速率,但加热温度不宜过高,原因是___________ 。
(3)“溶液Ⅱ”若浓度较大,则通入过量 (
( 过量时,生成
过量时,生成 )不利于减少
)不利于减少 滤饼中的杂质,其原因是
滤饼中的杂质,其原因是___________ 。
(4)试剂“X”是___________ ,书写试剂“X”参与的化学反应方程式___________ 。
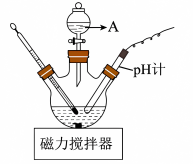
(5)“盐酸酸化”时的装置如图所示,仪器A的名称为___________ ,若要使产品盐基度为 ,则
,则
___________ 。
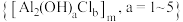 广泛用于废水处理。利用马矿的矿渣(成分为
广泛用于废水处理。利用马矿的矿渣(成分为 、
、 、
、 、
、 )制备绿矾(
)制备绿矾( )和聚合氯化铝的一种工艺流程如下:
)和聚合氯化铝的一种工艺流程如下:
已知:
 不溶于稀硫酸;硫酸铝和过量
不溶于稀硫酸;硫酸铝和过量 溶液反应生成
溶液反应生成 ;
; 的絮凝效果可用盐基度(盐基度
的絮凝效果可用盐基度(盐基度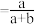 )衡量,当盐基度为0.60~0.85时,絮凝效果较好。
)衡量,当盐基度为0.60~0.85时,絮凝效果较好。回答下列问题:
(1)操作I的名称是
(2)“滤液”中加入
 发生的离子反应方程式是
发生的离子反应方程式是(3)“溶液Ⅱ”若浓度较大,则通入过量
 (
( 过量时,生成
过量时,生成 )不利于减少
)不利于减少 滤饼中的杂质,其原因是
滤饼中的杂质,其原因是(4)试剂“X”是
(5)“盐酸酸化”时的装置如图所示,仪器A的名称为
 ,则
,则

您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
【推荐3】X、Y、Z、M、G五种元素均为短周期主族元素,且原子序数依次增大。其中X、M同主族;元素Y原子的最外层电子数等于最内层电子数的一半;元素Z的最高价氧化物对应的水化物,与强碱或强酸均能反应生成盐和水;M的氧化物是形成酸雨的主要物质。回答下列问题:
(1)元素X在元素周期表中的位置是________ 。写出元素G的离子结构示意图_______ 。
(2)X、Y、M三种元素的简单离子半径由大到小的顺序为_______ (用离子符号表示)。
(3)M和G的最高价氧化物对应的水化物中,酸性强的是_______ (填写化学式)。
(4)写出元素Z的最高价氧化物对应的水化物与NaOH溶液反应的离子方程式_______ 。
(1)元素X在元素周期表中的位置是
(2)X、Y、M三种元素的简单离子半径由大到小的顺序为
(3)M和G的最高价氧化物对应的水化物中,酸性强的是
(4)写出元素Z的最高价氧化物对应的水化物与NaOH溶液反应的离子方程式
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐1】T、X、Y、Z、W五种短周期元素在周期表中的位置关系如图所示。
已知Z元素原子的最外层电子数是电子层数的2倍。
(1) 和
和 元素形成的常见化合物的化学式
元素形成的常见化合物的化学式___________
(2)元素T在元素周期表中的位置是___________
(3)X的简单氢化物的电子式为___________
(4)某同学为了比较碳元素和硅元素非金属性的强弱,用如图所示装置进行实验:

①M为___________ (填化学式),
②Na2SiO3溶液中发生反应的离子方程式___________ 。
(5) 的最高价氧化物对应水化物的浓溶液不稳定,受热可分解,分解产物中有2种气体单质,
的最高价氧化物对应水化物的浓溶液不稳定,受热可分解,分解产物中有2种气体单质,
其中一种是黄绿色,且当有28mol电子转移时,共产生2mol黄绿色气体,则该反应的化学方程式为___________ 。
| T | X | Y | |
| Z | W |
(1)
 和
和 元素形成的常见化合物的化学式
元素形成的常见化合物的化学式(2)元素T在元素周期表中的位置是
(3)X的简单氢化物的电子式为
(4)某同学为了比较碳元素和硅元素非金属性的强弱,用如图所示装置进行实验:

①M为
②Na2SiO3溶液中发生反应的离子方程式
(5)
 的最高价氧化物对应水化物的浓溶液不稳定,受热可分解,分解产物中有2种气体单质,
的最高价氧化物对应水化物的浓溶液不稳定,受热可分解,分解产物中有2种气体单质,其中一种是黄绿色,且当有28mol电子转移时,共产生2mol黄绿色气体,则该反应的化学方程式为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
【推荐2】下表列出了①~⑩十种元素在周期表中的位置:

请按要求回答下列问题:
(1)元素⑤的原子结构示意图为___________ ;元素②的最高价氧化物的电子式是____________ 。
(2)元素④在元素周期表中的位置为:_______________________ 。
(3)元素⑥的阳离子结构示意图为 ,其离子符号是
,其离子符号是__________ ;
(4)⑤、⑥、⑨三种元素原子半径由大到小的顺序是_______________ (填元素符号);这三种元素最高价氧化物对应水化物中碱性最强的是_______________ (填化学式)。
(5)③、④元素的简单氢化物的稳定性较弱的是_______________ (填化学式)。
(6)第3周期元素中,最高价氧化物对应水化物酸性最强的是________ (填化学式);
(7)元素②组成的某种有机物分子比例模型(填充模型)如图,该有机物的结构简式为_____________ ,所含的官能团的名称和结构分别为_____________ 和_____________ 。

(8)元素②组成的某烃分子的球棍模型如图,结构简式为_____________ ,该烃能使溴的四氯化碳溶液褪色,发生反应的化学方程式_____________________ 。

(9)元素⑦的最高价氧化物对应的水化物与氢氧化钠溶液反应的离子方程式:________________ 。

请按要求回答下列问题:
(1)元素⑤的原子结构示意图为
(2)元素④在元素周期表中的位置为:
(3)元素⑥的阳离子结构示意图为
 ,其离子符号是
,其离子符号是(4)⑤、⑥、⑨三种元素原子半径由大到小的顺序是
(5)③、④元素的简单氢化物的稳定性较弱的是
(6)第3周期元素中,最高价氧化物对应水化物酸性最强的是
(7)元素②组成的某种有机物分子比例模型(填充模型)如图,该有机物的结构简式为

(8)元素②组成的某烃分子的球棍模型如图,结构简式为

(9)元素⑦的最高价氧化物对应的水化物与氢氧化钠溶液反应的离子方程式:
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐3】Ⅰ.某同学设计了如下系列实验验证元素周期律。
(1)常温下,若将钠、钾、镁、铝各 分别投入到水中,与水反应最剧烈的是
分别投入到水中,与水反应最剧烈的是_______ ,(填元素符号,下同);若将钠、镁、铝各 分别投入到足量含同浓度的稀盐酸中,
分别投入到足量含同浓度的稀盐酸中,_______ 与盐酸反应产生的气体最多。
(2)仪器 的名称为
的名称为_______ ,干燥管D的作用为_______ 。
(3)若要证明非金属性: ,仪器
,仪器 中装有
中装有 溶液,仪器
溶液,仪器 中装有
中装有 固体,仪器
固体,仪器 中装有浓盐酸,观察到C中出现黄色浑浊,可证明非金属性:
中装有浓盐酸,观察到C中出现黄色浑浊,可证明非金属性:
_______ S(填“>”或“<”), 中反应的离子方程式为
中反应的离子方程式为_______ 。从环境保护的角度考虑,此装置缺少尾气处理装置,可用_______ 溶液吸收尾气(填化学式)。
(4)甲同学在仪器 中加盐酸,仪器
中加盐酸,仪器 中加
中加 ,仪器
,仪器 中装有
中装有 溶液。观察到
溶液。观察到 中溶液
中溶液_______ (填现象),甲同学认为该实验证明非金属性: 。但是乙同学认为盐酸具有挥发性,挥发的
。但是乙同学认为盐酸具有挥发性,挥发的 可进入仪器
可进入仪器 中干扰实验,应在两装置之间添
中干扰实验,应在两装置之间添_______ 溶液的洗气瓶除去 ;丙同学认为这种改进还是不能证明非金属性:
;丙同学认为这种改进还是不能证明非金属性: ,理由是
,理由是_______ 。
(1)常温下,若将钠、钾、镁、铝各
 分别投入到水中,与水反应最剧烈的是
分别投入到水中,与水反应最剧烈的是 分别投入到足量含同浓度的稀盐酸中,
分别投入到足量含同浓度的稀盐酸中,
(2)仪器
 的名称为
的名称为(3)若要证明非金属性:
 ,仪器
,仪器 中装有
中装有 溶液,仪器
溶液,仪器 中装有
中装有 固体,仪器
固体,仪器 中装有浓盐酸,观察到C中出现黄色浑浊,可证明非金属性:
中装有浓盐酸,观察到C中出现黄色浑浊,可证明非金属性:
 中反应的离子方程式为
中反应的离子方程式为(4)甲同学在仪器
 中加盐酸,仪器
中加盐酸,仪器 中加
中加 ,仪器
,仪器 中装有
中装有 溶液。观察到
溶液。观察到 中溶液
中溶液 。但是乙同学认为盐酸具有挥发性,挥发的
。但是乙同学认为盐酸具有挥发性,挥发的 可进入仪器
可进入仪器 中干扰实验,应在两装置之间添
中干扰实验,应在两装置之间添 ;丙同学认为这种改进还是不能证明非金属性:
;丙同学认为这种改进还是不能证明非金属性: ,理由是
,理由是
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐1】表中列出了①~⑨九种元素在周期表中的位置:
请按要求回答下列问题。
(1)元素③的元素名称是______ ,其在周期表中所处位置______ ;从元素原子得失电子的角度看,元素⑨的单质应具有______ 性(填“氧化”或“还原”)。
(2)④、⑧的氢化物稳定性由强到弱的顺序是______ (用化学式表示)。
(3)元素⑨的原子结构示意图是_____ ;其与元素⑤形成的化合物的电子式是______ 。
(4)这些元素的最高价氧化物中属于两性氧化物的是______ (填写化学式);它与⑤的最高价氧化物对应的水化物反应的离子方程式是_____ 。
| IA | ||||||||
| 1 | ① | IIA | IIIA | IVA | VA | VIA | VIIA | |
| 2 | ② | ③ | ④ | |||||
| 3 | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ | |||
(1)元素③的元素名称是
(2)④、⑧的氢化物稳定性由强到弱的顺序是
(3)元素⑨的原子结构示意图是
(4)这些元素的最高价氧化物中属于两性氧化物的是
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐2】有周期表序数前20 的A、B、C、D、E五种元素,原子序数E<C<D<A<B;E原子是最外电子层有4个电子;A-离子和B+离子的核外电子层结构相同;D的气态氢化物的化学式为H2D,D在其最高价氧化物中的质量分数为40%,且D原子核内质子数和中子数相等;C的原子序数比D少5,比B少8。
(1)各元素的名称为A_____ 、B_____ 、C_____ 、D_____ 、E_____ 。
(2)D元素位于第____ 周期____ 族。
(3)五种元素最高价氧化物的水化物中,酸性最强的是___ (写化学式下同),碱性最强的是____ 。
(4)写出C元素的单质与水反应的离子方程式______ 。
(5)写出B元素的氧化物的电子式________ 。
(6)写出E元素的氢化物的结构式________ 。
(1)各元素的名称为A
(2)D元素位于第
(3)五种元素最高价氧化物的水化物中,酸性最强的是
(4)写出C元素的单质与水反应的离子方程式
(5)写出B元素的氧化物的电子式
(6)写出E元素的氢化物的结构式
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐3】A、B、C、D、E 均为短周期主族元素,其原子序数依次增大。其中 A 元素 原子核内只有 1 个质子;A 与 C,B 与 D 分别同主族; B、D 两元素原子序数 之和是 A、C 两元素原子序数之和的 2 倍。请回答下列问题:
(1)由上述元素组成的下列物质中属于非电解质的是________ (填字母编号)。
a.A2B b.E2 c.DB2 d.C2DB3
(2)B元素在元素周期表中的位置为________ ;化合物 C2B2 中含有的化学键类型是________ ;化合物C2B中两种离子的半径大小关系为________ <________ (填离子符号)。
(3)实验室中欲选用下列装置制取并收集纯净干燥的E2气体。

①实验中应选用的装置为________ (按由左到右的连接顺序填写);
②装置A中发生反应的化学方程式为________ 。
(1)由上述元素组成的下列物质中属于非电解质的是
a.A2B b.E2 c.DB2 d.C2DB3
(2)B元素在元素周期表中的位置为
(3)实验室中欲选用下列装置制取并收集纯净干燥的E2气体。

①实验中应选用的装置为
②装置A中发生反应的化学方程式为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
【推荐1】下表为元素周期表的一部分。请参照元素①~⑨在表中的位置,用相应化学用语回答下列问题:

(1)画出表中形成化合物种类最多的元素的原子结构示意图___________ ;考古工作者利用该元素的一种核素测定一些文物的年代,这种核素的原子符号为___________ 。写出该元素与原子半径最小的原子形成的10电子分子的结构式___________ ,上述分子的空间结构呈___________ 形。
(2)写出①③两种元素形成的18电子微粒的电子式___________ 。
(3)③⑦⑨的最高价氧化物对应水化物的酸性由强到弱的顺序为___________ (填离子符号)④⑤⑥⑧形成的简单离子半径由大到小的顺序为___________ (填离子符号),用电子式表示⑤和⑧形成化合物的过程___________ 。
(4)有两种化合物A和B都由①④⑤⑧四种元素组成,若A与B在水溶液中能发生离子反应、则该反应的离子方程式为___________ 。

(1)画出表中形成化合物种类最多的元素的原子结构示意图
(2)写出①③两种元素形成的18电子微粒的电子式
(3)③⑦⑨的最高价氧化物对应水化物的酸性由强到弱的顺序为
(4)有两种化合物A和B都由①④⑤⑧四种元素组成,若A与B在水溶液中能发生离子反应、则该反应的离子方程式为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
【推荐2】下表为元素周期表的一部分,回答下列问题。
(1)写出单质⑥与强碱水溶液反应的离子方程式:__________________ 。
(2)关于⑩所在主族的单质及化合物的叙述错误的是________(填字母)
(3)⑤与⑨可以形成________ (填“共价”或“离子”)化合物,用电子式表示其形成过程为________ 。
(4)为了探究元素②、③、⑦的非金属性强弱,该兴趣小组又设计如下装置, 、稀盐酸、碳酸钙、
、稀盐酸、碳酸钙、 溶液、饱和
溶液、饱和 溶液,
溶液,
已知 不溶于水。据此回答以下问题。
不溶于水。据此回答以下问题。
分液漏斗内装入的试剂为________ ,B中装入的试剂为________ ,烧杯C中发生反应的离子方程式为________________________________ 。(已知硅酸钠溶液足量)
ⅠA | 0 | |||||||
1 | ① | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | |
2 | ② | ③ | ④ | |||||
3 | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ | ⑩ |
(2)关于⑩所在主族的单质及化合物的叙述错误的是________(填字母)
| A.从上到下,单质颜色越来越深,熔、沸点越来越高 |
| B.单质均可与水发生反应生成两种酸 |
C.单质均具有强氧化性,能将Fe氧化成 |
| D.氢化物均易溶于水,且均为强酸 |
(4)为了探究元素②、③、⑦的非金属性强弱,该兴趣小组又设计如下装置,

 、稀盐酸、碳酸钙、
、稀盐酸、碳酸钙、 溶液、饱和
溶液、饱和 溶液,
溶液,已知
 不溶于水。据此回答以下问题。
不溶于水。据此回答以下问题。分液漏斗内装入的试剂为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
【推荐3】如图为元素周期表的一部分,参照元素①~⑩在表中的位置,回答下列问题:
(1)写出元素锗(Ge,原子序数32)在元素周期表中的位置______ 。
(2)第三周期中非金属性最强的元素的原子形成简单离子的结构示意图为______ 。
(3)③⑦⑧最高价氧化物对应水化物酸性由强到弱的顺序为(填化学式)______ 。
(4)写出②的单质在足量④的单质中燃烧产物的电子式______ 。用电子式表示⑤和⑩组成简单化合物的形成过程______ 。
(5)④和⑨的单质均能与 反应生成
反应生成 型化合物,请判断这两种
型化合物,请判断这两种 型化合物的热稳定性
型化合物的热稳定性______ (填化学式)。
(6)由表中①、③、④、⑥、⑩元素形成的常见物质Z、M、N可发生以下反应:

i.M中所含的化学键种类为______ (填字母)。
a.离子键 b.极性共价键 c.非极性共价键
ⅱ.生成Z和M的离子方程式______ 。
ⅲ.Z→N的化学方程式______ 。
族 周期 | ⅠA | 0 | ||||||
| 1 | ① | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | |
| 2 | ② | ③ | ④ | |||||
| 3 | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ | ⑩ | ||
(1)写出元素锗(Ge,原子序数32)在元素周期表中的位置
(2)第三周期中非金属性最强的元素的原子形成简单离子的结构示意图为
(3)③⑦⑧最高价氧化物对应水化物酸性由强到弱的顺序为(填化学式)
(4)写出②的单质在足量④的单质中燃烧产物的电子式
(5)④和⑨的单质均能与
 反应生成
反应生成 型化合物,请判断这两种
型化合物,请判断这两种 型化合物的热稳定性
型化合物的热稳定性(6)由表中①、③、④、⑥、⑩元素形成的常见物质Z、M、N可发生以下反应:

i.M中所含的化学键种类为
a.离子键 b.极性共价键 c.非极性共价键
ⅱ.生成Z和M的离子方程式
ⅲ.Z→N的化学方程式
您最近一年使用:0次



