Ⅰ.实验小组利用传感器探究Na2CO3和NaHCO3的性质。
【查阅资料】pH越小,OH-浓度越小,溶液碱性越弱。
【实验过程】
【分析与解释】
(1)实验①中,溶解时吸收热量的物质是___________ 。
(2)实验②中,Na2CO3溶液和澄清石灰水反应的离子方程式为___________ ,OH-未参与该反应的实验证据是___________ 。
(3)实验②中,滴加NaHCO3溶液的pH变化与滴加Na2CO3溶液的有明显差异,原因是滴加NaHCO3溶液的烧杯中,参与反应的离子有___________ 。
(4)工业上制得的纯碱中常含有一定量的NaHCO3,取质量为a g的纯碱样品,充分加热后,质量减少b g,此样品中Na2CO3的质量分数___________ 。
Ⅱ.可用Cl2和Ca(OH)2制备漂粉精,漂粉精常用于游泳池的消毒,起消毒作用的是HClO,池水的酸碱性对漂粉精的消毒效果影响明显。
(5)写出制备漂粉精的化学方程式___________ 。
(6)若池水碱性过强,消毒作用会___________ (填“增强”或“减弱”)。
(7)若池水酸性过强,会刺激眼睛和皮肤。有时加入Na2CO3、NaHCO3以降低酸性,起到降低酸性作用的离子分别是___________ (填离子符号)。
【查阅资料】pH越小,OH-浓度越小,溶液碱性越弱。
【实验过程】
| 编号 | 实验操作 | 实验数据 |
| 实验① | 测量下述实验过程的温度变化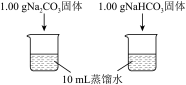 |  |
| 实验② | 测量下述实验过程的pH变化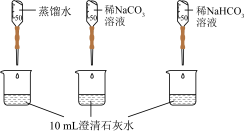 | 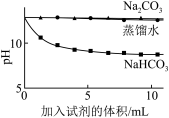 |
(1)实验①中,溶解时吸收热量的物质是
(2)实验②中,Na2CO3溶液和澄清石灰水反应的离子方程式为
(3)实验②中,滴加NaHCO3溶液的pH变化与滴加Na2CO3溶液的有明显差异,原因是滴加NaHCO3溶液的烧杯中,参与反应的离子有
(4)工业上制得的纯碱中常含有一定量的NaHCO3,取质量为a g的纯碱样品,充分加热后,质量减少b g,此样品中Na2CO3的质量分数
Ⅱ.可用Cl2和Ca(OH)2制备漂粉精,漂粉精常用于游泳池的消毒,起消毒作用的是HClO,池水的酸碱性对漂粉精的消毒效果影响明显。
(5)写出制备漂粉精的化学方程式
(6)若池水碱性过强,消毒作用会
(7)若池水酸性过强,会刺激眼睛和皮肤。有时加入Na2CO3、NaHCO3以降低酸性,起到降低酸性作用的离子分别是
更新时间:2024-01-27 11:34:52
|
相似题推荐
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐1】实验室常用二氧化锰与浓盐酸反应制备氯气,装置如图1所示,同时证明氯气的某些性质,装置如图2所示。按要求回答下列问题:

(1)制备实验开始时,先检查装置的气密性。接下来的操作依次是_____ (填字母)。
a 往烧瓶中加入 粉末 b 加热 c 分液漏斗中装入浓盐酸,旋开活塞往烧瓶中加入浓盐酸
粉末 b 加热 c 分液漏斗中装入浓盐酸,旋开活塞往烧瓶中加入浓盐酸
(2)写出烧瓶中反应的离子方程式___ 。
(3)制备反应会因盐酸浓度下降而停止,为测定反应残余液中盐酸的浓度,甲同学提出:与足量 溶液反应,称量生成的AgCl沉淀质量。方案不可行,原因是
溶液反应,称量生成的AgCl沉淀质量。方案不可行,原因是_____ 。
(4)图2中,浓硫酸的作用是____ ;试管A和B中出现的不同现象说明的事实是____ 。
(5)含氯气的尾气必须吸收处理,装置如图3所示。

烧杯中的吸收剂可选用___ (填序号)。
①饱和食盐水 ②澄清石灰水 ③饱和NaOH溶液
④饱和 溶液 ⑤饱和
溶液 ⑤饱和 溶液
溶液

(1)制备实验开始时,先检查装置的气密性。接下来的操作依次是
a 往烧瓶中加入
 粉末 b 加热 c 分液漏斗中装入浓盐酸,旋开活塞往烧瓶中加入浓盐酸
粉末 b 加热 c 分液漏斗中装入浓盐酸,旋开活塞往烧瓶中加入浓盐酸(2)写出烧瓶中反应的离子方程式
(3)制备反应会因盐酸浓度下降而停止,为测定反应残余液中盐酸的浓度,甲同学提出:与足量
 溶液反应,称量生成的AgCl沉淀质量。方案不可行,原因是
溶液反应,称量生成的AgCl沉淀质量。方案不可行,原因是(4)图2中,浓硫酸的作用是
(5)含氯气的尾气必须吸收处理,装置如图3所示。

烧杯中的吸收剂可选用
①饱和食盐水 ②澄清石灰水 ③饱和NaOH溶液
④饱和
 溶液 ⑤饱和
溶液 ⑤饱和 溶液
溶液
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐2】如图是实验室制备氯气并验证氯气性质的装置(其中夹持装置已省略)。

已知:装置A是氯气的发生装置,反应的化学方程式为 。
。
据此回答下列问题:
(1)装置B中饱和食盐水的作用是_________ 。
(2)装置B也是安全瓶,目的是监测实验进行时装置C中是否发生堵塞,请写出装置C中发生堵塞时装置B中的实验现象:_________ 。
(3)装置C的作用是验证氯气是否具有漂白性,则装置C中 、
、 处依次应放入的物质是
处依次应放入的物质是_________ (填序号)。
(4)装置D的作用是_________ ,写出其发生反应的离子方程式:_________ 。
(5)图中四条直线分别表示钠、镁、铝、铁和足量 反应时消耗金属的质量与反应消耗氯气的质量的关系,其中代表钠与
反应时消耗金属的质量与反应消耗氯气的质量的关系,其中代表钠与 反应的直线是
反应的直线是_________ ,代表铁与氯气反应的直线是_________ 。


已知:装置A是氯气的发生装置,反应的化学方程式为
 。
。据此回答下列问题:
(1)装置B中饱和食盐水的作用是
(2)装置B也是安全瓶,目的是监测实验进行时装置C中是否发生堵塞,请写出装置C中发生堵塞时装置B中的实验现象:
(3)装置C的作用是验证氯气是否具有漂白性,则装置C中
 、
、 处依次应放入的物质是
处依次应放入的物质是| 序号 |  |  | 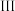 |
| a | 干燥的有色布条 | 碱石灰 | 湿润的有色布条 |
| b | 干燥的有色布条 | 无水硫酸铜 | 湿润的有色布条 |
| c | 湿润的有色布条 | 浓硫酸 | 干燥的有色布条 |
| d | 湿润的有色布条 | 无水氯化钙 | 干燥的有色布条 |
(4)装置D的作用是
(5)图中四条直线分别表示钠、镁、铝、铁和足量
 反应时消耗金属的质量与反应消耗氯气的质量的关系,其中代表钠与
反应时消耗金属的质量与反应消耗氯气的质量的关系,其中代表钠与 反应的直线是
反应的直线是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐3】次氯酸溶液是常用的消毒剂,可利用一氧化二氯(Cl2O,可通过Cl2与潮湿的Na2CO3反应制得)与水反应得到,实验装置如图所示(夹持装置已略)。
Cl2O的部分性质如下表:

(1)盛装浓盐酸的仪器名称为___________ ,装置A中发生反应的离子方程式为___________ 。
(2)装置B中饱和食盐水的作用是___________ ,装置C中多孔球泡和搅拌棒的作用是___________ 。
(3)装置C的水槽中水温最好控制在___________ (填标号),原因是___________ 。
A.0℃~3℃ B.10℃~20℃ C.40℃~50℃
(4)装置C中潮湿的Cl2与Na2CO3发生反应:______ (请配平该方程式)
___________Na2CO3+___________Cl2+___________H2O ___________NaHCO3+___________Cl2O+___________NaCl。
___________NaHCO3+___________Cl2O+___________NaCl。
(5)装置D中所得的溶液应保存在棕色试剂中并避免光照,长时间不避光保存,该溶液会变质。检验该溶液是否完全变质的操作及现象是___________ 。
Cl2O的部分性质如下表:
| 物理性质 | 常温下,具有强烈刺激性气味的黄棕色气体;熔点:﹣116℃;沸点:3.8℃ |
| 化学性质 | Cl2O极易溶于水并与水反应生成HClO,42℃以上分解为Cl2和O2;强氧化性,与有机物、还原剂接触或浓度过高时会发生爆炸 |

(1)盛装浓盐酸的仪器名称为
(2)装置B中饱和食盐水的作用是
(3)装置C的水槽中水温最好控制在
A.0℃~3℃ B.10℃~20℃ C.40℃~50℃
(4)装置C中潮湿的Cl2与Na2CO3发生反应:
___________Na2CO3+___________Cl2+___________H2O
 ___________NaHCO3+___________Cl2O+___________NaCl。
___________NaHCO3+___________Cl2O+___________NaCl。(5)装置D中所得的溶液应保存在棕色试剂中并避免光照,长时间不避光保存,该溶液会变质。检验该溶液是否完全变质的操作及现象是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐1】实验室以石灰乳和氯气为原料制备漂白粉的过程如下:在烧瓶和烧杯中(实验装置如图1)均加入一定量石灰乳和水,搅拌,通入氯气和空气混合气体,反应20min。停止通入气体,充分搅拌,取出糊状物,避光,晾干,密封保存。
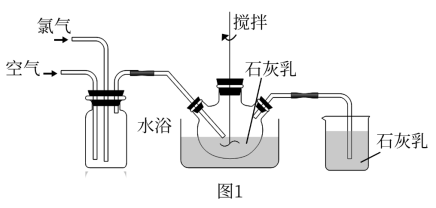
(1)石灰乳和氯气反应的化学方程式为___________ 。
(2)图1中通入空气的目的是___________ ,烧杯中石灰乳的作用是___________ 。
(3)石灰乳吸收氯气放出热量。实验中控温的方法是___________ 。
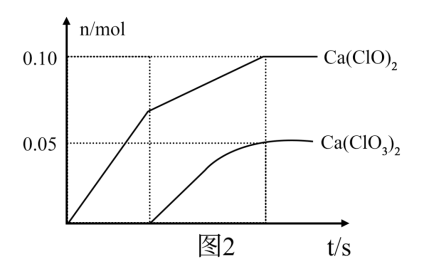
(4)在不控温的条件下,石灰乳吸收氯气的产物随时间的变化如图2所示。则制备漂白粉过程中发生的副反应的化学方程式为___________ 。

(1)石灰乳和氯气反应的化学方程式为
(2)图1中通入空气的目的是
(3)石灰乳吸收氯气放出热量。实验中控温的方法是
(4)在不控温的条件下,石灰乳吸收氯气的产物随时间的变化如图2所示。则制备漂白粉过程中发生的副反应的化学方程式为

您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐2】回答下列问题:
(1)在某防空防灾演习现场,模拟一起大客车与一辆装有氯气的槽罐车发生追尾事故,造成槽罐翻落、氯气泄漏。人防办立即指挥专业救援队在事发地点,测定风向,进行事故处置,引导大客车上的乘客___________。(填序号)
(2)如图所示,将氯气依次通过盛有干燥有色布条的广口瓶A和盛有潮湿有色布条的广口瓶B,可观察到布条褪色的是___________ (填A或B)。
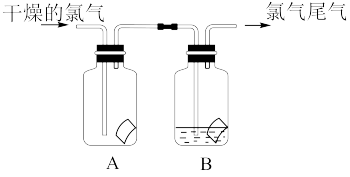
(3)为防止氯气尾气污染空气,根据氯气的性质,可用 溶液吸收多余的氯气,原理是
溶液吸收多余的氯气,原理是___________ (用离子方程式表示)。根据这一原理,工业上常用廉价的石灰乳吸收工业氯气尾气制得漂白粉,漂白粉的有效成分是___________ (填化学式)
(4)漂粉精常用于游泳池的消毒,起消毒作用的是 。漂粉精在水中释放
。漂粉精在水中释放 的途径如下:
的途径如下:
途径一:
途径二: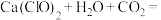 ___________+___________(把反应补充完整)
___________+___________(把反应补充完整) ___________
(5)池水的酸碱性对漂粉精的消毒效果影响明显。
①池水碱性过强,杀毒作用会___________ 。(填“增强”或“减弱”)
②池水酸性过强,会刺激眼睛和皮肤。有时加入 、
、 以降低酸性,起到降低酸性作用的离子分别是
以降低酸性,起到降低酸性作用的离子分别是___________ 。(填离子符号)
(1)在某防空防灾演习现场,模拟一起大客车与一辆装有氯气的槽罐车发生追尾事故,造成槽罐翻落、氯气泄漏。人防办立即指挥专业救援队在事发地点,测定风向,进行事故处置,引导大客车上的乘客___________。(填序号)
| A.顺风向高处转移 | B.顺风向低处转移 |
| C.逆风向高处转移 | D.逆风向低处转移 |

(3)为防止氯气尾气污染空气,根据氯气的性质,可用
 溶液吸收多余的氯气,原理是
溶液吸收多余的氯气,原理是(4)漂粉精常用于游泳池的消毒,起消毒作用的是
 。漂粉精在水中释放
。漂粉精在水中释放 的途径如下:
的途径如下:途径一:

途径二:
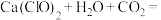 ___________+___________(把反应补充完整)
___________+___________(把反应补充完整) (5)池水的酸碱性对漂粉精的消毒效果影响明显。
①池水碱性过强,杀毒作用会
②池水酸性过强,会刺激眼睛和皮肤。有时加入
 、
、 以降低酸性,起到降低酸性作用的离子分别是
以降低酸性,起到降低酸性作用的离子分别是
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
解题方法
【推荐3】用 氧化HCl,可提高效益,减少污染,其反应的热化学方程式为
氧化HCl,可提高效益,减少污染,其反应的热化学方程式为
 。
。
(1)传统上用 氧化HCl可通过如图1所示的催化循环实现,其中反应①为
氧化HCl可通过如图1所示的催化循环实现,其中反应①为
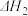 ,则反应②生成
,则反应②生成 的热化学方程式为
的热化学方程式为__________ (反应热用含 和
和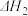 的代数式表示)
的代数式表示)

(2)新型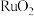 催化剂对
催化剂对 氧化HCl的反应具有更好的催化活性。
氧化HCl的反应具有更好的催化活性。
①实验测得在一定压强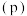 下,HCl的平衡转化率
下,HCl的平衡转化率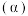 与温度、时间的变化曲线如图2,则
与温度、时间的变化曲线如图2,则
__________ (填“>”“=”或“<”)0;在温度为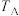 和
和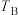 对应的平衡常数
对应的平衡常数 和
和 中,较大的是
中,较大的是__________ 。
②下列措施中,有利于提高HCl的平衡转化率的有__________ (填标号)。
A.增大n(HCl) B.增大 C.使用更好的催化剂 D.移去
C.使用更好的催化剂 D.移去
(3)一定条件下测得反应过程中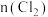 的数据如下:
的数据如下:
计算 内以
内以 的物质的量变化表示的反应速率
的物质的量变化表示的反应速率___________ (以 为单位)。
为单位)。
(4) 用途广泛,写出用
用途广泛,写出用 制备漂白粉的化学方程式:
制备漂白粉的化学方程式:___________ 。
 氧化HCl,可提高效益,减少污染,其反应的热化学方程式为
氧化HCl,可提高效益,减少污染,其反应的热化学方程式为
 。
。(1)传统上用
 氧化HCl可通过如图1所示的催化循环实现,其中反应①为
氧化HCl可通过如图1所示的催化循环实现,其中反应①为
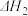 ,则反应②生成
,则反应②生成 的热化学方程式为
的热化学方程式为 和
和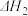 的代数式表示)
的代数式表示)
(2)新型
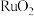 催化剂对
催化剂对 氧化HCl的反应具有更好的催化活性。
氧化HCl的反应具有更好的催化活性。①实验测得在一定压强
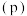 下,HCl的平衡转化率
下,HCl的平衡转化率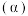 与温度、时间的变化曲线如图2,则
与温度、时间的变化曲线如图2,则
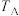 和
和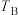 对应的平衡常数
对应的平衡常数 和
和 中,较大的是
中,较大的是②下列措施中,有利于提高HCl的平衡转化率的有
A.增大n(HCl) B.增大
 C.使用更好的催化剂 D.移去
C.使用更好的催化剂 D.移去
(3)一定条件下测得反应过程中
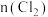 的数据如下:
的数据如下: | 0 | 2.0 | 4.0 | 6.0 | 8.0 |
 | 0 | 1.8 | 3.7 | 5.4 | 7.2 |
 内以
内以 的物质的量变化表示的反应速率
的物质的量变化表示的反应速率 为单位)。
为单位)。(4)
 用途广泛,写出用
用途广泛,写出用 制备漂白粉的化学方程式:
制备漂白粉的化学方程式:
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐1】某校化学课外小组为了鉴别碳酸钠和碳酸氢钠两种白色固体,用不同的方法做了以下实验,如图Ⅰ~Ⅳ所示。
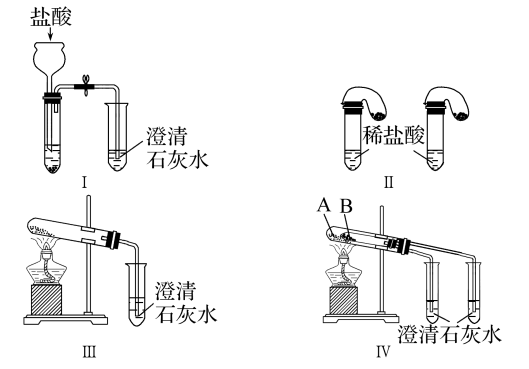
(1)图Ⅰ、Ⅱ所示实验能够达到实验目的的是(填装置序号)_______ ;
(2)图Ⅲ、Ⅳ所示实验均能鉴别这两种物质,其反应的化学方程式为__________________________ ,______________________ ;
(3)若用实验Ⅳ验证碳酸钠和碳酸氢钠的稳定性,则试管B中装入的固体最好是_______ ;
(4)另有两瓶溶液,已知分别是等物质的量浓度的K2CO3和NaHCO3,请你写出两种不同的鉴别方法。(写出简要操作、现象和结论)
①___________________ 。
②___________________ 。

(1)图Ⅰ、Ⅱ所示实验能够达到实验目的的是(填装置序号)
(2)图Ⅲ、Ⅳ所示实验均能鉴别这两种物质,其反应的化学方程式为
(3)若用实验Ⅳ验证碳酸钠和碳酸氢钠的稳定性,则试管B中装入的固体最好是
(4)另有两瓶溶液,已知分别是等物质的量浓度的K2CO3和NaHCO3,请你写出两种不同的鉴别方法。(写出简要操作、现象和结论)
①
②
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐2】某实验小组欲探究 和
和 的性质,发现实验室里盛放两种固体的试剂瓶丢失了标签。于是他们先对固体A、B进行鉴别,再通过实验进行性质探究。
的性质,发现实验室里盛放两种固体的试剂瓶丢失了标签。于是他们先对固体A、B进行鉴别,再通过实验进行性质探究。
(1)图1实验在加热过程中能观察到烧杯Ⅱ中有白色沉淀产生,则物质B为_______ (填化学式)。
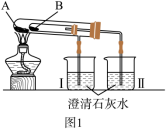
(2)称取两种固体各2g,分别加入两个小烧杯中,再各加10mL蒸馏水振荡,待固体充分溶解,恢复至室温,向所得溶液中各滴入2滴酚酞溶液。
①实验过程中发现 固体完全溶解,而
固体完全溶解,而 固体有剩余,由此可得出的结论是
固体有剩余,由此可得出的结论是_______ 。
②同学们在两烧杯中还观察到以下现象,其中盛放 的烧杯中出现的现象是
的烧杯中出现的现象是_______ (填字母)。
a.溶液温度下降 b.溶液温度升高 c.滴入酚酞后呈浅红色 d.滴入酚酞后呈红色
(3)如图2所示,在气密性良好的I和Ⅱ试管中分别加入足量等浓度、等体积的稀盐酸,将气球内的固体同时倒入试管中。

①两试管中均产生气体,_______ (填“I”或“Ⅱ”)的反应程度更为剧烈。
②反应结束后,气球均有膨胀,恢复至室温,_______ (填“I”或“Ⅱ”)的气球体积较大。
 和
和 的性质,发现实验室里盛放两种固体的试剂瓶丢失了标签。于是他们先对固体A、B进行鉴别,再通过实验进行性质探究。
的性质,发现实验室里盛放两种固体的试剂瓶丢失了标签。于是他们先对固体A、B进行鉴别,再通过实验进行性质探究。(1)图1实验在加热过程中能观察到烧杯Ⅱ中有白色沉淀产生,则物质B为

(2)称取两种固体各2g,分别加入两个小烧杯中,再各加10mL蒸馏水振荡,待固体充分溶解,恢复至室温,向所得溶液中各滴入2滴酚酞溶液。
①实验过程中发现
 固体完全溶解,而
固体完全溶解,而 固体有剩余,由此可得出的结论是
固体有剩余,由此可得出的结论是②同学们在两烧杯中还观察到以下现象,其中盛放
 的烧杯中出现的现象是
的烧杯中出现的现象是a.溶液温度下降 b.溶液温度升高 c.滴入酚酞后呈浅红色 d.滴入酚酞后呈红色
(3)如图2所示,在气密性良好的I和Ⅱ试管中分别加入足量等浓度、等体积的稀盐酸,将气球内的固体同时倒入试管中。

①两试管中均产生气体,
②反应结束后,气球均有膨胀,恢复至室温,
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐3】碳酸钠、碳酸氢钠与盐酸反应的比较。
(1)按上图要求完成实验:在两支试管中分别加入3 mL稀盐酸,将两个各装有少量等质量的碳酸钠、碳酸氢钠粉末的小气球套在两支试管的管口。将气球内的碳酸钠和碳酸氢钠同时倒入试管中,观察到的实验现象是_________ 。
(2)实验结论是_____________________ 。
(3)碳酸钠与盐酸反应的化学方程式是____________ ,离子方程式是_________________ 。
(4)碳酸氢钠与盐酸反应的化学方程式是____________ ,离子方程式是__________ 。

(1)按上图要求完成实验:在两支试管中分别加入3 mL稀盐酸,将两个各装有少量等质量的碳酸钠、碳酸氢钠粉末的小气球套在两支试管的管口。将气球内的碳酸钠和碳酸氢钠同时倒入试管中,观察到的实验现象是
(2)实验结论是
(3)碳酸钠与盐酸反应的化学方程式是
(4)碳酸氢钠与盐酸反应的化学方程式是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐1】下图是实验室制取Cl2并以Cl2为原料进行特定反应的实验:
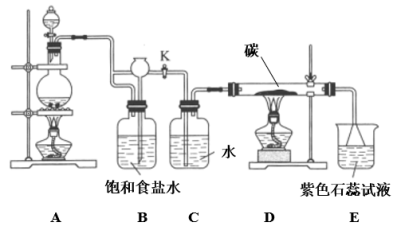
(1) A为氯气发生装置,写出该反应的化学方程式_______________________ 。
(2) 实验开始,打开弹簧夹K,先点燃____________ 处的酒精灯, 后点燃__________ 处的酒精灯。Cl2通过C瓶后进入D。D装置内盛有碳粉,加热时发生反应生成CO2和HCl(气),试写出D装置中反应的化学方程式_______________________ 。装置C的作用是____________________________________ 。
(3) E处石蕊试液的现象是_________________________________________ ;
(4) 若将E处溶液改为石灰水,反应过程的现象是___ 。(填序号)
A.有白色沉淀生成
B.无白色沉淀生成
C.先生成白色沉淀,然后沉淀消失
(5) D处反应完毕后,关闭弹簧夹K,移去酒精灯,由于余热的作用,A处仍有少量Cl2产生,此时B中的现象是______________ ; B的作用是_______________ 。

(1) A为氯气发生装置,写出该反应的化学方程式
(2) 实验开始,打开弹簧夹K,先点燃
(3) E处石蕊试液的现象是
(4) 若将E处溶液改为石灰水,反应过程的现象是
A.有白色沉淀生成
B.无白色沉淀生成
C.先生成白色沉淀,然后沉淀消失
(5) D处反应完毕后,关闭弹簧夹K,移去酒精灯,由于余热的作用,A处仍有少量Cl2产生,此时B中的现象是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐2】Ⅰ.有人设计了如图所示实验,以确认某混合气体中含有 和
和 。
。

实验中提供的试剂有:A.品红溶液 B. 溶液 C.浓硫酸 D.酸性
溶液 C.浓硫酸 D.酸性 溶液。
溶液。
试回答下列问题:
(1)写出图中①②③④装置盛放试剂的顺序为(将上述有关试剂的序号填入空格内,试剂可重复使用)___________ 。
(2)能确定混合气体中存在乙烯的现象是___________ 。
(3)乙烯与溴水反应的化学方程式为___________ ,该反应的反应类型为___________ 。
(4)关于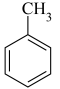 分子有下列问题:
分子有下列问题:
①分子中同一平面的原子最多有___________ 个。
②若用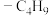 取代
取代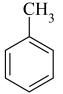 上的一个H原子,得到的有机物的同分异构体共有
上的一个H原子,得到的有机物的同分异构体共有___________ 种。
 和
和 。
。
实验中提供的试剂有:A.品红溶液 B.
 溶液 C.浓硫酸 D.酸性
溶液 C.浓硫酸 D.酸性 溶液。
溶液。试回答下列问题:
(1)写出图中①②③④装置盛放试剂的顺序为(将上述有关试剂的序号填入空格内,试剂可重复使用)
(2)能确定混合气体中存在乙烯的现象是
(3)乙烯与溴水反应的化学方程式为
(4)关于
 分子有下列问题:
分子有下列问题:①分子中同一平面的原子最多有
②若用
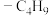 取代
取代 上的一个H原子,得到的有机物的同分异构体共有
上的一个H原子,得到的有机物的同分异构体共有
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
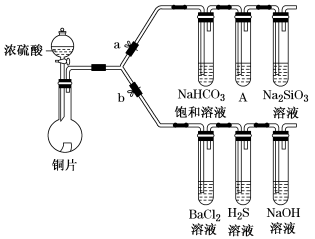
【推荐3】根据要求完成下列各小题实验目的。(a、b为弹簧夹,加热及固定装置已略去)
① 连接仪器、________ 、加药品后,打开a关闭b,然后滴入浓硫酸,加热。
② 铜与浓硫酸反应的化学方程式是_______ 。装置A中试剂是_______ 。
③ 能说明碳的非金属性比硅强的实验现象是_________ 。
(2)验证SO2的氧化性、还原性和酸性氧化物的通性。
① 在(1)①操作后打开b,关闭a。
② H2S溶液中有浅黄色浑浊出现,化学方程式是____ 。
③ BaCl2溶液中无明显现象,将其分成两份,分别滴加下列溶液,将产生的沉淀的化学式填入下表相应位置。
写出其中SO2显示还原性生成沉淀的离子方程式_________ 。
① 连接仪器、
② 铜与浓硫酸反应的化学方程式是
③ 能说明碳的非金属性比硅强的实验现象是
(2)验证SO2的氧化性、还原性和酸性氧化物的通性。
① 在(1)①操作后打开b,关闭a。
② H2S溶液中有浅黄色浑浊出现,化学方程式是
③ BaCl2溶液中无明显现象,将其分成两份,分别滴加下列溶液,将产生的沉淀的化学式填入下表相应位置。
| 滴加的溶液 | 氯水 | 氨水 |
| 沉淀的化学式 |
您最近一年使用:0次



