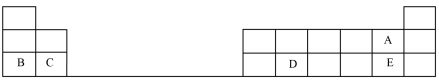
下图为元素周期表的一部分,用化学用语回答下列问题:
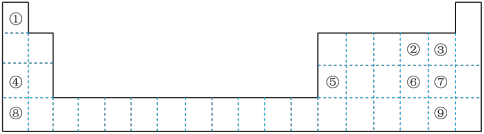
(1)请画出上述九种元素中非金属性最强的元素的原子结构示意图___________ 。
(2)④⑤⑧的阳离子中氧化性最强的是___________ (填离子符号)。
(3)上述元素中最高价氧化物对应的水化物中酸性最强的酸与氢氧化钠反应的化学方程式为___________ 。
(4)用电子式表示⑥和④形成化合物的过程___________ 。
(5)②和④形成原子个数比为1 :1的化合物中所含化学键类型为___________ 。
(6)现在含有元素硒(Se)的保健品开始进入市场,已知硒元素与氧元素同主族,比氧多2个电子层,则下列叙述中正确的是___________。
(7)①和④可形成AB型离子化合物,该离子化合物的电子式为___________ ,其与水反应放出气体的化学方程式为___________ 。

(1)请画出上述九种元素中非金属性最强的元素的原子结构示意图
(2)④⑤⑧的阳离子中氧化性最强的是
(3)上述元素中最高价氧化物对应的水化物中酸性最强的酸与氢氧化钠反应的化学方程式为
(4)用电子式表示⑥和④形成化合物的过程
(5)②和④形成原子个数比为1 :1的化合物中所含化学键类型为
(6)现在含有元素硒(Se)的保健品开始进入市场,已知硒元素与氧元素同主族,比氧多2个电子层,则下列叙述中正确的是___________。
| A.原子序数为34 |
| B.气态氢化物的还原性H2Se>H2S |
| C.SeO2不能与氢氧化钠反应 |
| D.SeO2既有氧化性又有还原性 |
(7)①和④可形成AB型离子化合物,该离子化合物的电子式为
更新时间:2024-01-25 13:14:29
|
相似题推荐
填空题
|
较易
(0.85)
名校
解题方法
【推荐1】用化学语言表达下列各微粒
(1)与氖原子电子层结构相同的-2价阴离子的电子式___________ 。
(2)第2层电子数为第1层、第3层电子数之和的原子的结构示意图___________ 。
(3)观察下列A、B、C、D、E五种粒子(原子或离子)的结构示意图,回答有关问题:
A.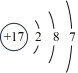 B.
B.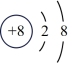 C.
C.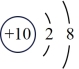 D.
D.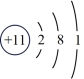 E.
E.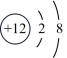
①属于离子结构示意图的是___________ (填编,下同)。
②属于金属元素的是___________ 。
③性质最稳定的原子是___________ ,最容易失去电子的原子是___________ ,最容易得到电子的原子是___________ 。
(1)与氖原子电子层结构相同的-2价阴离子的电子式
(2)第2层电子数为第1层、第3层电子数之和的原子的结构示意图
(3)观察下列A、B、C、D、E五种粒子(原子或离子)的结构示意图,回答有关问题:
A.
 B.
B.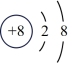 C.
C.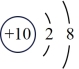 D.
D. E.
E.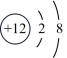
①属于离子结构示意图的是
②属于金属元素的是
③性质最稳定的原子是
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐2】我国的冶金工业十分发达,钢铁年产量已达到十亿吨,占世界产量的一半以上,同时有色金属产量也超过了七千万吨。
(1)铜是人类最早使用的金属,其电阻率小、延展性好,常用于制作电路板,在使用氯化铁溶液蚀刻铜制电路板时,发生反应的化学方程式为___________ 。
(2)铝与 溶液反应的化学方程式为
溶液反应的化学方程式为___________ ;铝的化学性质较活泼,但在空气中不会完全锈蚀,其原因是___________ 。
(3)电镀是一种常见的金属处理工艺,然而在生产过程中,电镀厂会产生大量的高毒性废水,将其直接排放会造成严重的污染。因此,废水的处理是电镀行业面临的主要问题之一。
①在电镀之前,镀件需要用酸性 溶液浸泡清洗。清洗废液的处理需要去除其中的悬浮颗粒物,并加入足量的
溶液浸泡清洗。清洗废液的处理需要去除其中的悬浮颗粒物,并加入足量的 固体,将
固体,将 还原为
还原为 ,则还原过程中发生反应的离子方程式为
,则还原过程中发生反应的离子方程式为___________ ,当有 被完全处理时,理论上需要加入
被完全处理时,理论上需要加入 的质量为
的质量为___________ 。
②为了减缓镀件表面的金属沉积速率,得到均匀、光滑的镀层,电解液中除重金属盐外,还需要加入剧毒的 。已知
。已知 中各原子均满足8电子稳定结构,则
中各原子均满足8电子稳定结构,则 的电子式为
的电子式为___________ 。在碱性的废电解液中通入氯气可以将 氧化,并生成两种无毒的氧化产物(其中一种为大气中占比最多的成分),则反应的离子方程式为
氧化,并生成两种无毒的氧化产物(其中一种为大气中占比最多的成分),则反应的离子方程式为___________ 。
(1)铜是人类最早使用的金属,其电阻率小、延展性好,常用于制作电路板,在使用氯化铁溶液蚀刻铜制电路板时,发生反应的化学方程式为
(2)铝与
 溶液反应的化学方程式为
溶液反应的化学方程式为(3)电镀是一种常见的金属处理工艺,然而在生产过程中,电镀厂会产生大量的高毒性废水,将其直接排放会造成严重的污染。因此,废水的处理是电镀行业面临的主要问题之一。
①在电镀之前,镀件需要用酸性
 溶液浸泡清洗。清洗废液的处理需要去除其中的悬浮颗粒物,并加入足量的
溶液浸泡清洗。清洗废液的处理需要去除其中的悬浮颗粒物,并加入足量的 固体,将
固体,将 还原为
还原为 ,则还原过程中发生反应的离子方程式为
,则还原过程中发生反应的离子方程式为 被完全处理时,理论上需要加入
被完全处理时,理论上需要加入 的质量为
的质量为②为了减缓镀件表面的金属沉积速率,得到均匀、光滑的镀层,电解液中除重金属盐外,还需要加入剧毒的
 。已知
。已知 中各原子均满足8电子稳定结构,则
中各原子均满足8电子稳定结构,则 的电子式为
的电子式为 氧化,并生成两种无毒的氧化产物(其中一种为大气中占比最多的成分),则反应的离子方程式为
氧化,并生成两种无毒的氧化产物(其中一种为大气中占比最多的成分),则反应的离子方程式为
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐3】(1)短周期中,金属性最强的元素是___________ (写元素符号,下同),非金属性最强的元素是___________ ,原子半径最小的元素是___________ 。
(2)寻找所需元素:在___________ 区域找到制造半导体材料,如___________ (写元素符号);
(3)写出下列物质的电子式:NaOH___________ ;N2___________ ;Na2O2___________ ;CO2___________ ;NH4Cl___________ ;HClO___________ 。
(4)现有下列几种微粒:1H、2H、3H、1H+、234U、235U、238U、40K、40Ca、Cl2、14N、14C,以上微粒分别属于___________ 种元素,互为同位素的原子分别为___________ 、___________ 。
(2)寻找所需元素:在
(3)写出下列物质的电子式:NaOH
(4)现有下列几种微粒:1H、2H、3H、1H+、234U、235U、238U、40K、40Ca、Cl2、14N、14C,以上微粒分别属于
您最近一年使用:0次
【推荐1】性质比较:
(1)半径比较Al___________ S(填“大于”、“等于”或“小于”,下同)
(2)第一电离能比较Mg___________ Al,解释原因___________
(3)酸性强弱比较HClO4、HClO3___________ ,解释原因___________
(1)半径比较Al
(2)第一电离能比较Mg
(3)酸性强弱比较HClO4、HClO3
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐2】回答下列问题
(1) 比
比 稳定,其原因是
稳定,其原因是___________ 。
(2)金刚石、硅和锗的熔点和硬度依次下降,从原子结构角度解释原因___________ 。
(3)水晶中___________ (填“是”或“否”)存在许多小分子 (1个
(1个 分子中含有一个硅原子与两个氧原子),从微观结构解释原因
分子中含有一个硅原子与两个氧原子),从微观结构解释原因__________ 。
(4)同为分子晶体,干冰中 的配位数(一个分子周围最邻近的分子的数目)大于冰中水分子的配位数,其原因是
的配位数(一个分子周围最邻近的分子的数目)大于冰中水分子的配位数,其原因是___________ 。
(1)
 比
比 稳定,其原因是
稳定,其原因是(2)金刚石、硅和锗的熔点和硬度依次下降,从原子结构角度解释原因
(3)水晶中
 (1个
(1个 分子中含有一个硅原子与两个氧原子),从微观结构解释原因
分子中含有一个硅原子与两个氧原子),从微观结构解释原因(4)同为分子晶体,干冰中
 的配位数(一个分子周围最邻近的分子的数目)大于冰中水分子的配位数,其原因是
的配位数(一个分子周围最邻近的分子的数目)大于冰中水分子的配位数,其原因是
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐1】元素在周期表中的位置反映了元素的原子结构和性质,矿物白云母是一种重要的化工原料,其化学式的氧化物形式为:K2O·3Al2O3·6SiO2·2H2O。就其组成元素完成下列填空:
(1)Al元素在元素周期表中的位置为_____ ,K2O的电子式为_____ 。
(2)上述元素中(Si、H除外),形成的简单离子的半径最小,该离子与过量氨水反应的离子方程式为_____ 。
(3)根据KH的存在,有人提议可把氢元素放在第ⅦA族,那么根据其最高正价与最低负价的绝对值相等,又可把氢元素放在周期表中的第_____ 族。
(4)某元素R与氧元素同主族,对延长人类寿命起着重要作用,被誉为“生命元素”。已知R元素的原子有4个电子层,则元素R的质子数是_____ 。
(1)Al元素在元素周期表中的位置为
(2)上述元素中(Si、H除外),形成的简单离子的半径最小,该离子与过量氨水反应的离子方程式为
(3)根据KH的存在,有人提议可把氢元素放在第ⅦA族,那么根据其最高正价与最低负价的绝对值相等,又可把氢元素放在周期表中的第
(4)某元素R与氧元素同主族,对延长人类寿命起着重要作用,被誉为“生命元素”。已知R元素的原子有4个电子层,则元素R的质子数是
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐2】下表为元素周期表的短周期部分,请参照元素①~⑧在表中的位置,用化学用语回答下列题:
(1)半径最小的元素是______________ ,金属性最强的元素是____________ ;(填元素符号)
(2)⑤和⑧两元素可形成化合物,灼烧该化合物时火焰颜色为___________ 色;
(3)元素⑧在周期表中的位置是__________________________ ;
(4)①和③两元素形成的化合物的电子式为__________________ ;
(5)①分别与②、③、④形成的化合物中,最稳定是(填写化学式)______________________ ;
(6)④、⑤、⑥三种元素形成的简单离子中,离子半径最大的是(填离子符号)__________________ ;
(7)②、③的最高价含氧酸的酸性强弱比较(用化学式表示)_____________________________ 。
① | |||||||
② | ③ | ④ | |||||
⑤ | ⑥ | ⑦ | ⑧ | ||||
(1)半径最小的元素是
(2)⑤和⑧两元素可形成化合物,灼烧该化合物时火焰颜色为
(3)元素⑧在周期表中的位置是
(4)①和③两元素形成的化合物的电子式为
(5)①分别与②、③、④形成的化合物中,最稳定是(填写化学式)
(6)④、⑤、⑥三种元素形成的简单离子中,离子半径最大的是(填离子符号)
(7)②、③的最高价含氧酸的酸性强弱比较(用化学式表示)
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐3】下表中阿拉伯数字(1、2…)是元素周期表中行或列的序号。请参照元素A~I在周期表中的位置,回答下列问题。
(1)B、C两元素中非金属性较强的是____ (写出元素名称),I元素在周期表中的位置是_____ 。
(2)表中某元素能形成两性氧化物,写出该氧化物溶于氢氧化钠溶液的离子反应方程式_______ 。
(3)表中某元素的单质在常温下为气态,该元素能与A~I中的一种元素构成原子个数比为1∶1和1∶2的两种共价化合物X和Y,请写出Y的电子式_____ ,该元素还能与A~I中的另一种元素以原子个数之比为1∶1和1∶2形成两种离子化合物Z和M,用电子式表示M的形成过程:____ 。
(4)表中某两种元素的气态单质可以形成燃料电池,其产物清洁无污染,请写出碱性环境中负极反应式_______ 。
| 1 | 2 | 13 | 14 | 15 | 16 | 17 | 18 | |
| 1 | A | |||||||
| 2 | B | C | D | E | ||||
| 3 | F | G | H | I |
(1)B、C两元素中非金属性较强的是
(2)表中某元素能形成两性氧化物,写出该氧化物溶于氢氧化钠溶液的离子反应方程式
(3)表中某元素的单质在常温下为气态,该元素能与A~I中的一种元素构成原子个数比为1∶1和1∶2的两种共价化合物X和Y,请写出Y的电子式
(4)表中某两种元素的气态单质可以形成燃料电池,其产物清洁无污染,请写出碱性环境中负极反应式
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐1】Ⅰ.根据下列6种符号回答问题:
①1H ②2H ③3H ④14C ⑤14N ⑥16O
(1)共有_____ 种核素,属于______ 种元素。
(2)互为同位素的是________ 。(填序号,下同)
(3)质量数相等的是______ ,中子数相等的是________ 。
II.现有6种物质: ①MgCl2 ②Cl2 ③SO2 ④K2CO3 ⑤Na2O2 ⑥NaOH
请根据下列标准,对上述物质进行分类(填序号):
(1)属于共价化合物的是_________ 。
(2)只含离子键的化合物是_________ 。
(3)含非极性共价键的离子化合物是_________ 。
①1H ②2H ③3H ④14C ⑤14N ⑥16O
(1)共有
(2)互为同位素的是
(3)质量数相等的是
II.现有6种物质: ①MgCl2 ②Cl2 ③SO2 ④K2CO3 ⑤Na2O2 ⑥NaOH
请根据下列标准,对上述物质进行分类(填序号):
(1)属于共价化合物的是
(2)只含离子键的化合物是
(3)含非极性共价键的离子化合物是
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐2】以下是中学化学中熟悉的物质:①NH4NO3 ②Cl2 ③HCl ④Na2O2 ⑤MgCl2 ⑥CO2 ⑦AlCl3,请回答下列问题:
(1)只含离子键的是_______ 。
(2)含极性键的离子化合物是_______ 。
(3)由极性键构成的非极性分子的是_______ 。
(4)“神舟”七号载人飞船内需要有一种化合物来吸收航天员呼出的CO2,你认为该物质应该是上述中的______ (填序号),用化学方程式来表示吸收原理:_______ 。
(5)羰基硫(COS)与CO2的结构相似,羰基硫(COS)分子的结构式为_______ 。
(6)NH4NO3中 的空间构型为
的空间构型为_______ 。
(1)只含离子键的是
(2)含极性键的离子化合物是
(3)由极性键构成的非极性分子的是
(4)“神舟”七号载人飞船内需要有一种化合物来吸收航天员呼出的CO2,你认为该物质应该是上述中的
(5)羰基硫(COS)与CO2的结构相似,羰基硫(COS)分子的结构式为
(6)NH4NO3中
 的空间构型为
的空间构型为
您最近一年使用:0次