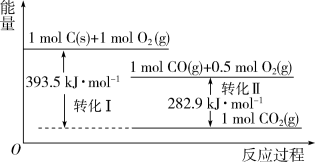
如图所示为NH4Cl的热循环过程,结合数据计算可得ΔH6(kJ·mol-1)为
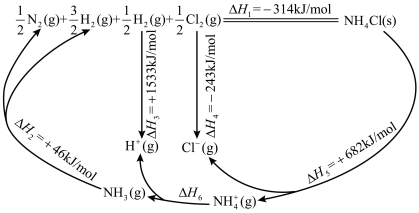

| A.–2332 | B.+248 | C.+876 | D.–1704 |
更新时间:2024-01-29 14:25:33
|
【知识点】 盖斯定律及其有关计算
相似题推荐
单选题
|
适中
(0.65)
名校
【推荐1】下列四幅图示所表示的信息与对应的叙述相符的是
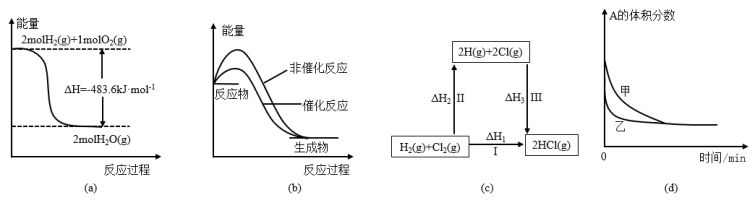

A.图(a)表示 与 与 发生反应过程中的能量变化,则 发生反应过程中的能量变化,则 的标准燃烧热为 的标准燃烧热为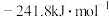 |
| B.图(b)表示某吸热反应分别在有、无催化剂的情况下反应过程中的能量变化 |
C.图(c)表示一定条件下 和 和 生成HCl的反应热与途径无关,则 生成HCl的反应热与途径无关,则 |
D.图(d)表示压强对可逆反应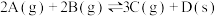 的影响,甲的压强大 的影响,甲的压强大 |
您最近一年使用:0次
【推荐2】符合如图所示的转化关系,且当X、Y、Z的物质的量相等时,存在焓变△H=△H1+△H2。满足上述条件的X、Y可能是
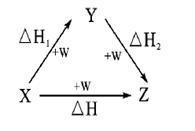
①C、CO ②S、SO2 ③Na、Na2O ④AlCl3、Al(OH)3⑤Fe、Fe(NO3)2 ⑥NaOH、Na2CO3

①C、CO ②S、SO2 ③Na、Na2O ④AlCl3、Al(OH)3⑤Fe、Fe(NO3)2 ⑥NaOH、Na2CO3
| A.①④⑤ | B.①②③ | C.①③④ | D.①③④⑤⑥ |
您最近一年使用:0次